ЗППП — это заболевания передающиеся половым путем. Возбудители ЗППП, как правило, попадают в организм человека в результате незащищенного полового контакта с носителем инфекции или больным человеком. На сегодняшний день известно около 20 инфекций, которые поражают в основном половые органы.
Синдром приобретенного иммунного дефицита (СПИД), гепатиты В или С, цитомегалия поражают практически все клетки человеческого организма.
При отсутствии должного лечения большинство ИППП приводят к другим хроническим воспалительным заболеваниям мочеполовой сферы.
Классификация ЗППП
Традиционно ЗППП подразделяют на:
1. классические венерические болезни:
1. сифилис,
2. гонорея,
3. шанкроид (мягкий шанкр);
4. лимфогранулематоз паховый;
5. гранулема венерическая.
2. инфекции, передающиеся половым путем, с преимущественным поражением половых органов:
1. мочеполовой хламидиоз;
2. мочеполовой трихомониаз;
3. кандидозные заболевания (вульвовагиниты и баланопоститы);
4. мочеполовой микоплазмоз;
5. генитальный герпес;
6. остроконечные бородавки;
7. генитальный контагиозный моллюск;
8. гарднереллез;
9. лобковый педикулез;
10. чесотка,
3. инфекции с преимущественным поражением других органов, способные передаваться половым путем (не относятся к венерическим болезням):
1. инфекция, вызываемая вирусом иммунодефицита человека;
2. гепатит В;
3. цитомегаловирусная инфекция.
А теперь подробнее о каждом…
Микоплазма — это микроорганизм, промежуточный между бактериями, грибками и вирусами. Паразитирует обычно на слизистых оболочках различных органов. У женщин вызывает воспаления матки, яичников, маточных труб, мочевого пузыря и почек, которые характеризуются обильными выделениями из половых путей, зудом, болями при мочеиспускании и половом акте. Мужчины обычно не испытывает неудобств, кроме слабых редких резей в процессе мочеиспускания, но данная инфекция может вызвать хронический простатит или воспаление почек.
Уреаплазма паразитирует на сперматозоидах, приводит к бесплодию у мужчин. Поражение организма на клеточном уровне вызывает преждевременное старение.
Генитальный герпес — это вирусная инфекция, основным симптомом которой являются болезненные пузырьки, на месте которых после их разрыва появляются красные мокнущие язвочки. Бывает бессимптомное вирусоносительство при сильных защитных свойствах иммунитета. Последствиями генитального герпеса могут стать бесплодие, эректильная дисфункция, хронические воспаления мочеполовых органов.
Хламидия — это микроорганизм, промежуточный между вирусами и бактериями. Передается половым путем, а также воздушно-капельным, контактным (в бане, бассейне). В течение одной — трех недель после заражения появляются выделения из половых путей, возможно кровотечение, боль в животе, жжение во время мочеиспускания, тошнота. Последствиями хламидиоза являются импотенция и бесплодие.
Кандидоз (молочница) — это инфекционное поражение слизистой влагалища, которое вызывается дрожжеподобными грибами. Молочница склонна к хроническому течению и частым рецидивам.
У женщин кандидоз вызывают воспаления наружных половых органов (вульвит) и влагалища (вагинит), может стать причиной появления уретрита, цистита; у мужчин — баланопостита, уретрита, простатита, эпидидимита, цистита.
Герпес и цитомегаловирус являются вирусами одной группы. Генитальный герпес — наиболее неприятный вид герпеса. Цитомегаловирус — заболевание, вызываемое вирусом семейства герпеса, которое поражает внутренние органы и нервную систему или протекает бессимптомно. Вирус может присутствовать в крови, в слюне, в молоке, поэтому возможны различные пути передачи вируса: воздушно-капельным путем, при переливании крови, а также половым путём. Герпес и цитомегаловирус опасны тем, что, попав в организм однажды, они остаются там на всю жизнь.
Синдром приобретенного иммунодефицита (СПИД) тоже относится к ЗППП. Причиной СПИДа является вирус иммунодефицита человека. Вначале заболевания симптомы практически отсутствуют. Позднее заболевание проявляется лихорадкой, повышением температуры, потерей веса, слабостью, повышенным потоотделением, усталостью. Через две — шесть недель после заражения вирусом увеличиваются лимфатические узлы. Незащищенный половой контакт любого вида — самый распространенный путь инфицирования СПИДом.
СПИДом можно заразиться во время стоматологических манипуляций, косметических процедур, во время переливания зараженной крови, инъекций зараженным шприцем. Возможен внутриутробный способ заражения плода от инфицированной матери. СПИД ведет к разрушению внутренних органов, поражению нервной системы — к смерти!
Сифилис вызывается бледной трепонемой, которая попадает в организм половым путем, а также во время бытового контакта с зараженными предметами быта или гигиены больного человека. Заражение новорожденных происходит от больной матери. Первичный сифилис характеризуется небольшой безболезненной язвой красного цвета на половых органах, во рту, в области ануса. Увеличиваются лимфатические узлы. Вторичный сифилис характеризуется сыпью и светлыми пятнами на коже, выпадением волос.
Гонорея возникает в результате заражения организма гонококком. Возможен половой и бытовой путь заражения. Гонорея характеризуется густыми обильными выделениями из наружных половых путей, жжением в процессе мочеиспускания, болями внизу живота. Гонорея может стать причиной импотенции и бесплодию.
Остроконечные кондиломы (генитальные бородавки) появляются вследствие заражения человека папилломавирусом. Папилломавирус человека имеет более 60 типов. Они поражают эпителий кожи и слизистых. Большинство бородавок регрессирует, но некоторые приобретают злокачественный характер.
Трихомониаз — распространенная инфекция, вызываемая простейшим жгутиковым паразитом, поражающая ежегодно около 200 млн. человек. Данное заболевание вызывает эректильную дисфункцию, бесплодие, преждевременные роды во время беременности. Трихомонады обитают у женщин во влагалище, у мужчин — в уретре и в простате. Трихомонады провоцируют рак.
Бактериальный вагиноз — это дисбактериоз влагалища, который возникает в результате дисбаланса микрофлоры влагалища, нормальная микрофлора замещается анаэробными микроорганизмами (Gardnerella vaginalis и Mycoplasma hominis).
Симптомы, лечение в Волгограде.

На сегодняшний день в список ИППП включены 31 наиболее часто встречаемых возбудителей: 15 видов бактерий, 10 видов вирусов, 3 вида простейших, 1 вид гриба и 2 вида эктопаразитов. Основным источником ИППП является больной или носитель инфекции, который может заразить своего партнера. При половом контакте передается следующие инфекций:
- гонорей;
- сифилиса;
- мягкого шанкра;
- венерического лимфогранулематоза;
- донованоза;
- ВИЧ – инфекции;
- вирусных гепатитов В, С, D;
- хламидиоза;
- микоплазмоза;
- уреаплазмоза;
- трихомониаза;
- гарнереллеза;
- генитального герпеса;
- остроконечной кондиломы;
- цитомегаловирусной инфекции;
- болезней кожи, передающихся половым путем (чесотка, лобковые вши, контагинозный моллюск).
Выделяют следующие репродуктивнозначимые мочеполовые инфекции:
- Trichomonas vaginalis
- Clamydia trachomatis
- Mycoplasma genitalium
- Nesseria gonorrhoeae
- Treponema pallidum
- Papillomavirus hominis(6;11;16;18;45)
- Hepatitis B, С, virus
- Mumps virus (>18 лет)
- Human immune deficiency virus
- Bacterii (enterobacteriaceae, enterocci, anaerobes, staphylococci, streptococci)
- Mycoplasma hominis
- Ureaplasma urealyticum T 960
- Ureaplasma parvum
- Candida albicans
- Herpes simplex virus I-II
- Cytomegalovirus
Если Вы имели новую половую связь и узнали, что сексуальный партнер болел ИППП, почувствовали характерные симптомы или просто сомневаетесь относительно отсутствия у Вас ИППП, необходимо пройти специальное медицинское обследование. Никогда не пытайтесь заниматься самолечением или пользоваться советами неспециалиста. Это может привести к хронизации воспалительного процесса и развитию осложнений. Самое печальное, что многие инфекции могут протекать скрыто. Человек не знает и не догадывается, что он болен. Он остается в неведении и может заразить своих партнеров. О том, что вы или ваш партнер больны, могут свидетельствовать следующие симптомы:
- воспаление в области половых органов;
- язвочки;
- пузырьки;
- бородавки;
- сыпь и налет на половых органах;
- выделения из половых органов;
- мочеиспускательного канала;
- сыпь на поверхности тела;
- не обоснованные подъемы температуры;
- желтушность кожи и белков глаз.
Лабораторная диагностика — это основное для назначения адекватного лечения. Современные методы диагностики ИППП: метод полимеразой цепной реакции (ПЦР), иммунофлюоресцентный метод (ПИФ), иммуноферментный анализ (ИФА), выделение возбудителей на клеточных культурах и др. чрезвычайно надежны (до 90%). Однако в условиях дефицита средств далеко не все лаборатории в нашей стране имеют достаточно качественные реактивы и оборудование. Другая проблема, не всегда удается выявить точно инфекционный возбудитель.
Лечить инфекции передаваемые половым путем согласно принятой в г. Рига Международного соглашения в 1990 году могут врачи: дерматовенеролог, уролог, гинеколог. Грамотно провести обследование, поставить диагноз и назначить системное, целенаправленное лечение может только квалифицированный специалист.
В основе правильно подобранного патогенетического лечения должно лежать пять основных правил:
- Антибактериальная/противовирусная терапия (зависит от возбудителя заболевания);
- Улучшение артериального притока и венозного оттока крови (это обеспечивает полноценную доставку антибактериальных/противовирусных средств к месту воспаления, восстановление прежних функций). Недостаток артериального кровоснабжения и венозный застой в области предстательной железы, отрицательно сказываются на течении воспалительного процесса, репродуктивной и эректильной функциях у мужчин;
- Улучшение оттока секрета предстательной железы и семенных пузырьков (может быть достигнуто путем сокращения мышц таза, промежности и мышечных волокон предстательной железы);
- Общая и местная иммунокоррекция;
- Комфорт и минимальные временные затраты, помноженные на высокую эффективность проводимой терапии.
Использование аппаратов электромагнитолазерной терапии, позволяет в комплексе достичь, все необходимые эффекты воздействия на больной орган: восстановить физиологические процессы, измененные заболеванием и активировать естественные защитные функции организма против патологии. Так как комбинация лазерной, магнитной и электротерапии обеспечивает одновременно противовоспалительный эффект, стимуляцию различных мышц, ликвидацию застойных явлений, улучшение лимфо- и кровотока. Лечебный эффект основан на биостимуляции и мобилизации имеющегося энергетического потенциала организма.
Успешно применяют магнитоинфракрасную лазерную терапию. Наиболее часто используют уретральное облучение. Возможно воздействие на область промежности и зону над лоном. Низкоинтенсивное лазерное излучение оказывает выраженное противоспалительное действие, стимулирует местный иммунитет, улучшает микроциркуляцию в очаге воспаления, действует на проницаемость сосудистой стенки, проявляет обезболивающий эффект. Внутривенное лазерное облучение крови (ВЛОК), является наиболее эффективной и универсальной методикой лазерной терапии. В отличие от местных процедур лазерной терапии, лечебный эффект обусловлен активацией системных лечебных механизмов всего организма, повышением эффективности функционирования систем кровоснабжения, иммунной, других органов и систем, а также всего организма в целом.
При хроническом воспалении, применяют электрофорез антибиотиков, уросептиков. Сила тока подбирается до появления легкого покалывания. Используется внутриорганный (уретральный, ректальный и уретроректальный) электрофорез с лекарственными веществами. При затяжном течении воспаления и нарастания признаков склероза в простаты — возможно проведение эндоуретрально электрофора с коллализином.
Широко применяют трансуретральную или трансректальную термотерапия или гипертермия. При лечении инфекций передаваемых половым путем, требуется поверхностный прогрев слизистой уретры и предстательной железы на глубину не более 5 мм с целью санации урогенитального тракта или обеспечения лучших условий для последующей местной лекарственной терапии. Обеспечивается прогрев уретры и железы по трансуретральной или трансректальной методике равномерно по длине уретры с плавным подъемом температуры от 39 до 45°С и автоматическим контролем ее непосредственно в уретре или прямой кишке. Показания к применению гипертермии являются: хронические уретриты, простатиты, кольпиты, цервициты, ганглионевриты.
При использовании магниотерапии появляется возможность одновременного использования уретрального и ректального нагрева на фоне воздействия бегущим магнитным полем. Такая возможность позволяет оптимизировать воздействие и сократить сроки лечения с максимальным процентом благоприятных исходов даже в запущенных случаях. Магнитотерапия оказывает противоспалительное и болеутоляющее действие, нормализует кровообращение, изменяет течение окислительно-восстановительных и тканевых ферментативных процессов, создает условия для более эффективного действия антибиотиков на воспалительный процесс.
Самой частой причиной является повторное заражение, которое наступает в результате новой половой связи во время лечения, отсутствия лечения половой партнерши, при половом контакте без использования презерватива супружеской парой, проходящей лечение. Еще причинами неудачного лечения ИППП является неправильная диагностика, неверно подобранный антибактериальный препарат, нарушение лечения пациентом и устойчивость инфекции к антибиотику.
Контроль излеченности инфекций проводится не ранее чем через 2 недели после завершения приема антибиотика. Пациент должен знать, что некоторые симптомы заболевания могут оставаться в течение нескольких недель и даже месяцев после успешного лечения. Возобновлять половую жизнь без презерватива с постоянной половой партнершей (партнером) можно только после контрольного обследования, показавшего отсутствие инфекций и воспалительного процесса.
Проводить плановый осмотр необходимо не реже 1 раза в полгода. Нельзя самостоятельно принимать лекарственные препараты. Бесконтрольный прием антибиотиков и противовоспалительных препаратов искажает клиническую картину, переводит заболевание в бессимптомную форму, приводит к хронизации процесса и тяжелым осложнениям. Инфекция, передаваемая половым путем,- это проблема, которая касается каждого. Оптимальная тактика – не заболеть вовсе. Лучшим профилактическим средством предупреждения ИППП является презерватив. Следует одевать и снимать его правильно и пользоваться им при всех видах секса, включая оральный. Если все же незащищенный контакт произошел, существует методы личной профилактики, когда половые пути промывают раствором антисептика. Сделать это необходимо в первые 2-4 часа после контакта, не позже. При некоторых инфекциях для профилактики могут использоваться специальные лекарственные препараты. Их выбор необходимо обсудить с врачом.
Среди возможных последствий инфекционного поражения половых путей у мужчин:
- Распространение заболевания, которое приводит к развитию заболевания или бесплодия у женщины, инфицирование яйцеклеток и эмбриона, выкидыш, аномалии эмбриона и плода;
- Изменение половых клеток, клеток Сертоли, клеток Лейдига, что приводит к мужскому бесплодию (стерильность);
- Лейкоцитарная инфильтрация половых путей — это опосредованная Т-клетками реакция на сперматозоиды и аутоиммунное бесплодие;
- Снижение образования тестостерона и как следствие — кахексия, мужское бесплодие;
- Встраивание вирусного генома в геном половой клетки с возможным риском передачи последующим поколениям.
Роль инфекций в нарушении оплодотворяющей способности сперматозоидов неоднозначна. Несмотря на множество работ о наличии возбудителей в половых путях, существуют противоречивые выводы относительно их роли, которые они играют в возникновении бесплодия. Прежде всего, это объясняется тем, что данные инфекции часто выявляются как у фертильных, так и у бесплодных пар.
- Mycoplasma genitalium – данный вид микоплазм является 100% патогенным возбудителем. Это ведущий возбудитель негонорейный уретритов (10-30% случаев) у мужчин. M.genitalium чаще вызывает острый уретрит у мужчин, но встречаются и малосимптомные рецидивирующие или бессимптомные формы. Есть данные о взаимосвязи инфицирования M.genitalium с бесплодием и течением беременности. Показаниями к лечению M.genitalium являются: подтвержденная инфекция, вызванная данным возбудителем любой локализации, выявление M.genitalium у полового партнера, клинические симптомы воспалительных заболеваний нижних отделов мочеполового тракта при отсутствие возможности диагностического обследования на наличие M.genitalium.
- Ureaplasma urealiticum и Mycoplasma hominis – условно-патогенные микроорганизмы, встречаются у 10-50% практически здоровых лиц репродуктивного возраста. При определенных условиях они могут вызывать инфекционно-воспалительные процессы мочеполовых органов, нередко в ассоциации с другими возбудителями. Уреаплазмы могут уменьшить подвижность сперматозоидов, прикрепляясь непосредственно к ним. Это было доказано при обнаружении большого количества уреаплазм. Показания к лечению (при отсутствии других значимых возбудителей) U.urealiticum и M.hominis: клинические или лабораторные признаки воспаления любого органа мочеполовой системы, выявление M.hominis или U.urealyticum в количестве > 10 4 КОЕ/мл, предстоящие оперативные или инвазивные лечебно-диагностические манипуляции в области мочеполовых органов, осложненное течение настоящей беременности с риском инфицирования плода, отягощенный акушерско-гинекологический анамнез.
- Трихомонады колонизируются в половых путях мужчин, проявляясь различной симптоматикой вплоть до гематосперимии и эпидидимита. Доказано, что присутствие трихомонад может быть связано с мужским бесплодием, а его наличие в сперме вызывает нарушение подвижности и жизнеспособности сперматозоидов. Механизм влияния данной инфекции на фертильность обусловлен созданием благоприятных условий для проявления других инфекционных агентов в половых путях, а также возможным уменьшением содержанием фруктозы в сперме.
- Установлено существенное ингибирующее влияние Candida albicans в образцах спермы с исходной концентрацией микроорганизмов 2х107/мл in vitro. Есть предположение, что микотический вагинит негативно влияет на подвижность сперматозоидов и усиливает их агглютинацию.
- Роль вирусов во многом неизвестна. Вирусную ДНК обнаруживают методом полимеразной цепной реакции (ПЦР) в эякуляте бесплодных мужчин в 56% случаев (вирус простого герпеса – в 49% случаев, вирус Эпштейна – Барр – у 17% пациентов, цитомегаловирус – в 7% случаев).
- Только присутствие вируса простого герпеса (ВПГ) связано с уменьшением количества сперматозоидов и снижением их подвижности. ВПГ 1 и 2 типа находят в яичках, простате, сперме и это может привести к бесплодию, азооспермии, олигозооспермии. По некоторым данным, лечение ацикловиром обоих партнеров с положительными анализами на ДНК ВПГ приводит к беременности.
- Цитомегаловирус (ЦМВ) находят в простате, семенных пузырьках, сперме и он может вызвать гематоспермию, уменьшение количества CD4-клеток. Обсуждалась роль ЦМВ как возможного этиологического фактора гематоспермии. В исследованиях его определение связывали с уменьшением концентрации и подвижности сперматозоидов. В исследованиях его определение связывали с уменьшением концентрации и подвижности сперматозоидов.
- Если в сперме присутствовал вирус папилломы человеческий (ВПЧ), то частота встречаемости астенозооспермии была значительно выше.
- Вирус эпидемического паротита находят в яичках, паротит приводить к орхиту, атрофии яичек, стерильности, уменьшению секреции андрогенов, возможно к раку яичка.
- Золотистый стафилококк, кишечная палочка, гемолитический стрептококк группы В, обладают высокой спермицидной активностью, когда как у микрококков, энтерококков, белого стафилококка, дифтероидов и негемолитического стрептококка эта активность отмечалась при концентрации более 10 5 КОЕ/мл. Когда эякулят содержит большое количество не только бактерий, но и лейкоцитов, сперматозоиды имеют низкую подвижность и агглютинацию. Некоторые микроорганизмы могут уменьшить подвижность сперматозоидов, прикрепляясь непосредственно к ним. Это было доказано при обнаружении большого количества Escherichia coli.
Материал подготовлен врачом урологом-андрологом, физиотерапевтом, дерматовенерологом Акимовым Олегом Викторовичем.
Ключевые слова: инфекции, передаваемые половым путем, осложнения, рациональная терапия, урогенитальный хламидиоз, уреаплазмоз, репродуктивное здоровье, рациональная фармакотерапия.
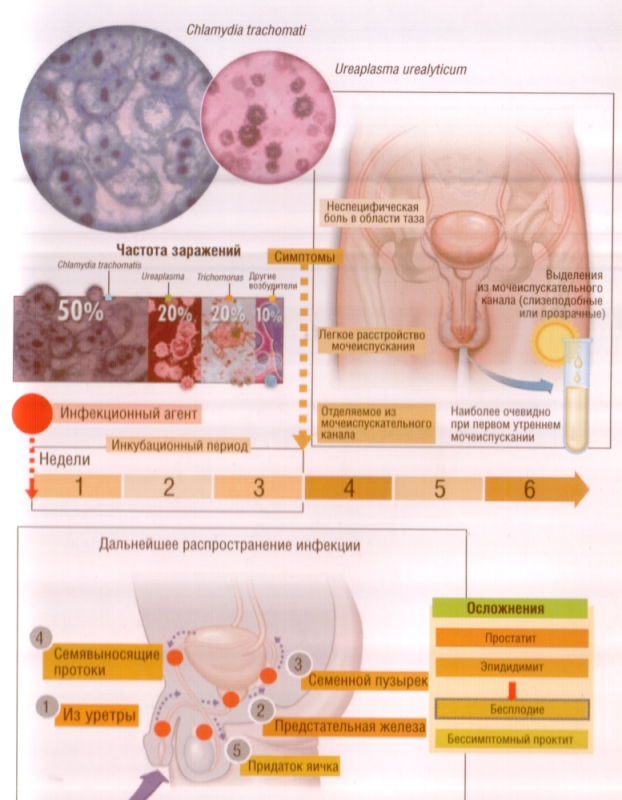
Уже первые клинико-эпидемиологические исследования позволили констатировать, что частота встречаемости урогенитального хламидиоза и уреаплазмоза крайне высока. Так, например, Ch. trachomatis была обнаружена у 51–57% пациентов с негонорейными уретритами (НГУ) в США, 40–58% в Англии, 56,3% во Франции и 58,3% в СССР. U. urealyticum, как причина воспаления уретры негонококковой природы, в разных странах была выделена у 10–40% больных [9]. Более того, уже тогда было отмечено преобладание этих возбудителей в структуре других ИППП. По разным оценкам, соотношение гонореи и НГУ в разных регионах составляло 1:2, 1:3 [6].
Следует отметить, что подобная тенденция сохранилась и в настоящее время. В частности, по данным нашей кафедры, частота встречаемости урогенитального хламидиоза и уреаплазмоза составляет примерно 70%, а на долю гонореи и трихомониаза приходится менее 30% случаев. Если при этом учесть, что только по официальной статистике, например, в России регистрируется более 500 000 больных с хламидийной и уреаплазменной инфекцией, то следует признать, что эпидемиологическая обстановка по этим возбудителям группы ИППП крайне неблагоприятна [2, 4].
Проведенные за последние 20–30 лет исследования позволили оценить значительную роль ИППП и, в первую очередь, Ch. trachomatis и U. urealyticum как причины развития вторичного бесплодия, формирующегося в результате воспалительных процессов в органах репродуктивной системы. Спектр осложнений вышеперечисленных инфекций достаточно широк. Однако с позиции репродуктивного здоровья наиболее значимыми представляются эпидидимит и простатит у мужчин, а у женщин — сальпингит, сальпингоофорит и пельвиоперитонит. Вместе с тем у женщин хроническое течение хламидиоза и уреаплазмоза может привести к развитию внематочной беременности, нарушению менструального цикла или послужить причиной перинатального инфицирования плода [1, 5, 7]. Необходимо также отметить еще один аспект, связанный с поражением хламидиями и уреаплазмами половых придатков, это снижение потенции и либидо, что в свою очередь также негативно отражается на репродуктивной функции человека.
По данным разных авторов, осложнения в результате инфицирования Ch. trachomatis и U. urealyticum, как у мужчин, так и у женщин, могут наблюдаться в 30–50% случаев [5, 7].
Такая высокая частота развития воспалительных процессов репродуктивных органов во многом объясняется особенностями клиники НГУ, в частности частой бессимптомностью течения инфекций. Это, в свою очередь, обуславливает длительное существование резервуара возбудителей и способствует их диссеминации с восходящим характером патологических изменений.
Однако, несмотря на заявленный сегодня приоритет профилактического начала в борьбе с ИППП, одним из актуальных аспектов проблемы по-прежнему остается их терапия. При этом следует подчеркнуть, что достаточно часто мы априори имеем дело не столько с уретритом хламидийной и/или уреаплазменной природы, сколько с их осложнениями. Поэтому лечение таких больных должно предусматривать не только этиотропные средства, но и препараты патогенетической направленности. Вместе с тем надо отметить, что независимо от остроты, длительности заболевания и наличия осложнений именно антибиотики являются базисной терапией урогенитального хламидиоза и уреаплазмоза и ассоциированных с ними синдромов, так как устраняют триггерный фактор воспалительного процесса.
В связи с вышесказанным, с одной стороны, необходим постоянный поиск и создание новых антибактериальных препаратов, с другой — соблюдение при их назначении принципов рациональной фармакотерапии [14, 16].
Наиболее важные положения современной антибактериальной фармакотерапии можно сформулировать следующим образом:
Одним из наиболее перспективных направлений терапии урогенитального хламидиоза и уреаплазмоза представляется применение современных макролидов и фторхинолонов, в частности джозамицина и моксифлоксацина.
Джозамицин относится к группе макролидов и был выделен из Streptomyces narbonensis var. josamyceticus. В отличие от большинства других макролидов, он содержит 16-членное лактонное кольцо и длинную боковую цепь, в то время как эритромицин, кларитромицин и рокситромицин имеют 14-членное, а азитромицин — 15-членное лактонное кольцо. Различия химической структуры имеют важное значение, так как к джозамицину не развивается устойчивость, связанная с эффлюксом. Таким образом, джозамицин по сути дела следует рассматривать отдельно от других представителей этого класса антибиотиков [19].
Джозамицин хорошо проникает в клетки и проявляет очень высокую активность в отношении внутриклеточных патогенов, таких как Мycoplasma hominis, M. pneumoniae, U. urealyticum, Ch. psittaci, Ch. trachomatis и другие.
В клинических исследованиях активность джозамицина изучалась более чем у 35 000 больных, в том числе и при урогенитальном хламидиозе и уреаплазмозе. При этом было показано, что его эффективность, при стандартной схеме назначения, составила в целом около 97%. Такой высокий этиотропный эффект препарата при урогенитальных инфекциях объясняется его высокой активностью в отношении внутриклеточных патогенов, особенно U. urealyticum и М. hominis. По данным недавно проведенного исследования, 96,7% штаммов U. urealyticum были чувствительны к джозамицину. При смешанных инфекциях, вызванных U. urealyticum и М. hominis, джозамицин проявлял активность в отношении 71,4% штаммов этих возбудителей и превосходил другие макролиды (рокситромицин, азитромицин), тетрациклины (доксициклин, миноциклин) и некоторые фторхинолоны (спарфлоксацин, офлоксацин). Клиническая эффективность джозамицина при негонококковом уретрите, цистите и эпидидимите составила 90–100%. В отличие от других макролидов, в последние годы не было отмечено роста устойчивости к джозамицину, поэтому его можно применять в качестве препарата первого ряда при микоплазменных инфекциях урогенитального тракта [23]. Благоприятный эффект джозамицина был продемонстрирован также при инфекциях, вызванных несколькими возбудителями и у мужчин с бесплодием [11].
Немаловажным преимуществом джозамицина является также возможность его применения у беременных. Тем не менее, назначать препарат при беременности, особенно в первом триместре, следует осторожно. Имеющийся опыт применения джозамицина (500 мг три раза в сутки в течение 10 дней) для лечения урогенитального хламидиоза у женщин со сроком беременности от 19 до 34 недель свидетельствует, что через три недели после завершения терапии излечение было отмечено в 100% случаев [3].
Макролиды в целом характеризуются хорошей переносимостью. В клинических исследованиях нежелательные явления были зарегистрированы всего у 4,9% из 27 090 больных, получавших джозамицин [22]. Чаще всего встречаются желудочно-кишечные нарушения (тошнота, рвота, отсутствие аппетита, чувство переполнения желудка, тенезмы, боли в желудке), значительно реже — аллергические реакции. Головокружение и головная боль отмечались только в отдельных случаях.
Хинолоны (фторхинолоны) используются в клинической практике более 40 лет, однако интерес к этой группе возник после появления первого истинного фторхинолона — норфлоксацина. Его высокая антибактериальная активность дала основание для разработки новых препаратов этой группы. Сегодня в медицине достаточно широко используются около 15 антибиотиков производных 6-фторхинолонов.
Однако клиническое значение фторхинолонов не ограничивается исключительно широким спектром их антибактериальной активности. Основным достоинством препаратов этой группы является высокая бактерицидная эффективность по отношению к инфекциям, устойчивым к другим классам антибиотиков, включая полирезистентные штаммы. Это обусловлено механизмом их действия, которое заключается в ингибировании ферментов-топоизомераз (ДНК-гиразы) микробной клетки, ответственных за процесс репликации ДНК, что естественно ведет к нарушению жизнедеятельности возбудителя. При этом топоизомеразы клеток человека практически не подвергаются воздействию антибиотика.
Следует отметить и низкую частоту побочных реакций при применении фторхинолонов, большинство из которых связано с диспепсическими расстройствами и не требует прекращения лечения. Однако при заболеваниях центральной нервной системы, у беременных, а также в педиатрии диапазон их применения ограничен, и они назначаются в основном по жизненным показаниям. Необходимо также помнить и о фотосенсибилизирующем эффекте фторхинолонов и связанных с этим мерах предосторожности, особенно весной и летом.
В настоящее время наиболее перспективным препаратом следует признать фторхинолон четвертого поколения — моксифлоксацин.
Моксифлоксацин является монофторхинолоном и по химической структуре несколько отличается от других препаратов своей группы. За счет введения в хинолиновое кольцо метокси-группы (ОСН3) и циклопропильного радикала резко возросла активность соединения в отношении грамположительных бактерий и, что наиболее важно для дерматовенерологов, достигнута максимальная бактерицидная активность в отношении атипичных внутриклеточных микроорганизмов (хламидии, уреаплазмы). При этом препарат сохранил традиционную для всех фторхинолонов высокую активность и в отношении грамотрицательных бактерий. Механизм действия антибиотика заключается в ингибировании ферментов, ответственных за биосинтез ДНК клетки, — топоизомеразы-2 (ДНК-гираза) и топоизомеразы-4. Благодаря этому механизму бактерицидный эффект моксифлоксацина проявляется на уровне минимальных подавляющих концентраций.
Биодоступность препарата при пероральном приеме составляет не менее 90%. После однократного применения максимальная концентрация в сыворотке крови достигается в среднем через 2–3 часа, однако всасывание моксифлоксацина снижается при одновременном приеме с антацидными препаратами, что следует учитывать при его назначении. Моксифлоксацин на 40% связывается с белками плазмы (в основном альбумином) и быстро распределяется по тканям, создавая высокую бактерицидную концентрацию антибиотика практически во всех системах организма, поддерживая ее в течение суток. Такая продолжительность действия обусловлена длительным периодом полувыведения препарата (12–14 часов). Благодаря этому кратность приема составляет один раз в сутки, что особенно удобно в амбулаторной практике. Следует отметить хорошую переносимость препарата. По данным литературы, наблюдение более 5000 пациентов, принимавших моксифлоксацин, показало, что лишь у 3,8% развились побочные эффекты, потребовавшие отмены антибиотика [18].
Обобщенные данные зарубежных и отечественных исследователей, а также собственный опыт говорят об очень высокой клинико-этиологической эффективности моксифлоксацина при лечении негоноккоковых уретритов.
Так, в одном из первых контролируемых международных исследований (43 центра из 14 стран) была изучена эффективность 14-дневного курса лечения у 232 женщин, страдающих воспалительными заболеваниями органов малого таза (ВЗОМТ) хламидийной природы. Клинический эффект монотерапии моксифлоксацина отмечался у 224 больных (96,6%), бактериологический к концу лечения составил 95,5% [21].
В другом многоцентровом проспективном рандомизированном исследовании, при терапии моксифлоксацином 275 пациентов с урогенитальным хламидиозом по схеме 400 мг один раз в сутки в течение 14 дней, клиническая эффективность была отмечена в 95,9% случаев при этиологическом излечении у 87,5% больных при первом контрольном обследовании через 5 дней после окончания лечения [20].
В Центре простатологии Санкт-Петербургской медицинской академии терапия моксифлоксацином была проведена 34 мужчинам с уретритом и уретропростатитом, у 19 из которых была диагностирована хламидийная, у 10 уреаплазменная и у 5 смешанная хламидийно-уреаплазменная инфекции. После проведенного 10-дневного курса лечения и контрольного обследования через две недели и два месяца после его окончания клинико-бактериологическое излечение наблюдалось в 94,73% при хламидийной и в 86% при уреплазменной инфекциях [11].
По вопросам литературы обращайтесь в редакцию.
