– На старение человека, как и на его здоровье, влияют 5 основных факторов: образ жизни, профессия, экология, болезни и генетика. При этом вклад генетического фона составляет 25-30% (не учитывая случая тяжелых генетических отклонений), а за оставшиеся эффекты отвечают так называемые эпигенетические факторы. В целом, эпигенетика является сегодня наиболее активно развивающимся направлением биологии.
Как известно, из всех когда-либо живших на Земле существ остался всего 1%, остальные 99% состарились и вымерли. Любой биологический вид стареет так же, как организм, только процесс растянут на тысячи лет, и человечество в этом плане не является исключением. По сравнению с 1960 г. количество лиц пожилого возраста в 2000 г. увеличилось примерно в 3 раза, а по прогнозам к 2020 г. этот показатель еще удвоится. Данная проблема актуальна для всех континентов, включая Африку, но наибольшую остроту она приобрела в странах Азии.
По современным научным данным, видовой предел жизни человека составляет 110-120 лет. Однако сегодня средняя продолжительность жизни колеблется в пределах 75-80 лет, что является результатом преждевременного старения. В странах с высоким уровнем культуры и экономики и развитых в социальном плане, например в Скандинавии, средняя продолжительность жизни достигла 85-87 лет. В исследовании, проведенном нами в Санкт-Петербурге, были получены интересные результаты: в микрорайоне, где традиционно проживает интеллигенция, средняя продолжительность жизни женщин и мужчин составила 82 и 74 года соответственно. Очевидно, это связано прежде всего с отсутствием в данном микрорайоне наркоманов, алкоголиков и других лиц, которые ведут асоциальный образ жизни; кроме того, там практически не было людей с ожирением. Таким образом, у каждого из нас есть в запасе биологический резерв жизни, составляющий 35-40 лет, но реализация этого резерва нарушается из-за воздействия на организм различных неблагоприятных факторов, изменяющих экспрессию и структуру генов, что сопровождается нарушением синтеза белка и снижением функций организма.
Данные современных исследований позволяют цсделать вывод, что ведущую роль в механизмах клеточных взаимодействий играют пептиды, которые координируют процессы биосинтеза путем воздействия на экспрессию генов. Многообразие пептидов и их биологических эффектов, обеспечивающих стабильность функционирования организма, позволяет говорить о пептидергической регуляции как ведущем звене гомеостаза и жизнеобеспечения организма. В основе пептидергической регуляции лежит общий тип получения и переноса информации на субклеточном, клеточном и тканевом уровнях. Именно наличие универсального химического языка объединяет три системы, управляющие жизнедеятельностью организма (нервную, эндокринную и иммунную), в единый механизм регуляции функций.
Пептидергическая регуляция гомеостаза обеспечивает постепенные переходы спектров биологической активности отдельных пептидов, способных адекватно реагировать на разнообразные вмешательства в жизнедеятельность организма. При этом представляется вероятным инициирование сложных цепных реакций всего континуума регуляторных пептидов первичным изменением уровня одного из них.
Характерной особенностью пептидергической регуляции гомеостаза является процессинг полипептидов, который позволяет путем активации пептидаз образовывать в нужном месте и в нужное время необходимое количество коротких пептидных фрагментов, обладающих более высокой биологической активностью, чем исходные соединения.
В 1970-х гг. мы изучали механизм иммунодепрессии в эксперименте и клинике и установили, что по мере старения происходит инволюция центрального органа иммунной системы – тимуса и нейроэндокринной системы эпифиза. Также было выявлено достоверное снижение синтеза белка в клетках различных тканей организма, включая предстательную железу и семенники.
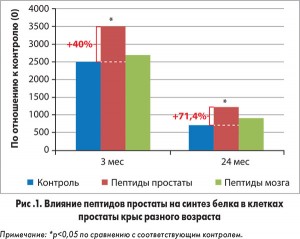
В специальных экспериментах было обнаружено, что короткие пептиды, выделенные из различных органов и тканей, а также их синтезированные аналоги (ди-, три-, тетрапептиды) обладают выраженной тканеспецифической активностью как в культуре клеток, так и в экспериментальных моделях у молодых и старых животных. Воздействие пептидов приводило к тканеспецифической стимуляции синтеза белка в клетках тех органов, из которых эти пептиды были выделены, и эффект усиления синтеза белка при введении пептидов выявлен как у молодых, так и у старых животных. Введение пептидов предстательной железы (ПЖ), например, повышало синтез белка в этом органе у 3- и 24-месячных крыс на 40 и 71,4% соответственно (рис. 1).
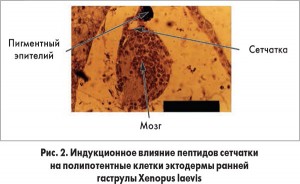
Важнейшим экспериментальным фактом явилось обнаружение способности пептидов индуцировать дифференцировку полипотентных клеток. Так, добавление пептидов сетчатки к полипотентным клеткам эктодермы ранней гаструлы лягушки Xenopus laevis привело к возникновению клеток сетчатки и пигментного эпителия, а добавление пептидов ПЖ – к возникновению ткани этого органа (рис. 2). Т.е. пептиды простаты стимулируют дифференцировку собственных клеток (как известно, все органы живых организмов содержат примерно 30% стволовых клеток). Другими важными эффектами пептидов в экспериментах на животных были увеличение лимита Хейфлика (детерминированное количество делений клеток) более чем на 40-67%, повышение синтеза белка на 42,9%, уменьшение частоты развития опухолей в 3,1 раза, а также увеличение средней продолжительности жизни на 20-40% и максимальной продолжительности жизни – на 42,3%.
Результаты этих исследований послужили основой для разработки методики получения из тканей животных особых веществ – цитомединов (от греч. cytos – клетка и лат mediator – посредник). Цитомедины представляют собой комплексы щелочных полипептидов с относительно небольшой молекулярной массой (обычно не более 10 кД). Один из лекарственных препаратов цитомединов – Витапрост – давно и успешно применяется для лечения заболеваний ПЖ. Основными преимуществами цитомединов являются их природное происхождение, высокая специфичность, абсолютная безвредность и эффективность при применении в микродозах.
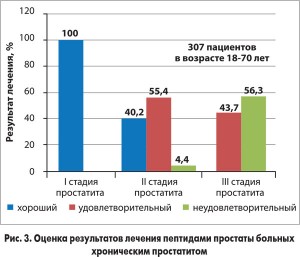
Высокая эффективность и безопасность пептидов ПЖ доказаны клинически. Так, при оценке результатов лечения препаратом Витапрост пациентов (n=307; возраст 18-70 лет) с хроническим простатитом (ХП) хороший эффект при I стадии заболевания был получен в 100% случаев. При ХП II стадии такой же эффект наблюдался у 40,2% пациентов, удовлетворительный – у 55,4%. У больных с III стадией ХП удовлетворительного результата удалось добиться у 43,7%. В динамике лечения болевые ощущения исчезли или значительно уменьшились у 64 и 32,7% пациентов соответственно (рис. 3) (Ткачук В. Н. и соавт., 1991).
За 30-летний период исследований были получены убедительные доказательства эффективности пептидов ПЖ не только при остром и хроническом простатите, но и при острых и хронических пиелонефрите, цистите и панкреатите, травматическом шоке, гравитационных перегрузках и баротравме (в т. ч. у космонавтов и подводников), гиперактивном мочевом пузыре, доброкачественной гиперплазии ПЖ, расстройствах акта мочеиспускания, интерорецептивных формах сексуальной дисфункции, а также при миоме матки, что объясняется развитием ПЖ и матки из одного эмбрионального зачатка.
В настоящее время одобренными показаниями к назначению Витапроста являются абактериальный и бактериальный простатит, доброкачественная гиперплазия ПЖ и различные послеоперационные состояния. В ближайшем будущем ожидается регистрация новой инъекционной формы препарата, оптимальной для реабилитации после трансуретральной резекции и биопсии простаты.
Чтобы как можно дольше оставаться молодым и здоровым, необходимо, как ни банально это звучит, вести здоровый образ жизни. С возрастом у любого человека начинается инволюция жизненно важных систем организма – проще говоря, они постепенно стареют. Первыми, как правило, под прессингующее действие внешних и внутренних факторов попадают иммунная, нейроэндокринная и центральная нервная системы. Поэтому после 35 лет стоит задуматься о профилактике возрастных изменений в своем организме, правильно организовать свой режим и подобрать программу восстановления и омоложения организма на основе пептидов, потому что применение пептидных биорегуляторов – это путь к активному долголетию.
Препарат Витапрост восстанавливает метаболизм белков в клетках предстательной железы.
СТАТТІ ЗА ТЕМОЮ Урологія та андрологія
Гематурия является одним из проявлений мочевого синдрома. По данным различных популяционных скринингов, частота гематурии у детей колеблется от 1-4 до 12-18% случаев [2, 11, 19]. Уровень распространенности среди детей школьного возраста составляет 4,1-5,13% на основании только одного анализа мочи [19, 26] и 0,5-2% при исследовании двух и более анализов мочи [11, 19, 26]. Связь гематурии с расой, социально-экономическим статусом, полом и возрастом пациента не установлена [11, 19].
Известно, что у мужчин ожирение и метаболические осложнения связаны с более низкими уровнями сывороточного тестостерона и дигидротестостерона (ДГТ), а также с повышенным риском развития и смертностью от сердечно-сосудистых заболеваний (ССЗ). Причинно-следственные связи между этими факторами остаются предметом дискуссий. Предлагаем вашему вниманию обзор статьи E. J. Meyer и G. Wittert (университет Аделаиды, Австралия), в которой представлены результаты метаанализа доказательных данных, касающихся связи уровня эндогенного циркулирующего тестостерона со смертностью от всех и конкретных причин.
Доброякісна гіперплазія передміхурової залози (ДГПЗ) та хронічний простатит (ХП) є одними з найбільш розповсюджених захворювань у чоловіків. Частота ДГПЗ широко відома. Так, якщо в 60-річному віці це захворювання спостерігається у 50% випадків, то у 80 років воно вражає понад 80% чоловіків. .
Цистит – одне з найбільш поширених захворювань сечовивідних шляхів, яке зустрічається переважно у молодих жінок. Симптоми циститу можуть суттєво знижувати якість життя та працездатність, а відсутність адекватного лікування сприяє формуванню рецидивуючого перебігу захворювання. Менеджмент циститу передбачає проведення комплексної терапії, спрямованої на усунення інфекційного патогена, полегшення клінічної симптоматики та запобігання розвитку редицивів у майбутньому.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.

Читайте в новом номере
Хронический простатит (ХП) – самая частая причина рецидивирующих инфекций мочевыводящих путей у мужчин. Основной причиной развития ХП является нарушение микроциркуляции в предстательной железе и дренирования ее ацинусов. Антибактериальная терапия, которая помогает во время лечения, не всегда сохраняет эффект в отдаленной перспективе, и в результате остается нерешенной проблема рецидива простатита. К методам лечения, которые приводят к улучшению кровообращения в предстательной железе, относят α-адреноблокаторы, массаж предстательной железы, физиотерапию, препараты тестостерона, цитомедины.
Цитомедины, относящиеся к пептидам, это уникальный класс лекарственных препаратов. Применение простатических цитомединов приводит к восстановлению гемодинамики предстательной железы, ликвидации отека и воспаления, уменьшению клинических проявлений простатита, улучшению качества эякулята. Они повышают тонус детрузора, регулируют детрузор путем влияния на ритм спонтанной сократительной активности. Простатические пептиды не обладают токсическим или мутагенным эффектами. Препарат простатических цитомединов
Витапрост, представленный в различных лекарственных формах, нашел широкое применение при лечении ХП.
Ключевые слова: хронический простатит, синдром хронической тазовой боли, СХТБ, цитомедины, Витапрост, альфа-адреноблокаторы, тестостерон, массаж простаты.
Для цитирования: Карпов Е.И. Современный взгляд на лечение синдрома нижних мочевыводящих путей: цитомедины как класс лекарственных препаратов. РМЖ. 2017;27:1992-1996
Modern view on the treatment of the lower urinary tract syndrome: cytomedines as a class of drugs
Karpov E.I.
Chronic prostatitis is the most common cause of recurrent urinary tract infections in men. The main cause of the development of chronic prostatitis is a violation of microcirculation in the prostate gland and drainage of its acini. Antibiotic therapy is effective during the treatment, but it is sometimes unreliable in the long term. As a result, the problem of recurrence of prostatitis remains unresolved. The methods of treatment that lead to the better blood circulation in the prostate include α-adrenoblockers, prostate massage, physiotherapy, testosterone preparations, cytomedins.
Cytomedines are peptides, a unique class of drugs. The use of prostatic cytomedines leads to the restoration of hemodynamics of the prostate gland, the elimination of edema and inflammation, decrease of the clinical manifestations of prostatitis, and improves the quality of the ejaculate. They increase detrusor tone, regulate detrusor by influencing the rhythm of spontaneous contractile activity. Prostatic peptides do not have toxic or mutagenic effects. The prostatic cytomedines preparation Vitaprost, presented in various dosage forms, is widely used in the treatment of chronic prostatitis.
Key words: chronic prostatitis, chronic pelvic pain syndrome, CPPS, cytomedines, Vitaprost, α-adrenoblockers, testosterone, prostate massage.
For citation: Karpov E.I. Modern view on the treatment of the lower urinary tract syndrome: cytomedines as a class of drugs // RMJ. 2017. № 27. P. 1992–1996.
Статья посвящена возможностям лечения синдрома нижних мочевыводящих путей. Хронический простатит – самая частая причина рецидивирующих инфекций мочевыводящих путей. Применение простатических цитомединов (Витапрост) приводит к восстановлению гемодинамики предстательной железы, ликвидации отека и воспаления, уменьшению клинических проявлений простатита, улучшению качества эякулята.
Только для зарегистрированных пользователей
Нормальная жизнедеятельность любого многоклеточного организма возможна только при слаженной работе всех его органов и тканей, что обеспечивается различными физиологическими механизмами. К ним относятся нейроэндокринная регуляция, а также межклеточные взаимодействия, которые могут быть формообразующими и информационными. Среди информационных межклеточных взаимодействий выделяют контактные и дистанционные. Дистанционная регуляция обеспечивается различными информационными молекулами. К ним относятся и гормоны, небольшие белки, стероиды, ионы, пептиды 1 .
Жизнь любой клетки организма напрямую зависит от поступающих к ней сигналов, которые влияют на характер и интенсивность протекающих в ней биохимических процессов и экспрессию генов внутри неё 2 .
В 1980-х годах при изучении механизмов адаптации из предстательной железы крупного рогатого скота был выделены пептиды, которые оказывали влияние на метаболизм и функцию простаты. Эти вещества получили общее название пептидные биорегуляторы или цитомедины (от лат. citos – клетка и media – посредник) 3 .
В исследованиях пептидных биорегуляторов продемонстрирована их способность усиливать сократительную активность гладкомышечных клеток мочевого пузыря и других гладкомышечных органов, а также сосудов 5, 6, 7 , нормализовать гемостаз за счёт активации фибринолиза и влияния на тромбоциты 8 , стимулировать регенерацию тканей 9 , а также улучшать качество спермы 10 .
Интерес к клиническому применению цитомединов не уменьшается. Вопросы их применения обсуждались на прошедшем 8-10 ноября 2017 года в Москве XVII конгрессе Российского общества урологов 14, 15 .
Ренессанс интереса урологов к проблеме простатита может быть обусловлен пересмотром в 2017 году его классификации. Вместо классификации Национального института здоровья США, которая применялась с 1990-х годов, предлагается использовать фенотипическую классификацию UPOINTS, которая учитывает многообразие клинических проявлений у больных хроническим простатитом 16 .
Эта классификация позволяет индивидуализировать лечение больных простатитом. Используя эту классификацию можно определить место цитомединов в лечении простатита. Это, прежде всего, коррекция органоспецифических симптомов (О), а также нарушений половой функции (S).
Цель. Изучение эффективности препарата, созданного на основе экстракта предстательной железы, Витапрост форте в лечении пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ).
Материал и методы. Проведено лечение 35 больных с ДГПЖ, клинически проявляющейся симптомами нижних мочевых путей. Всем больным назначали Витапрост форте по одному ректальному суппозиторию (100 мг) на ночь в течение 20 дней в виде монотерапии.
Результаты. Полученные данные показали эффективность применения Витапроста форте у больных с ДГПЖ. К окончанию лечения отмечено уменьшение суммы баллов по международной шкале оценки симптомов заболеваний предстательной железы (International Prostate Symptom Score) на 25,8% и улучшение качества жизни на 13,8%. Субъективное улучшение сопровождалось положительной динамикой показателей, характеризующих отток мочи из мочевого пузыря. К окончанию лечения максимальная скорость потока мочи выросла в среднем на 25,4%, а объем остаточной мочи уменьшился на 41,3%. Достоверного изменения размеров предстательной железы и уровня простатического специфического антигена в процессе лечения не отмечено.
Выводы. Проведенное исследование показало, что назначение Витапроста форте способствует уменьшению интенсивности клинических проявлений ДГПЖ. Лечебное действие препарата основано на наличии у него противовоспалительного, иммуномодулирующего и миотропного эффекта. Применение Витапроста форте при лечении больных с ДГПЖ можно считать патогенетически обоснованным, поскольку он оказывает влияние на основные звенья патогенеза заболевания.
- КЛЮЧЕВЫЕ СЛОВА: доброкачественная гиперплазия предстательной железы, пептиды предстательной железы, Витапрост форте
Цель. Изучение эффективности препарата, созданного на основе экстракта предстательной железы, Витапрост форте в лечении пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ).
Материал и методы. Проведено лечение 35 больных с ДГПЖ, клинически проявляющейся симптомами нижних мочевых путей. Всем больным назначали Витапрост форте по одному ректальному суппозиторию (100 мг) на ночь в течение 20 дней в виде монотерапии.
Результаты. Полученные данные показали эффективность применения Витапроста форте у больных с ДГПЖ. К окончанию лечения отмечено уменьшение суммы баллов по международной шкале оценки симптомов заболеваний предстательной железы (International Prostate Symptom Score) на 25,8% и улучшение качества жизни на 13,8%. Субъективное улучшение сопровождалось положительной динамикой показателей, характеризующих отток мочи из мочевого пузыря. К окончанию лечения максимальная скорость потока мочи выросла в среднем на 25,4%, а объем остаточной мочи уменьшился на 41,3%. Достоверного изменения размеров предстательной железы и уровня простатического специфического антигена в процессе лечения не отмечено.
Выводы. Проведенное исследование показало, что назначение Витапроста форте способствует уменьшению интенсивности клинических проявлений ДГПЖ. Лечебное действие препарата основано на наличии у него противовоспалительного, иммуномодулирующего и миотропного эффекта. Применение Витапроста форте при лечении больных с ДГПЖ можно считать патогенетически обоснованным, поскольку он оказывает влияние на основные звенья патогенеза заболевания.
Длительное время основным методом лечения ДГПЖ была операция. Однако в последние десятилетия в связи с активным внедрением в клиническую практику медикаментозной терапии хирургическое лечение применяют все реже и, как правило, на поздних стадиях заболевания. Так, лекарственную терапию получают 85–90% больных ДГПЖ, и только 10–15% подвергаются оперативному вмешательству.
В настоящее время медикаментозная терапия ДГПЖ включает ингибиторы 5-альфа-редуктазы, блокаторы альфа-1-адренергических рецепторов, препараты растительного и биологического происхождения. Общепризнано, что медикаментозная терапия ДГПЖ должна быть патогенетически обоснована. Вопросам изучения патогенеза ДГПЖ посвящены сотни научных исследований, но до сих пор многие принципиальные вопросы развития заболевания остаются неясными.
На сегодняшний день достоверно известно, что гистологическая ДГПЖ связана со старением мужского организма и изменением баланса половых гормонов [2]. Основной причиной усиления пролиферации клеток предстательной железы является увеличение содержания в ней дигидротестостерона. Дигидротестостерон – активный метаболит тестостерона – образуется из него с помощью фермента 5-альфа-редуктазы. Ингибирование 5-альфа-редуктазы приводит не только к прекращению дальнейшего роста простаты, но и к уменьшению ее объема.
Размер предстательной железы играет важную роль в развитии клинических проявлений болезни: выраженность СНМП и инфравезикальной обструкции напрямую связана со степенью гиперплазии. Так, у мужчин с объемом предстательной железы более 50 см3 в пять раз чаще отмечают среднюю и тяжелую степень СНМП и в три раза чаще – выраженную инфравезикальную обструкцию, чем у пациентов с объемом простаты менее 50 см3 [3]. Таким образом, препараты, способные уменьшать размер простаты, в частности ингибиторы 5-альфа-редуктазы, могут снижать не только степень инфравезикальной обструкции, но и выраженность ирритативных симптомов. Для лечения ДГПЖ часто используется и другая группа препаратов – альфа-адреноблокаторы, которые также способствуют редукции ирритативных и обструктивных симптомов за счет расслабления гладких мышц уретры, шейки мочевого пузыря и простаты, не влияя при этом на объем предстательной железы.
Правомерность гипотезы о гормональной природе развития ДГПЖ не подлежит сомнению. Однако некоторые факты указывают на более сложный характер патогенеза этого заболевания, главный из которых – отсутствие прямой корреляции между степенью увеличения простаты и содержанием в ней дигидротестостерона. Это обстоятельство свидетельствует о наличии и других, не только гормональных факторов, влияющих на появление и прогрессирование ДГПЖ. Получены доказательства, что вторым важнейшим патогенетическим фактором является хроническое воспаление [4, 5].
Хроническое воспаление предстательной железы, то есть хронический простатит, традиционно считалось заболеванием молодых мужчин. Однако для пациентов старшего возраста эта проблема также оказалась весьма актуальной. Так, у мужчин в возрасте до 50 лет частота подтвержденного простатита всего только в два раза выше, чем у мужчин старше 50 лет [6]. При этом у мужчин старшей возрастной группы достаточно часто простатит сочетается с ДГПЖ. Результаты обширного исследования показали, что 57,2% больных хроническим простатитом имели ДГПЖ, а 38,7% пациентов с ДГПЖ – хронический простатит [7]. Обнаружена связь между наличием гистологических признаков воспаления в простате и выраженностью клинической симптоматики, оцениваемой по международной шкале оценки симптомов заболеваний предстательной железы (International Prostate Symptom Score – IPSS) [8]. Следовательно, снижение интенсивности воспаления должно приводить к клиническому улучшению у больных ДГПЖ. Установлено, что наличие хронического простатита в молодом возрасте может быть фактором риска развития ДГПЖ позднее. Проведенные исследования показали, что ДГПЖ развивается в 2,4 раза чаще у пациентов с ранее диагностированным хроническим простатитом [9]. Таким образом, наличие хронического простатита можно рассматривать как ранний маркер дальнейшего развития ДГПЖ.
Относительно механизма влияния хронического воспаления на развитие ДГПЖ известно следующее. При воспалении в ткани простаты образуются инфильтраты, состоящие в основном из Т-клеток и макрофагов. В этих воспалительных инфильтратах продуцируются цитокины (интерлейкины 2, 6, 8, 15 и гамма-интерферон), которые усиливают пролиферацию клеток предстательной железы, в частности фибробластов. Граничащие с очагами воспаления клетки простаты по неясным причинам гибнут, их место занимают участки стромальной гиперплазии [10]. Подобное влияние воспаления на пролиферацию ткани простаты связывают с возрастным ослаблением иммунной системы. Наряду с измененным гормональным состоянием оно способствует повреждению популяции супрессорных клеток, приводя к постепенной инфильтрации простаты лимфоцитами и запуская каскад событий, ведущих к развитию ДГПЖ [11].
Цитомедины в лечении ДГПЖ
Исходя из патогенеза заболевания лекарственное средство для медикаментозного лечения ДГПЖ должно обладать противовоспалительным и иммуномодулирующим эффектом. В этой связи патогенетически обосновано использование при лечении больных с ДГПЖ препаратов, в состав которых входит экстракт из предстательной железы. Данные лекарственные средства относятся к группе пептидных биорегуляторов – цитомединам – пептидам с молекулярной массой от 1000 до 10 000 Да [12]. Первые простатические пептиды были получены отечественными учеными в середине 1980-х гг. из предстательной железы быков методом уксуснокислой экстракции и представляли собой комплекс щелочных пептидов с молекулярной массой около 10 000 Да. Затем путем ультрафильтрации этого комплекса была выделена лечебная форма препарата, состоящая из пептидов, молекулярная масса которых уже не превышала 5000 Да.
Пептиды предстательной железы обладают множеством значимых биологических эффектов. Они уменьшают время свертывания крови и повышают антиагрегационную активность сосудистой стенки [13, 14], улучшают микроциркуляцию крови [14], усиливают фибринолитическую активность крови [15], оказывают иммуномодулирующее и иммуностимулирующее действие [16], усиливают синтез антигистаминовых и антисеротониновых антител [17]. Простатические пептиды способны воздействовать на состояние мочевого пузыря. Доказано, что они увеличивают сократительную активность миоцитов детрузора in vivo и in vitro, способствуют повышению базального тонуса полоски детрузора и амплитуды его фазических сокращений [15, 18]. Кроме того, простатические пептиды оказывают регулирующее действие на детрузор за счет изменения ритма его спонтанной сократительной активности. Возможно, это связано с влиянием пептидов на пейсмекерные гладкомышечные клетки детрузора [18].
Несмотря на свою высокую биологическую активность, пептиды предстательной железы не имеют каких-либо побочных эффектов в отношении структуры и функции различных органов и систем и не обладают мутагенным свойством [19].
Простатические пептиды широко используются при лечении различных урологических заболеваний. Наибольший опыт накоплен при лечении заболеваний предстательной железы – хронического простатита и ДГПЖ. Препараты, созданные на основе простатических экстрактов, способствуют восстановлению гемодинамики в предстательной железе, вследствие чего снижается активность воспалительного процесса, уменьшается отек и восстанавливается функция простаты, что сопровождается клиническим улучшением [20, 21]. Снижению интенсивности симптоматики у больных ДГПЖ сопутствует улучшение оттока мочи из мочевого пузыря [21–24].
Простатические пептиды показали свою эффективность при восстановлении мочеиспускания у больных с рефлекторной задержкой мочи после операций на тазовых органах и у пациентов с гипоактивностью детрузора, что связано с наличием прямого миотропного действия на гладкомышечные клетки и повышением вследствие этого сократительной активности детрузора [25, 26]. Доказана эффективность использования пептидов предстательной железы при лечении больных хроническим пиелонефритом [27].
В настоящее время среди лекарственных средств, созданных на основе экстрактов предстательной железы, наибольшее распространение получили препараты семейства Витапрост (регистрационный номер ЛС-001136 от 26.02.2002). Витапрост выпускается как в форме ректальных суппозиториев (Витапрост, Витапрост форте), так и в пероральной форме (таблетки Витапрост).
Задачей настоящего исследования явилось подтверждение эффективности и переносимости препарата Витапрост форте у больных с СНМП, вызванных ДГПЖ.
Материал и методы
Под наблюдением находились 35 больных с ДГПЖ, клинически проявлявшейся СНМП. Критериями включения в исследование были умеренная и выраженная симптоматика заболевания по шкале IPSS (более 8 баллов) и умеренная или легкая степень инфравезикальной обструкции (Qmax менее 12 мл/c и объем остаточной мочи более 50 мл).
Критериями исключения были:
- другие, не связанные с ДГПЖ, возможные причины расстройства мочеиспускания (камни и опухоли мочевого пузыря, стриктура уретры и др.);
- острые или в активной фазе хронические инфекции нижних мочевых путей и половых органов;
- подозрение на нейрогенный характер нарушений мочеиспускания;
- уровень простатического специфического антигена выше 4,0 нг/мл;
- наличие показаний к оперативному лечению ДГПЖ – острая задержка мочи в анамнезе или наличие на момент осмотра выраженной инфравезикальной обструкции – Qmax менее 4,0 мл/с и объем остаточной мочи более 200 мл;
- операции по поводу ДГПЖ или других заболеваний предстательной железы и нижних мочевых путей в анамнезе.
Средний возраст пациентов составил 64,8 ± 6,4 года. Всем больным назначали Витапрост форте по одному ректальному суппозиторию в сутки в течение 20 дней (20 суппозиториев на курс). Каждый суппозиторий содержал 100 мг экстракта простаты – субстанции Сампрост (в пересчете на водорастворимые пептиды 20 мг). Никаких других лекарственных препаратов для лечения симптомов, связанных с ДГПЖ, пациенты в этот период не получали.
До начала лечения и сразу после его окончания все пациенты прошли комплексное обследование, включавшее в себя оценку выраженности симптоматики с помощью анкеты IPSS, урофлоуметрию, ультразвуковое измерение объема остаточной мочи и объема предстательной железы. Переносимость Витапроста форте оценивали по наличию побочных эффектов лечения.
Результаты и их обсуждение
Результаты проведенного исследования указывают на эффективность применения Витапроста форте у больных с ДГПЖ. В процессе лечения Витапростом форте отмечено достоверное снижение выраженности симптоматики ДГПЖ, что нашло отражение в уменьшении суммы баллов по шкале IPSS. Если до начала лечения этот показатель составил 15,9 ± 1,6 балла, то через 20 дней лечения – 11,8 ± 1,5 (-25,8%) балла (таблица).
Снижение интенсивности клинических проявлений ДГПЖ сопровождалось улучшением качества жизни (Quality of life – QoL). Исходное значение показателя QoL составило 3,6 ± 0,2 балла. После окончания лечения Витапростом форте значение этого показателя снизилось до 3,1 ± 0,2 (-13,8%) балла.
Уменьшение симптоматики ДГПЖ при применении Витапроста форте сопутствовало улучшению оттока мочи из мочевого пузыря. Об этом свидетельствовало существенное повышение скорости потока мочи по результатам урофлоуметрии и снижение количества остаточной мочи в мочевом пузыре. Максимальная объемная скорость потока мочи к окончанию лечения увеличилась с исходных 10,2 ± 1,4 до 12,8 ± 1,4 мл/с (+25,4%). Объем остаточной мочи уменьшился с 63,2 ± 6,7 до 37,6 ± 4,9 мл (-41,3%) к 20-му дню от начала терапии.
Результаты проведенных исследований не показали достоверного изменения размеров предстательной железы в процессе лечения. До начала курса терапии и по его окончании объем простаты составил 45,7 ± 4,1 и 43,9 ± 4,5 см3 соответственно. Кроме того, не было отмечено влияния Витапроста форте на уровень простатического специфического антигена.
Таким образом, применение Витапроста форте сопровождалось достоверным уменьшением симптоматики ДГПЖ и улучшением качества жизни больных, увеличением скорости потока мочи и снижением объема остаточной мочи. На размер предстательной железы и содержание простатического специфического антигена в крови больных Витапрост форте влияния не оказывал.
Переносимость Витапроста форте была удовлетворительной. Ни у одного больного не отмечено негативных явлений, связанных с применением препарата.
Согласно полученным данным, применение препарата Витапрост форте способствует уменьшению интенсивности клинических проявлений и улучшает качество жизни больных с ДГПЖ. На фоне лечения снижается степень инфравезикальной обструкции, о чем свидетельствует повышение скорости потока мочи и снижение количества остаточной мочи. Объяснить улучшение оттока мочи только противовоспалительным эффектом Витапроста форте и связанным с этим уменьшением механического компонента инфравезикальной обструкции нельзя, поскольку объем предстательной железы в процессе лечения не изменился.
Полагаем, что важную роль в лечебном действии Витапроста форте играет обнаруженная у простатических пептидов способность воздействовать непосредственно на гладкомышечные клетки мочевого пузыря, усиливая их сократительную активность [15, 18]. Этот эффект имеет особое значение, поскольку у больных ДГПЖ часто наблюдается нарушение сократимоcти детрузора [28]. Необходимо отметить, что применение Витапроста форте сопровождалось снижением интенсивности ирритативной симптоматики и ни в одном случае, несмотря на влияние на сократительную активность детрузора, не привело к увеличению частоты мочеиспусканий или императивных позывов. Вероятным объяснением этого служит тот факт, что простатические пептиды могут регулировать ритм спонтанной активности детрузора [18].
Полученные в ходе настоящего исследования результаты подтверждают целесообразность использования Витапроста форте для лечения ДГПЖ у больных с умеренно выраженной инфравезикальной обструкцией, а его применение в виде монотерапии патогенетически обосновано.
