| Классы МПК: | A61B8/06 измерение тока крови A61B8/08 обнаружение органических изменений в организме, например различных новообразований, кист, опухолей |
|||||||||||||
| Автор(ы): | Резайкин Александр Васильевич (RU) , Зубарев Андрей Русланович (RU) | |||||||||||||
| Патентообладатель(и): | Резайкин Александр Васильевич (RU) | |||||||||||||
| Приоритеты: |
| Таблица | ||
| Показатели уровня ПСА и ультразвуковые параметры у обследованных мужчин | ||
| Уровень ПСА (общий) нг/мл | Доплеровский спектр венозного оттока | Серошкальные признаки злокачественного новообразования (ТРУЗИ) |
| 4,2-4,6 (212 чел.) | Переходный (212 чел.) | Не выявлены |
| 4,8-6,5 (108 чел.) | Атипичный (108 чел.) | У 58 пациентов — в периферической зоне и на границе гипоэхогенные образования без четких границ. |
| 6,8-7,5 (30 чел.) | Выраженно-атипичный (30 чел.) | У всех 30 пациентов — гипоэхогенные образования в периферической зоне и на границе зон. |
Пациенты с уровнем ПСА от 4,8 нг/мл до 6,5 нг/мл и атипичным спектром кровотока (108 чел.), а также 58 пациентов с серошкальными признаками возможного неопластического процесса были направлены на биопсию простаты, у 14 (24,1%) из них при первом же исследовании были выявлены атипичные клетки во взятом материале, у 44 — их не было.
Пациенты (30 чел.) с уровнем ПСА от 6,8 нг/мл до 7,5 нг/мл с выраженно-атипичным спектром кровотока также были направлены на биопсию предстательной железы. У данной группы больных при первом же исследовании были выявлены атипичные клетки во взятом материале.
По данным отечественных онкологов ПСА не является специфическим маркером рака предстательной железы, что обусловливает одинаковые показатели маркера у пациентов с доброкачественной гиперплазией простаты и начальными формами рака. Частота ложно-положительных значений при доброкачественной гиперплазии простаты при пороговом уровне 4 нг/мл колеблется от 20 до 55%, в связи с этим определяют плотность ПСА, представляющую собой отношение концентрации общего ПСА к объему предстательной железы, определяемому с помощью ТРУЗИ. Учитывая более высокие концентрации ПСА у больных раком по сравнению с доброкачественной гиперплазией простаты при одинаковом объеме железы плотность ПСА теоретически может быть использован для определения вероятности наличия аденокарциномы в нормальной при пальцевом исследовании железе при значениях ПСА 4-10 нг/мл и соответственно, для принятия решения о показаниях к биопсии. Некоторые авторы полагают, что при нормальных данных пальцевого исследования и плотности ПСА
Этиология опухолей
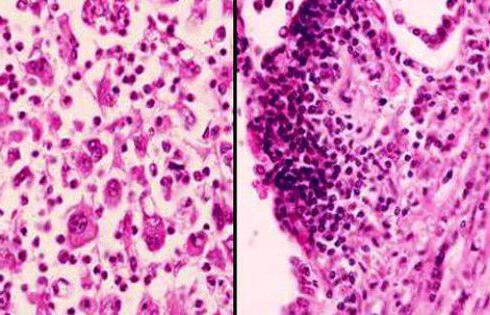
Деление
Количество делений
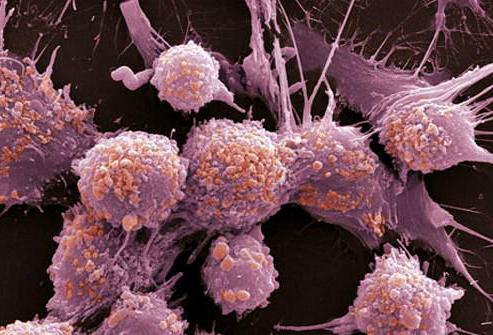
Бессмертие
Неоангиогенез
Уникальное свойство раковых опухолей состоит в их способности к очень активному ангиогенезу, то есть, к образованию новых кровеносных сосудов. В здоровом организме ангиогенез происходит в незначительном объеме, например, при образовании рубцов либо при заживлении очагов воспаления. Неопластические процессы многократно увеличивают эту функцию организма, потому что если в разросшемся теле опухолей не будут появляться кровеносные сосуды, то не все раковые клетки будут получать питательные вещества, которые им тоже необходимы. Кроме того, кровеносные сосуды они используют для продвижения дальше по организму (для образования метастаз).
Генетическая нестабильность
Причины
Клетка начинает вести себя неправильно из-за изменений в ее ДНК. Почему они происходят, пока точного ответа нет, есть лишь теории, согласно которым неопластические процессы могут начаться с той или иной степенью вероятности.
1. Наследственная генетическая предрасположенность. Установлено 200 видов злокачественных новообразований, вызываемых наследственной аномалией следующих генов:
-отвечающих за восстановление поврежденных участков ДНК;
-регулирующих взаимодействие между клетками;
-отвечающих за подавление развития опухолей.
2. Химические вещества (канцерогены). По статистике ВОЗ они повинны в 75% случаев возникновения рака. Общепризнанными канцерогенами являются: табачный дым, нитрозамины, эпоксиды, ароматические углеводороды – всего более 800 элементов и их соединений.
3. Физические агенты. К ним относятся радиация, излучение, воздействие высокими температурами, травмирование.
4. Эндогенные канцерогены. Это вещества, образуемые в организме при гормональных нарушениях, сбоях в обменных процессах.
5. Онковирусы. Считается, что существует особый вид вирусов, способных запустить неопластические процессы. К ним относятся вирус герпеса, папилломовирус, ретровирус и другие.
Плохая экология, некачественная еда, высокие психологические нагрузки ведут к тому, что клетки-мутанты в организмах людей появляются постоянно, но иммунная защита их обнаруживает и вовремя уничтожает. Если иммунитет ослаблен, атипичные клетки остаются жить и постепенно становятся злокачественными.
Виды опухолей
Часто спрашивают, неопластический процесс, это рак или нет? Однозначного ответа на него нет. Все опухоли делятся на две категории:
Доброкачественными считаются такие, в которых можно дифференцировать клетки, и которые не дают метастаз.
В злокачественных опухолях клетки часто полностью утрачивают сходство с тканями, из которых они развились. Эти образования обладают быстрым ростом, способностью к инфильтрации (проникновению в соседние ткани и органы), метастазированию и оказывают патологическое влияние на весь организм.
Доброкачественные опухоли без надлежащего лечения очень часто перерастают в злокачественные. Различают такие их виды:
-эпителиальные (не имеют специфической локализации);
-эпителиальные опухоли эндокринных желез и покровов;
-мезенхимальные (мягких тканей);
-органов нервной системы;
Стадии развития
Отвечая на вопрос, неопластический процесс, это рак или нет, следует сказать, что в патогенезе развития опухолей наблюдается такое состояние, как предрак. Существует два его типа:
-облигатный (практически всегда переходящий в рак);
-факультативный (переходящий в рак не всегда). Факультативным предраком можно назвать бронхит курильщиков или хронический гастрит.
Любой неопластический процесс развивается не мгновенно, а постепенно, часто начинаясь с атипичных изменений всего в одной клетке. Этот этап называется инициацией. При этом в клетке появляются онкогены (любые гены, способные превратить клетку в злокачественную). Самый известный онкоген р53, который в нормальном состоянии является антионкогеном, то есть, борется с развитием опухолей, а при мутации сам их и вызывает.
На следующем этапе, называющемся промоцией, такие измененные клетки начинают делиться.
Третий этап называется прединвазивным. При этом опухоль растет, но в соседние органы еще не проникает.
Четвертый этап – инвазивный.
Пятый этап – метастазирование.
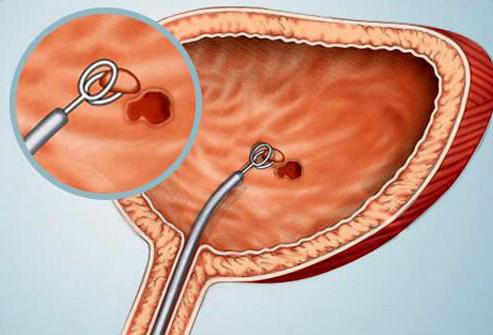
Признаки неопластического процесса
На первых этапах начавшаяся патология себя никак не проявляет. Обнаружить ее очень сложно даже при таких исследованиях, как УЗИ, рентген, различные анализы. В дальнейшем у больных появляются специфические симптомы, характер которых зависит от места локализации первичной опухоли. Так, о ее развитии в коже или в молочной железе сигнализируют новообразования и уплотнения, о развитии в ухе – ухудшение слуха, в позвоночнике – затруднения при движении, в головном мозге – неврологические симптомы, в легких – кашель, в матке – кровяные выделения. Когда раковые клетки начинают проникать в соседние ткани, они разрушают в них кровеносные сосуды. Именно это становится причиной появления крови в выделениях, причем не только из половых органов. Так, кровь в моче наблюдается, когда развивается неопластический процесс почки, мочевого пузыря или мочевыводящих путей, кровь в кале может свидетельствовать о начале рака в кишечнике, кровь из соска – об опухоли в молочной железе. Такой симптом обязательно должен вызвать тревогу и сподвигнуть на немедленное обращение к врачу.
Еще одним ранним симптомом является, так называемый, синдром малых признаков. Его главная особенность состоит в широком разнообразии проявлений. Общими можно назвать жалобы больных на слабость, усталость, возникающие вдруг скачки температуры, необъяснимое раздражение или, наоборот, безразличие ко всему, потерю аппетита, а на этой почве исхудание.
На последующих стадиях появляются симптомы интоксикации, а также изменение цвета кожи на желтушный с бледным оттенком, снижение тургора кожи, раковая кахексия.
При новообразованиях в тканях мозга по причине того, что этот орган ограничен костями черепа, и для развивающейся опухоли пространство сильно ограничено, а также по причинам специфичности функций каждого отдела мозга, симптомы имеют характерные черты, позволяющие дифференцировать локализацию. Так, неопластический процесс в затылочной части проявляется появлением у больного видений, нарушением восприятия цвета. При процессе в височной области видений не наблюдается, но есть слуховые галлюцинации. Опухоль в лобной доли характеризуется психическими расстройствами пациента, нарушением у него речи, а в теменной области нарушением двигательных функций и чувствительности. Симптомы поражения мозжечка – частые рвоты и ужасные головные боли, а поражения ствола мозга – затруднения при глотании, расстройства дыхания, сбои в работе многих внутренних органов.
На последних стадиях все раковые больные испытывают мучительные боли, купировать которые можно только наркотическими препаратами.
Диагностика
Для уточнения диагноза пациенту проводят такие анализы:
-анализы крови, мочи;
-биопсию (это очень важный анализ, с помощью которого не только определяют наличие раковой опухоли, но и стадию ее развития).
При подозрении на рак кишечника выполняют:
— анализ кала на присутствие в нем скрытой крови;
Неопластический процесс головного мозга лучше всего обнаруживается с помощью МРТ. Если больному этот вид диагностики противопоказан, ему выполняют КТ. Также при опухолях мозга проводят:
Лечение
Если недуг поразил детей, их лечение заключается в основном в химиотерапии и в лучевой терапии, хирургическое вмешательство проводят редко. Для лечения взрослых применяют все доступные методы, целесообразные при конкретной стадии неопластического процесса и в зависимости от места его локализации:
-химиотерапию (системное лечение, оказывающее воздействие на весь организм);
-лучевую и радиотерапию (оказывает воздействие непосредственно на опухоль, может затрагивать соседние здоровые участки);
-гормонотерапию (призвана продуцировать гормоны, препятствующие росту опухоли или ее уничтожающие, например, неопластический процесс предстательной железы может быть купирован уменьшением уровня тестостерона);
-иммунотерапию (положительно воздействует на весь организм);
-генную терапию (ученые пытаются заменить мутировавший на нормальный ген р53);
-хирургическую операцию (может проводиться для удаления опухоли либо для уменьшения страданий больного путем снижения разросшейся неоперабельной опухоли на соседние ткани).
Прогноз
Неопластический процесс – это не приговор. У детей в связи с тем, что их молодой организм способен быстро восстанавливаться, прогноз благоприятный в 90 % случаев, если развитие опухоли выявлено на ранних стадиях. Но даже на поздних стадиях выявления при интенсивной терапии дети могут полностью излечиваться.
У взрослых благоприятный прогноз на первой стадии опухоли составляет 80 % и выше. На третьей стадии благоприятный исход лечения наблюдается в 30 %-50 % случаев (в зависимости от локализации образования и особенностей организма каждого человека). На четвертой стадии по статистике от 2 % до 15 % пациентов после терапии живут 5 лет и более. Эти цифры также зависят от локализации опухоли. Наименее благоприятный прогноз при раке предстательной железы и головного мозга.
ПИН (простатическая интраэпителиальная неоплазия) является предраковым состоянием. Это доказанный предшественник рака предстательной железы
Простатическая интраэпителиальная неоплазия имеет много других названий. Она известна как ПИН (PIN), гиперплазия с малигнизацией, атипичная первичная гиперплазия, крупноацинарная атипичная гиперплазия, дуктально-ацинальная дисплазия. Все эти понятия обозначают одно состояние — очаговый рост клеток, который постепенно начинает сопровождаться их перерождением. Заболевание коварно тем, что длительное время не проявляется никакими симптомами.
ПИН разделяется на две формы:
- простатическая интраэпителиальная неоплазия низкой степени (начинающаяся дисплазия);
- простатическая интраэпителиальная неоплазия высокой степени.
При обнаружении ПИН высокой степени, выполняется повторная биопсия простаты через один — три месяца. Она проводится с использованием расширенной методики, при которой ткани для исследования забираются не менее чем из двенадцати точек.

Считается, что ПИН низкой степени опережает развитие рака простаты в среднем на пять лет, а обнаружение ПИН высокой степени с большой долей вероятности означает обнаружение рака при повторной (через 6 месяцев) биопсии.
Общепринятая схема лечения ПИН отсутствует. Терапия либо совсем не назначается, либо используются ингибиторы 5α-редуктазы (Финаст, Проскар, Аводарт, Пенестер). Данные препараты, могут снизить вероятность дальнейшего развития ПИН. Однако при этом они обладают рядом существенных побочных эффектов, таких, как:
- импотенция;
- рост молочных желез;
- снижение либидо;
- уменьшение объёма эякулята.
По данным некоторых исследований, длительное применение финастерида (Проскар, Пенестер, Финаст) увеличивает риск развития опухолей агрессивных, которые очень сложно поддаются терапии.
Возможной альтернативой для пациента с обнаруженной ПИН является Индигал. Клинические исследования подтвердили, что Индигал вызывает обратное развитие ПИН высокой и низкой степени. Его эффективность сравнима с ингибиторами 5α-редуктазы. Но, в отличие от этих препаратов, Индигал совершенно безопасен. Он практически не вызывает побочных эффектов. Его длительный приём не сопровождается повышением риска развития агрессивных опухолей.
Некоторые специалисты не считают ПИН состоянием, связанным с раком.
Предраковое значение ПИН доказывают следующие обстоятельства:
- Простатическая интраэпителиальная неоплазия в предстательной железе, явно поражённой раковой опухолью, встречается гораздо чаще. При этом она обладает большей злокачественностью. Имеет распространённое, многоочаговое расположение. В предстательной железе с аденомой и другими доброкачественными гиперплазиями ПИН встречается значительно реже.
- Простатическая интраэпителиальная неоплазия обнаруживается там же, где и рак. В основном, в периферической зоне, в задней или боковой доле. Достаточно часто наблюдается соседствующее расположение ПИН и явного рака. В центральной, периуретральной зоне ПИН обнаруживается только в пяти процентах случаев. Причём она характеризуется меньшим стремлением к раковой прогрессии.
- Простатическая интраэпителиальная неоплазия постепенно замещается раковыми клетками. Поэтому её объём в простате обычно обратно пропорционален объёму расположенного рядом с ней рака.
- Простатическая интраэпителиальная неоплазия слабо продуцирует ПСА. Это её отличает от рака.

В последние годы наблюдается увеличение роста онкологических болезней. Этот факт подтолкнул развитие различных способов скринингового диагностирования, позволяющих обнаруживать подобные патологии в раннем периоде. С помощью этик методов также можно определять состояния, которые являются предвестниками раковых заболеваний.
При поражении предстательной на помощь приходит в первую очередь, проверка ПСА, исследование с помощью пальпации, ТРУЗИ, биопсия, выполненная, если есть причины для ее взятия.
Самым точным методом является пока лишь единственный, подразумевающий исследование под микроскопом фрагментов тканей простаты, которые были получены в ходе проведения биопсии. Эта статья описывает наиболее встречающиеся результаты обследований и ПИН.
Сущность термина ПИН и что он означает

Множественные международные исследования давно подтвердили: ПИН является одним из предвестников рака предстательной. Почти 85 случаев из ста удаленных опухолей, кроме раковых содержали и ПИН. А вот гистологическое исследование материалов удаленных аденом предстательной показывает ПИН примерно у 40 из ста.
Имеет ли значение степень ПИН и если да, то какое?
В конце девяностых прошлого столетия специалисты выделяли 2 стадии неоплазии предстательной.
Первая сигнализировала о незначительных изменениях эпителия железы. Само по себе это не было еще специфическим предвестником предраковый преобразований в органе, а вызвано вялотекущим воспалением или аденомой тканей.
Вторая стадия относится к запущенному процессу ПИН. Она означает некоторое преобразование клеток эпителия, при котором они больше напоминают очаги опухоли, чем нормальные.
Общепринятая терминология и классификация процессов неопластической природы клеток предстательной современные специалисты считают:
ПИН и ПСА
Среди диагностик, позволяющих определить группу лиц, у которых риск развития раковой патологии высок, есть наиболее верный. Это кровь на маркер, который называется ПСА. Именно он очень рано, хоть и не прямо указывает на вероятность заболевания простатическим раком. Если такой анализ получен подозрительный, назначаются дополнительные диагностические исследования, с помощью который возможно будет выяснить истинную картину патологии.
Среди методов диагностики, помогающих уточнить диагноз, могут быть различные УЗИ (ТРУЗИ), МТР, компьютерное исследование или биопсия. Среди перечисленных методов наиболее достоверно подтверждает или отвергает заболевание такой метод, как биопсия. Именно биопсия точно может определить есть ли в предстательной раковые клетки или нет до фактического появления опухолевых узлов.
Как лечить ПИН
Всем больным, которым был поставлен ПИН, и биопсия подтвердила этот факт, рекомендуется:
Гормональная терапия
Любые атипичные процессы в предстательной очень остро реагируют на изменения фона гормонов в организме. Поэтому терапия должна быть направлена на снижение уровня тестостерона и его влияния на клетки предстательной. Такие угнетающие гормоны эффекты имеют ингибиторы тестостеронредуктазы, некоторые нестероидные антиандрогенные препараты, средства, угнетающие рецепторы релизинг-гормонов.

В последние десятилетия наметилась четкая тенденция роста онкологической заболеваемости. Это вызвало развитие методов скрининговой диагностики, которые позволят не только выявлять заболевания на ранних стадиях развития, но и определить состояния, являющиеся предшественниками злокачественных опухолей. В отношении поражения простаты – это в первую очередь, определение ПСА (простатспецифического антигена), пальцевое исследование, ТРУЗИ и результаты биопсии, выполненной при наличии показаний.
Самым достоверным методом может быть только морфологическое исследование под микроскопом фрагментов простатических тканей, полученных в ходе биопсии. Описанию наиболее тревожных результатов данного исследования и тому, что такое ПИН и рак простаты, посвящена данная статья.
ПИН – это не диагноз, а заключение результатов изучения микропрепаратов тканей простаты. Расшифровка данной аббревиатуры звучит, как простатическая интраэпителиальная неоплазия. Это значит, что эпителиальные и железистые клетки, образующие ацинусы простаты или выстилающие их выводные протоки обладают аномальной структурой, но не похожи на раковые.
Многочисленными исследованиями было установлено, что ПИН относится к предвестникам рака простаты и в более, чем 85% случаев удаленных препаратов, помимо раковой трансформации определяется и простатическая интраэпителиальная неоплазия. В то же время, гистологические исследования препаратов и биоптатов удаленной аденомы простаты определяют ПИН не более, чем в 40% случаев.
Важно помнить! Простатическая интраэпителиальная неоплазия (ПИН) и рак простаты – очень частое сочетание. Но это два отдельных состояния. Их взаимосвязь построена таким образом, что большинство случаев ПИН со временем перерастает в рак. В тоже время, на фоне простатического рака рядом с опухолевой тканью могут быть участки с признаками интраэпителиальной неоплазии простаты!

До 90-х годов специалистами выделялось две степени простатической интраэпителиальной неоплазии. Первая или низкая говорила о том, что эпителий простатических желез изменен незначительно, что не было специфичным признаком предракового состояния, а могло быть вызвано хроническим воспалительным процессом или доброкачественной гиперплазией простатических тканей.
Вторая или высокая степень ПИН обозначала некое переходное состояние эпителиальных клеток, при котором они в большей степени напоминали опухолевые клетки, чем нормальные простатические. Некоторые современные специалисты используют данную классификацию ПИН и сегодня.
Общепринятой терминологией и градацией неопластических процессов простатических клеток (ПИН и рак простаты) на современном этапе онкоурологии считаются:
- Атипическая гиперплазия. Данный вариант заключения исследования биоптатов простаты по своим морфологическим изменениям соответствует ПИН низкой степени. Ее трансформация в аденокарциному (рак) происходит намного реже, чем при ПИН высокой степени (не более 15-20% случаев).
- Собственно ПИН (простатическая интраэпителителиальная неоплазия). Соответствует тому понятию ПИН, которое раньше расценивалось, как ПИН высокой степени (вероятность развития рака более 85%). Это значит, что в результатах анализов после биопсии достаточно просто указывать заключение простатическая интраэпителиальная неоплазия без указания ее степени.
- Клеточная атипия или рак. Не является степенью ПИН, но часто с ним сочетается. В таком случае наличие последнего диагностического и прогностического значения уже не имеет.
Важно помнить! Согласно рекомендациям Всемирной организации здравоохранения, градация ПИН по степеням не целесообразна. Заключение ПИН по результатам гистологического исследования предполагает наличие у больного предракового состояния с высоким риском трансформации в рак!
Самым распространенным методом определения лиц из группы риска по развитию рака простаты является анализ крови на ПСА. Этот онкомаркер рака простаты очень рано, но косвенно может указывать на возможность наличия простатического рака. По его данным назначаются дополнительные исследования, которые позволят установить истинное состояние и структуру простаты.
Это могут быть ТРУЗИ (ультразвуковое исследование простаты с помощью прямокишечного датчика), компьютерная или магнитно-резонансная томография, а также биопсия простаты. Самым достоверным подтверждением заключений ПИН и рак простаты считается последний метод, поскольку позволяет определить раковые клетки до того, как образуется опухолевый узел, который можно визуализировать инструментальными методами.
Показанием для биопсии простаты может стать высокий уровень ПСА (выше возрастных норм), особенно при сочетании с активным приростом в течении короткого времени. Но достоверной связи уровня ПСА с частотой обнаружения ПИН не установлено. Это значит, что простатическая интраэпителиальная неоплазия не вызывает повышения ПСА, как это делает рак или аденома. Поэтому уровень ПСА и ПИН относятся к отдельным критериям, которые используются для диагностики раковых и предраковых заболеваний простаты.
Всем пациентам, у которых по данным биопсии простаты обнаружено ПИН, показано:
- Диспансерное наблюдение в уролога.
- Обязательные осмотры, включающие пальцевое исследование простаты два раза в год.
- Мониторинг ПСА в динамике ежемесячно.
- ТРУЗИ простаты 1-2 раза в год. Количество исследований может увеличиваться при наличии показаний.
- Повторная биопсия простаты не менее 1 раза в год.
- Лучевая терапия. Показана при крайне высоком риске перерождения ПИН в рак на фоне повышения уровня и скорости прироста ПСА.
Гормональная терапия. Все неопластические процессы в простате (ПИН и рак простаты) очень чувствительны к колебанием гормонального фона. Поэтому их лечение должно быть направлено на уменьшение влияния тестостерона на аномальные железистые клетки. Такими антиандрогенными эффектами обладают ингибиторы тестостеронредуктазы (пенестер, простан), нестероидные антиандрогенные средства (ципротерон, флутамид, нилутамид), агонисты рецепторов релизинг-гормонов (лейпрорелин, бусерлин).
Важно помнить! Гормональная терапия простатической интраэпителиальной неоплазии – очень эффективный метод, который применяется и при лечении рака простаты. При наличии показаний он обязательно должен быть использован для предотвращения злокачественного перерождения простатических тканей!
detector



