Русское название
Латинское название вещества Гозерелин
Химическое название
6-[O-(1,1-Диметилэтил)-D-серин]-10-деглицинамидорилизинг фактора лютеинизирующего гормона (свиного) 2-(аминокарбонил)гидразид
Брутто-формула
Фармакологическая группа вещества Гозерелин
Нозологическая классификация (МКБ-10)
Код CAS
Характеристика вещества Гозерелин
Противоопухолевое гормональное средство, синтетический декапептид — аналог гонадотропин рилизинг-гормона ( ГнРГ ) . Гозерелина ацетат — почти белый порошок. Свободно растворим в уксусной кислоте, растворим в воде; 0,1М соляной кислоте; 0,1М растворе натрия хлорида, диметилформамиде, диметилсульфоксиде. Нерастворим в ацетоне, хлороформе, эфире. Молекулярная масса 1269,43 (гозерелин), 1328 (гозерелина ацетат).
Фармакология
При начальном или прерывистом применении стимулирует высвобождение из передней доли гипофиза ЛГ и ФСГ . При постоянном длительном применении гозерелин ингибирует секрецию ЛГ и ФСГ . Значительно понижает содержание в сыворотке крови тестостерона у мужчин и эстрадиола у женщин, в начале лечения возможно временное увеличение их концентраций (обычно в течение первых 7 дней). У мужчин концентрация тестостерона снижается до посткастрационного уровня примерно через 2–4 нед (3,6 мг) или к 21 дню после инъекции (10,8 мг) и продолжает оставаться сниженной при постоянном лечении, проводимом каждые 28 дней. У женщин концентрация эстрадиола в сыворотке снижается примерно к 21 дню после инъекции и при постоянном лечении, проводимом каждые 28 дней, остается сниженной до уровня, который можно сравнить с тем, что наблюдается у женщин в постклимактерическом периоде. У мужчин вызывает регресс опухоли предстательной железы, а у женщин — истончение эндометрия, уменьшение симптоматики и размеров объемных образований (гормонозависимые опухоли грудной железы, эндометриоз, фиброма матки). После прекращения терапии физиологическая секреция гормонов восстанавливается. Гозерелин оказывает более длительное действие, чем эндогенный ГнРГ .
Канцерогенность, мутагенность, влияние на фертильность
В экспериментальных исследованиях показано, что при п/к введении самцам и самкам крыс гозерелина ацетата каждые 4 нед в течение 1 года в дозах, превышавших МРДЧ в 31,5 или 62,4 раза (самцы) и в 21,5 или 42,4 раза (самки) была выявлена повышенная частота доброкачественной аденомы гипофиза. Сходные дозы, вводимые самцам крыс в течение 72 нед и самкам в течение 101 нед , также приводили к увеличению частоты аденомы гипофиза. Значимость этих фактов для человека не установлена.
В двухгодичных исследованиях у мышей, получавших гозерелин п/к в дозах до 2400 мкг/кг (выше МРДЧ примерно в 70 раз, в пересчете на мг/м 2 основания) каждые 3 нед , показано, что увеличивалась частота гистиоцитарных сарком позвоночника и бедренной кости.
В опытах на собаках при использовании в течение 1 года доз, превышающих МРДЧ в 100 раз, и на обезьянах, с применением в течение 6 мес доз, до 200 раз превышающих МРДЧ , повышения частоты развития аденом гипофиза выявлено не было; полученные данные наводят на мысль о видоспецифичном ответе.
Мутагенность. Гозерелин не проявлял мутагенных свойств в тестах с использованием бактериальных систем и систем клеток млекопитающих для оценки точечных мутаций и цитогенетических эффектов.
Беременность. Подавление секреции тестостерона приводит к нарушению фертильности. Неизвестно, восстанавливается ли фертильность после отмены гозерелина, но после отмены сходных аналогов восстановление фертильности происходило.
Исследования у крыс и кроликов при использовании гозерелина в дозах, примерно равных или бóльших чем 2 и 20 мг/кг/сут (около 1/10 и 2 МРДЧ , в пересчете на мг основания/м 2 ), введенных в период органогенеза, показали, что гозерелин приводит к увеличению частоты выкидышей, эмбриотоксичности/фетотоксичности (характеризуются повышением предимплантационных потерь, увеличением резорбции, повышением вероятности развития пупочной грыжи у крыс) при дозах ≥10 мкг/кг/сут (около 1/2 МРДЧ , в мг основания/м 2 ), эффект — дозозависимый. Кроме того, исследования репродукции показали, что гозерелин снижает выживание плодов и детенышей.
После п/к введения в дозе 50 и 1000 мг/кг крысам и кроликам гозерелин проходит через плаценту.
Биодоступность высокая. В первые 8 дней после введения гозерелин высвобождается из депо более медленно, чем в течение остальной части 28-дневного периода времени между введениями. Связывание с белками плазмы — около 30%. Cmax в плазме достигается примерно через 2–3 ч после введения у мужчин и через 1,5–2 ч — у женщин; после лечения в дозе 3,6 мг в течение 2 мес значительный уровень сохраняется в течение 12–15 и 22 дней соответственно. Т1/2 — 2,5 ч у женщин и 4,2 ч у мужчин, несколько увеличивается при хронической почечной недостаточности (коррекция режима дозирования не требуется). Не кумулирует.
Применение вещества Гозерелин
Гозерелин 3,6 мг: гормонозависимый рак предстательной железы, гормонозависимый рак молочной железы у женщин в репродуктивном периоде или в перименопаузе, эндометриоз, необходимость предварительного истончения эндометрия перед хирургическим вмешательством, фибромиома матки (в комплексе с хирургическим лечением), для угнетения функции гипофиза при подготовке стимуляции суперовуляции в рамках программы ЭКО (экстракорпоральное оплодотворение).
Гозерелин 10,8 мг: гормонозависимый рак предстательной железы, эндометриоз, фибромиома матки.
Противопоказания
Гиперчувствительность, в т.ч. к другим аналогам ГнРГ; детский и подростковый возраст (до 14 лет).
Ограничения к применению
Обструкция мочевыводящих путей (в анамнезе у мужчин), метастазы в позвоночник (риск сдавления спинного мозга в результате обострения заболевания в начале лечения).
Применение при беременности и кормлении грудью
Противопоказано при беременности (адекватных и строго контролируемых исследований у человека не проведено). Гозерелин может оказывать вредное эмбриональное воздействие при введении беременным женщинам. Влияние на репродуктивную функцию как результат антигонадотропных свойств вещества наблюдается при хроническом введении. У женщин детородного возраста перед началом терапии необходимо исключить беременность. Женщинам необходимо использовать для контрацепции негормональные методы в период лечения гозерелином и в течение 12 нед после его отмены. Если гозерелин применяют при беременности или если беременность наступила при терапии гозерелином, пациентка должна быть предупреждена о потенциальном вреде для плода и риске самопроизвольного выкидыша.
На время лечения следует прекратить грудное вскармливание (неизвестно, проникает ли гозерелин в грудное молоко женщин, но известно, что гозерелин экскретируется в молоко лактирующих крыс).
Побочные действия вещества Гозерелин
Со стороны нервной системы и органов чувств: головокружение, головная боль, нарушение сна, чрезмерная утомляемость или слабость, тревожность, депрессия, парестезия, нарушение мозгового кровообращения.
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): лабильность АД , повышение АД , аритмия, инфаркт миокарда, окклюзионные нарушения периферического кровообращения (болезненность или похолодание кистей и стоп), усугубление хронической сердечной недостаточности (отечность стоп, лодыжек), анемия.
Со стороны респираторной системы: обострение ХОБЛ , инфекция верхних дыхательных путей.
Со стороны органов ЖКТ : снижение аппетита, тошнота, рвота, запор или диарея.
Аллергические реакции: кожная сыпь, анафилактоидные реакции.
Прочие: обострение симптомов рака молочной железы, увеличение массы тела, гиперкальциемия (у больных с костными метастазами), подагра (боль в суставах), усиление потоотделения, приливы; у мужчин — обструкция мочевыводящих путей, синдром сдавления спинного мозга, снижение потенции, гинекомастия; у женщин — сухость слизистой оболочки влагалища, приливы, лабильность настроения, снижение либидо, менопауза, аменорея (после отмены терапии возобновления менструации может не произойти), кровянистые выделения (в начале лечения), образование кист яичников, снижение плотности костной ткани и костной массы.
Пути введения
Меры предосторожности вещества Гозерелин
Больные, получающие гозерелин, должны находиться под наблюдением врача. В связи с повышением частоты обострения заболевания ввиду увеличения концентрации тестостерона в крови, возникновения обструкции мочевыводящих путей и сдавления спинного мозга при наличии метастазов необходимо проводить систематический контроль состояния в течение первого месяца терапии, включая определение в сыворотке крови концентрации тестостерона, антигена предстательной железы, активности кислой фосфатазы.
Боль в костях при временном внезапном обострении болезни можно лечить симптоматически. Сдавление спинного мозга или почечную недостаточность, обусловленную обструкцией мочеточника, следует лечить общепринятым способом. В крайнем случае следует прибегнуть к орхиэктомии.
Повторные курсы при доброкачественных гинекологических заболеваниях не рекомендуются в связи с высокой вероятностью проявлений остеопороза. После отмены терапии возможно прогрессивное восстановление плотности костной ткани.
На фоне лечения повышается тонус шейки матки, могут возникнуть трудности при расширении шейки матки.
С осторожностью применяют гозерелин 3,6 мг при ЭКО у пациенток с синдромом поликистозных яичников, т.к. возможна стимуляция большого количества фолликулов.
К сожалению, онкологическими патологиями половых органов, а также проблемами с репродуктивной системой как мужчин, так и женщин никого не удивишь. Если не бороться с этими заболеваниями, то человек может умереть. «Гозерелин», инструкция по применению которого обязательно должна быть изучена пациентом, как раз и предназначен для лечения таких болезней.
Форма выпуска и особенности действия
Итак, данный препарат является синтетическим заменителем гонадотропин-рилизинг гормона. Длительный прием этого лекарства способствует снижению количества эстрадиола у женщин и тестостерона у мужчин. Это позволяет снизить скорость роста злокачественных опухолей простаты, молочной железы, миомы матки или полностью остановить его.

Что касается формы выпуска, то «Гозерелин» (инструкция по применению находится в упаковке с лекарством) продается в депо-капсулах в шприцах-аппликаторах, обладающих защитным механизмом. Их емкость составляет 3,6 мг. Кроме того, можно найти препарат в форме капсул продолжительного действия, вводимых под кожу. Их емкость в этом случае составляет 10,8 мг. Их тоже можно приобрести в специальном шприце-аппликаторе, оснащенном защитным механизмом.
Лекарство обладает высокой биодоступностью. Максимальный уровень концентрации в крови достигается уже через 1,5-3 часа после приема в зависимости от пола пациента. Что касается состава средства, то гозерелин сам по себе является главным действующим веществом.
Показания к использованию
Итак, для того чтобы начать принимать «Гозерелин», инструкция по применению предусматривает такие показания:
- Рак простаты у мужчин.
- Онкологическое заболевание груди у женщин, которые находятся в репродуктивном или предменопаузальном возрасте.
- Эндометриоз матки.
- Хирургическое вмешательство, которое требует предварительной подготовки — истончения эндометриального слоя.
- Миома матки.
- Подавление функциональной активности гипофиза в случае будущего искусственного оплодотворения.

Какие противопоказания существуют?
Как у всякого медикаментозного средства, есть противопоказания и к препарату «Гозерелин». Инструкция по применению предупреждает о таких запретах на прием данного лекарства:
- Слишком высокая чувствительность к препарату.
- Аллергическая реакция.
- Детский возраст до 14 лет.
- Кормление грудью.
- Беременность (даже если она и сохранится, у плода впоследствии могут возникнуть патологии внутриутробного развития).
- Сдавливание костного мозга.
- Непроходимость мочеточников.
Особенности применения
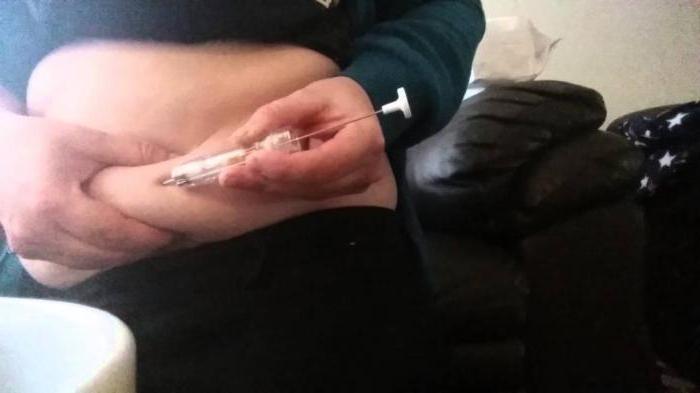
Если пациенту необходимо использовать «Гозерелин», инструкция по применению (длительность применения строго определяется врачом) должна быть внимательно изучена. В ней содержатся сведения о таких особенностях приема: капсула предназначена для подкожного введения. Ее локализация — передняя брюшная стенка.
Если производится лечение гинекологических патологий, то принимать капсулу следует каждый месяц. Дозировка составляет 3,6 мг. Для борьбы с раком простаты мужчине вводится 10,8 мг каждые 12 недель.
Нельзя забывать, что первые недели терапии самочувствие пациента сильно ухудшается, так как уровень гормонов возрастает. Это нормальная реакция на принимаемый препарат.
Длительность курса лечения определяется индивидуально. При гинекологических патологиях он может составлять не более полугода. Важно помнить, что если пациенту назначен «Гозерелин», инструкция не предусматривает прохождение повторного курса лечения. Дело в том, что препарат способствует уменьшению плотности костной ткани и развитию остеопороза.
Если прием капсулы был по каким-то причинам пропущен, то необходимо осуществить его сразу, как только пациент вспомнил об этом. У женщин, которые пропустили очередной прием лекарства, существует риск маточного кровотечения.
Какие нежелательные реакции могут возникнуть?
Если пациенту необходимо длительное время принимать такой препарат, как «Гозерелин», инструкция и отзывы других пациентов дадут возможность понять, как он действует. Естественно, каждому будет интересно, какие побочные эффекты может вызвать представленное лекарство.
У мужчин могут появляться такие реакции:
- Снижение потенции и полового влечения.
- Опухание груди и ее болезненность (не часто).
- Нарушение проходимости мочеточников.

У женщин же могут появляться такие побочные эффекты:
- Усиленное выделение пота.
- Частые смены настроения и депрессивное состояние.
- Боль в голове.
- Сухость слизистых оболочек половых органов.
- Сильное снижение полового влечения.
- Деминерализация костной ткани, что приводит к хрупкости костей.
- Изменение размера груди.
- Наступление климакса (в большинстве случаев месячное кровотечение не восстанавливается).
Общими для обоих полов являются еще и такие побочные эффекты: сыпь на коже, инфекции носа, повышение артериального давления, нарушение сердечного ритма.
Особые указания, взаимодействие и отзывы
Итак, если больному необходимо принимать препарат «Гозерелин», инструкция (состав препарата уже известен) дает такие особые указания:
- Капсулы нельзя принимать совместно с алкоголем, так как это усиливает деминерализацию костей.
- Не следует вместе с представленным препаратом пить противосудорожные средства, а также глюкокортикостероиды.
Что касается отзывов, то в них много говорится о большом количестве побочных эффектов и плохом самочувствии в первые недели лечения. Не всем пациентам препарат помогает, хотя в большинстве случаев он все-таки оказывается эффективным.

Если специалист считает, что больному желательно принимать «Гозерелин», инструкция по применению (отзывы врачей необходимо обязательно учитывать) должна постоянно быть под рукой у пациента на протяжении всего периода лечения. Специалисты же едины в своем мнении: несмотря на большое количество нежелательных реакций, которые проявляются практически у каждого больного, лекарство является достаточно эффективным.
Особые рекомендации
Есть ситуации, когда после приема препарата необходимо обратиться к доктору. Например, если:
- Начали появляться признаки повышения внутричерепного давления.
- Проявились признаки кровоизлияния в гипофиз: внезапная и сильная боль в голове, проблемы со зрением, головокружение, путаная речь. Эти симптомы могут появиться уже через 2 недели после начала терапии.
- Есть признаки сдавливания спинномозгового канала или проблемы с мочевыводящими путями. На это обычно указывает боль в области поясницы, слишком трудное движение верхних и нижних конечностей, примесь крови в моче. Мочеиспускание является болезненным.
Есть также некоторые факты, которые требуется учитывать еще перед началом лечения:
- Анамнез пациента, в котором учитывается наличие остеопороза, высокого содержания холестерина в крови, а также наличие маточных кровотечений непонятной природы, тромбозов у больного и его родственников.
- Склонность человека к курению, ведь эта вредная привычка способствует образованию тромбов.
- Желание пациентки иметь ребенка в ближайшее время или уже наступившую беременность.
- Прием любых медикаментозных препаратов, даже тех, которые отпускаются без рецепта. Важно рассказать доктору обо всех биологических добавках, которые принимаются, а также травяных отварах, которые используются в лечении.
- Наличие аллергической реакции на какие-либо препараты.
Особенности хранения и аналоги
Как и любой другой медикаментозный препарат, «Гозерелин» необходимо хранить при комнатной температуре, в месте, которое хорошо защищено от ультрафиолетовых лучей и детей.
Если у больного нет возможности принимать «Гозерелин», инструкция по применению (аналоги могут справиться с этой проблемой) советует проконсультироваться с доктором. Тем более что указанный препарат имеет высокую стоимость — от 8000 руб. за шприц. Среди аналогов можно отметить «Золадекс», «Бусерелин».
Вот и все особенности представленного средства. Будьте здоровы!
Похожие темы научных работ по клинической медицине , автор научной работы — Izaguirre Alejandra, Roach Iii Mask
Диагностика и лечение опухолей мочеполовой системы
Применение гозерелина ацетата в сочетании с лучевой терапией при лечении рака предстательной железы
Mask Roach III & Alejandra Izaguirre
Department of Radiation Oncology, University of California San Francisco, UCSF Comprehensive Cancer Center, 1600 Divisadero Street, Suite H1031, San Francisco, California 94143-1708, USA Expert Opin Pharmacother 2007;8(2):257—64
Рак предстательной железы (РПЖ) характеризуется наиболее высокой заболеваемостью (за исключением рака кожи) и смертностью среди злокачественных опухолей у мужчин. В США число выявленных случаев РПЖ в 2006 г. достигло 234 000, а смертельных исходов — 27 350 [1]. На основании этих показателей каждый третий случай злокачественной опухоли у мужчин представлен РПЖ. С 1994 по 2002 г. наблюдалось снижение смертности от РПЖ на 4%. Число летальных исходов сократилось с 34 902 случаев в 1994 г. до 7552 смертей ежегодно. Чем же объясняется наблюдаемая тенденция изменения частоты летальности от РПЖ? Рутинное использование уровня простат-специфического антигена (ПСА) не было внедрено до начала 90-х гг., и больные с ранними стадиями РПЖ могли прожить длительное время (10—20 лет) даже без лечения. Следовательно, снижение летальности не может быть вызвано применением скрининговых методов диагностики [2, 3] и скорее всего связано с уменьшением смертности среди больных местно-распространенным РПЖ и РПЖ высокого риска. Наиболее вероятная причина снижения летальности от РПЖ — раннее применение препаратов класса лютеинизирующего гормона рилизинг-гормона (ЛГРГ), в частности гозерилина ацетата (ГА).
Клиническая эффективность: рандомизированные исследования III фазы по применению максимальной андрогенной блокады и лучевой терапии
В большинстве исследований, выявивших преимущество применения максимальной андрогенной блокады (МАБ) у больных местно-распро-страненным РПЖ, лечение проводили в сочетании с лучевой терапией (ЛТ). В табл. 1 суммированы результаты клинических исследований (включая обновленную информацию об исследованиях,
опубликованных с 1995 по 1999 гг.). В целом, в рамках этих исследований более чем 6000 пациентов было проведено лечение и свыше 90% больных получали ГА в качестве МАБ.
Во всех завершенных проспективных рандомизированных исследованиях, в том числе в испытаниях 85—31 и 92—02 RTOG (Онкологическая группа по изучению ЛТ), EORTC (Европейская организация по исследованию и лечению рака) и Шведском исследовании, было продемонстрировано, что длительное применение адъювантной ГТ улучшило выживаемость больных группы высокого риска при сочетании ее с ЛТ [5, 7, 13, 14]. У этих пациентов отмечены местная распространенность процесса (стадии Т2с—Т3), наличие высоких показателей по шкале Глисона (7—10) и высокий уровень ПСА (> 20 нг/мл), у значительного числа больных также определялись пораженные лимфоузлы. Результаты данных 4 работ согласуются с выводами метааналитического изучения исследований RTOG: выявлено повышение общей выживаемости на 20% при длительном применении адъювантной ГТ в сочетании с ЛТ у больных группы высокого риска [15]. Метаанализ также показал отсутствие преимуществ применения ГТ в группе низкого риска.
У пациентов группы умеренного риска роль ГТ изучается. В каждом из 3 исследований по сравнению ЛТ в монотерапии и сочетания ЛТ с коротким курсом неоадъювантной ГТ наблюдали худшие результаты у больных, получивших только ЛТ [9, 12, 16]. Несмотря на разнообразие дизайнов исследований и определений ПСА-рециди-вов, существуют доказательства большей эффективности использования неоадъювантной ГТ в группе умеренного риска, согласно всем опубликованным рандомизированным исследованиям, в которых применяли общепринятые дозы и методики ЛТ. Нет данных, подтверждающих, что при-
ОНКОУРОЛОГИЯ 2′ 2 0 0 8 Диагностика и лечение опухолей мочеполовой системы
Таблица 1. Использование ГА в сочетании с ЛТ или хирургическим лечением у мужчин с клинически локализованным РПЖ
Pilepich (2001) [4] 456 пациентов с T2—4N0 стадией; Отсутствие терапии Преимущество в выживаемости
ЛТ ± ГТ* (2 мес до + 2 мес в сравнении для пациентов с GS** Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
ПСА Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Диагностика и лечение опухолей мочеполовой системы 2′ 2 0 0 8
менение неоадъювантной ГТ эффективно у больных группы умеренного риска при использовании эскалации дозы ЛТ и направляющих технологий, таких как трехмерная конформа-ционная ЛТ или ЛТ с модуляцией интенсивности.
Безопасность и переносимость
В клинических исследованиях отмечена относительно удовлетворительная переносимость ГА. Побочные эффекты редко достигали высокой степени выраженности, обусловливающей прекращение лечения.
Побочные эффекты, наблюдаемые у больных, участвовавших в контролируемых клинических исследованиях по сравнению эффективности применения ГА и орхиэктомии, описаны в табл. 2 [17].
Наиболее часто встречающиеся побочные эффекты (более 5%) приведены в табл. 3. Выводы
В литературе опубликова-
Примечание. Здесь и в табл. 3 представлен процент больных.
но много данных, свидетельствующих о достоверном улучшении бе3рецидивной и общей Таблица 3. Острые и поздние лучевые реакции
выживаемости при использовании ГА в сочетании с дистанционной ЛТ у больных РПЖ группы высокого риска.
Уменьшение смертности от РПЖ на 4% вероятнее всего объясняется ранним началом применения МАБ. Значение ПСА-скрининга в этом отношении сомнительно. Из 11 рандомизированных исследований III фазы, продемонстрировавших эффективность использования МАБ при лечении больных РПЖ с клинически локализованным процессом, в 10 был назначен ГА.
Таблица 2. Побочные эффекты при применении ГА
и орхиэктомии для лечения больных РПЖ
Горячие приливы 62
Сексуальная дисфункция 21
Снижение эрекции 18
Симптомы блокады мочевого тракта 13
Инфекция верхних дыхательных путей 7
Хронические обструктивные заболевания легких 5
Сердечные нарушения 5
Осложнения хирургического лечения 0
Флутамид + ГА + ЛТ (и=231)
ЛТ в монорежиме (n=235)
Острые лучевые реакции
Прямая кишка/толстая кишка 80
Мочевой пузырь 58
Кожа 37 Поздние лучевые реакции
Ректальные кровотечения 14
ОНКОУРОЛОГИЯ 2 ‘ 2 0 0 8 Диагностика и лечение опухолей мочеполовой системы
1. Jemal A., Siegel R., Ward E. et al. Cancer statistics, 2006. CA Cancer J Clin 2006;56:106-30.
2. Albertsen P.C., Hanley J.A., Gleason D.F., Barry M.J. Competing risk analysis of men aged 55 to 74 years at diagnosis managed conservatively for clinically localized prostate cancer. JAMA 1998;280:975-80.
3. Johansson J.E., Andren O., Andersson S.O. et al. Natural history of early, localized prostate cancer. JAMA 2004;291:2713-9.
4. Pilepich M.V., Winter K., John M.J. et al. Phase III radiation therapy oncology group (RTOG) trial 86-10 of androgen deprivation adjuvant to definitive radiotherapy in locally advanced carcinoma of the prostate. Int J Radiat Oncol Biol Phys 2001;50:1243-52.
5. Bolla M., Collette L., Blank L. et al. Long-term results with immediate androgen suppression and external irradiation in patients with locally advanced prostate cancer (an EORTC study): a Phase III randomised trial. Lancet 2002;360:103-6.
6. Roach M. III, Desilvio M., Lawton C. et al. Phase III trial comparing whole-pelvic versus prostate-only radiotherapy and neoadjuvant versus adjuvant combined androgen suppression: Radiation Therapy Oncology Group 9413. Clin Oncol 2003;21:1904-11.
7. Hanks G.E., Pajak T.F., Porter A. et al. Phase III trial of long-term adjuvant androgen deprivation after neoadjuvant hormon-
al cytoreduction and radiotherapy in locally advanced carcinoma of the prostate: the Radiation Therapy Oncology Group Protocol 92-02. Clin Oncol 2003;21:3972-8.
8. Laverdiere J., Gomez J.L., Cusan L. et al. Beneficial effect of combination hormonal therapy administered prior and following external beam radiation therapy in localized prostate cancer. Int J Radiat Oncol Biol Phys 1997;37:247-52.
9. D’Amico A.V., Manola J., Loffredo M. et al. 6-Month androgen suppression plus radiation therapy versus radiation therapy alone for patients with clinically localized prostate cancer: a randomized controlled trial. JAMA 2004;292:821-7.
10. Crook J., Ludgate C., Malone S. et al. Report of a multicenter Canadian Phase III randomized trial of 3 months versus 8 months neoadjuvant androgen deprivation before standard-dose radiotherapy for clinically localized prostate cancer. Int J Radiat Oncol Biol Phys 2004;60:15-23.
11. Pilepich M.V., Winter K., Lawton C.A. et al. Androgen suppression adjuvant to definitive radiotherapy in prostate carcinoma-long-term results of Phase III RTOG 85-31. Int J Radiat Oncol Biol Phys 2005;61:1285-90.
12. Denham J.W., Steigler A., Lamb D.S. et al. Short-term androgen deprivation and radiotherapy for locally advanced prostate cancer: results from the Trans-Tasman
Radiation Oncology Group 96.01 randomised controlled trial. Lancet Oncol 2005;6:841-50.
Гормональное лечение рака предстательной железы
Рак предстательной железы относится к числу наиболее тяжелых и часто встречающихся онкологических заболеваний. Среди причин смерти от злокачественных заболеваний рак предстательной железы во многих странах занимает второе-третье места.
В частности, в США он является одной из самых распространенных форм злокачественных опухолей у лиц мужского пола: в 1996 году заболеваемость составила 317 тыс. новых случаев в год, смертность — 41 400. Рост заболеваемости и смертности отмечается также и в России. В 1989 году этот показатель составлял 8,4 на 100 тыс.
населения, в 1996 году уже 11,3 [1]. Таким образом, темпы прироста за данный период оказались равны 34,5%, а смертности — 18,5%.
Гормонотерапия при раке предстательной железы позволяет приостановить рост опухоли, зависящей от мужского полового гормона — тестостерона. Лечение направлено на снижение выработки этого вещества в организме.
Существует несколько схем гормональной терапии при раке простаты, выбор которых зависит от типа и стадии развития опухоли, возраста пациента, общего состояния организма и наличия сопутствующих заболеваний.
Препараты могут использоваться как отдельно, так и в сочетании с другими методами лечения.
Подобное лечение может назначаться после хирургического вмешательства или курса лучевой терапии для профилактики повторного роста новообразования. Применяются гормональные препараты и на поздних стадиях рака, когда он становится неоперабельным.
Терапия позволяет предотвратить распространение метастазов и приостановить процессы деления атипичных клеток. Как правило, это касается пожилых пациентов.
Можно считать, что гормональная терапия считается паллиативным методом, ее редко используют на ранних стадиях, ограничиваясь облучением и операцией.
Хирургическая кастрация — метод, проверенный временем. Выработка тестостерона после такой операции сокращается на 90%. Так как после удаления яичек в организме происходят необратимые изменения, оно используется для лечения рака простаты у пожилых мужчин.
Основным недостатком этого метода является невозможность восстановления процессов синтеза половых гормонов. Процедура приводит к множеству неприятных изменений в организме. Увеличение толщины подкожной жировой клетчатки способствует ожирению. Наблюдается оволосение по женскому типу.

Импотенция — наиболее неприятное для мужчины последствие кастрации.
Перед проведением подобной операции необходимо осуществить тщательно обследование пациента. Нужно не только подтвердить наличие рака простаты с помощью гистологического анализа, но и провести ряд других исследований.
К ним относятся:
- общий и биохимический анализы крови;
- исследование на наличии инфекций, передаваемых половым путем.
Помимо результатов лабораторных диагностических процедур, врач должен изучить рентгеновский снимок органов грудной клетки, получить заключение кардиолога об отсутствии противопоказаний к проведению операции.
Медикаментозная кастрация — более безопасный вид гормональной терапии при раке предстательной железы.
Специальные препараты блокируют выработку тестостерона, терапевтическое действие начинается на 14-21 день введения вещества.
Химическая кастрация приносит меньше опасных для здоровья мужчины последствий, все изменения имеют обратимый характер. Использование этого способа целесообразно лишь на ранних стадиях заболевания.
Введение агонистов ЛГРГ — новейший метод гормонального лечения рака простаты. Специальные вещества нейтрализуют вырабатываемый тестостерон. Препарат вводят 1 раз в 30 дней.
Выработка тестостерона при этом не прекращается. Очень часто этот метод применяется в сочетании с кастрацией.
Любое вмешательство в работу организма, будь то операция или лечение гормонами, приводит как к незначительным, так и к тяжелым необратимым последствиям. Возможными осложнениями гормональной терапии являются:
- повышение чувствительности сосков и гинекомастия;
- синдром хронической усталости;
- депрессивные расстройства;
- резкие смены настроения.
Нередко на фоне снижения выработки мужских гормонов развивается остеопороз — патологическое снижение плотности костных тканей. Анемия — не менее распространенное последствие гормональной терапии, сопровождающееся снижением уровня гемоглобина в крови. Гормоны влияют и на центральную нервную систему, способствуя ухудшению памяти, снижению концентрации внимания, нарушению сна.
Гормонотерапия при раке предстательной железы, как и любой другой способ лечения, требует соблюдения всех рекомендаций врача. Помимо приема препаратов, необходимо пересмотреть рацион. Продукты с высоким содержанием жиров должны быть исключены, то же касается острых и соленых блюд.
Необходимо есть как можно больше свежих овощей и фруктов, кисломолочных продуктов. Питаться нужно 5-6 раз в день небольшими порциями. Кофе и алкоголь при гормонотерапии категорически противопоказаны. Следует соблюдать специальный питьевой режим, количество потребляемой в сутки жидкости доводят до 3-4 л.
Курение может спровоцировать активность раковых клеток, поэтому от этой привычки нужно избавиться раз и навсегда. Пациент должен организовать оптимальный режим труда и отдыха, исключить тяжелые физические нагрузки. Однако и малоподвижный образ жизни вреден.
Избегать нужно не только стрессов, но и травмоопасных ситуаций, способных спровоцировать рост опухоли.
Именно снижение ПСА свидетельствует об эффективности терапии. Несмотря на большое количество противопоказаний и побочных действий, от применения гормонов не стоит отказываться. На поздних стадиях рака оно становится единственным способом продления жизни и улучшения ее качества. На ранних этапах при правильном составлении схемы лечения возможно полное выздоровление.
Гормональное лечение рака простаты не поможет полностью избавиться от заболевания. Но оно остановит процесс прогрессирования болезни и существенно улучшит самочувствие пациента. Тестостерон – это мужские половые гормоны, способствующие прогрессированию и развитию злокачественной опухоли простаты.
Целью гормональной терапии является снижение выделение организмом тестостерона, а также блокирование его действия. Индивидуально для каждого пациента подбирается один из существующих способов гормонотерапия. Врачи обращает внимание на такие факторы:
- Показатели веса и роста;
- Общее состояние здоровья;
- Возраст;
- Стадия развития рака, распространенность опухоли;
В каких случаях назначается гормональная терапия при лечении рака простаты:
- Когда по показаниям не может быть проведения операция, радиационная терапия.
- В ситуации, когда рак распространился за пределы мужской железы;
- Перед проведением операции, чтобы уменьшить размер простаты;
- Если произошел рецидив рака мужской железы после проведенной операции, радиационного лечения;
- Перед проведением радиационной терапии, чтобы повысить эффективность процедуры;
- В комбинации с радиационной терапией, чтобы исключить рецидивы болезни, ее распространение за пределы железы;
Это операция, но она связана с гормональной перестройкой мужского организма. В течение операции удаляются яички, где вырабатывается более 90% андрогенов. Удаление яичек снижает концентрацию мужских гормонов в крови, что приводит к остановке роста опухоли, ее сморщиванию.
Операция выполняется в амбулаторных условиях, а для достижения удовлетворительного косметического эффекта на место удаленных яичек ставят искусственные имплантаты. Операция является более легким, а также дешевым способом, как снизить уровень андрогенов в крови.
Аналоги лютеинизирующего гормона
Препараты помогают достичь такой же эффект, который наблюдается после проведения операция. Уровень андрогенов в крови резко снижается. Прием таких препаратов оказывает эффект медикаментозной кастрации. В отличие от хирургической кастрации эффект от приема этих препаратов является обратимым.
Лекарственные средства данной категории продаются в виде подкожных инъекций. В зависимости от конкретного вида частота приема может быть раз в месяц или даже раз в год.
Полностью избавить от заболевания гормональное лечение рака предстательной железы не способно, но может существенно замедлить его прогрессирование и улучшить самочувствие пациента.
Развитию и прогрессированию злокачественной опухоли простаты способствуют половые мужские гормоны – тестостероны. Опухолевые клетки чувствительны к действию этих гормонов. Поэтому целью применения гормональных препаратов является снижение выделения организмом тестостерона или блокирование его действия.
Есть несколько способов применения гормонотерапии, которые подбираются индивидуально для каждого пациента, в зависимости от следующих факторов:
- Вес и рост пациента;
- Возраст;
- Общее состояние здоровья;
- Стадия развития заболевание и его распространенность.
Как правило, на ранних стадиях заболевания гормоны не назначают. В таких случаях стараются прибегать к радикальным методам лечения или к облучению. Однако есть ряд противопоказаний к этим методам, тогда используют гормоны.
В некоторых случаях после хирургического удаления опухоли остается большой риск рецидива. Тогда врач сразу после операции назначает курс гормонотерапии.
Гормонотерапия при раке простаты: основные методы терапии
Гормонотерапия при раке простаты рекомендована мужчинам, у которых опухоль уже вышла за пределы предстательной железы.
Также она помогает мужчинам, которые планируют операцию и хотят уменьшить опухоль, чтобы повысить эффективность хирургического вмешательства. Кроме того, гормонотерапию назначают людям с рецидивом рака простаты.
Гормональная терапия обычно используется во время роста ПСА.
Есть три основных вида гормонотерапии при раке простаты. Это имплантанты, предотвращающие производство тестостерона в яичках, таблетки, блокирующие эффекты тестостерона и кастрация, то есть хирургическое удаление яичек полностью или лишь частей яичек, ответственных за выработку тестостерона.

Эта операция носит название орхиэктомия. Предпочтительный тип лечения гормонами зависит от локализации рака, степени его роста и действенности других терапевтических методов.
Агонисты ЛГРГ (лютеинизирующего гормона рилизинг-гормона) являются наиболее распространенным типом инъекций или имплантатов.
Есть несколько различных агонистов ЛГРГ, в том числе:
- гозерелин (бренды Золадекс или Новагос);
- лейпрорелин ацетат (Простап или Лейпрорелин);
- трипторелин (Декапептил депо);
- бусерелина ацетат (Супрефакт).
Агонисты ЛГРГ заставляют организм вырабатывать больше тестостерона в течение короткого промежутка времени после первой инъекции.
Этот временный всплеск тестостерона может заставить рак расти быстрее в течение короткого промежутка времени, который может усилить симптомы у больного.
Чтобы побороть этот всплеск больному, принимающему агонисты ЛГРГА, назначают краткий курс анти-андрогенных лекарственных средств.
Существуют медикаментозные препараты, позволяющие предотвратить попадание тестостерона в раковые клетки. Эти таблетки называются антиандрогенами.
Антиандрогенная гормонотерапия при раке простаты реже вызывает сексуальные проблемы и истончение костей, чем другие виды гормональной терапии. Но она часто вызывает боль и отек груди. При прогрессирующем заболевании блокирование тестостерона антиандрогенами не оказывает большого эффекта на ход лечения.
Есть несколько различных антиандрогенов, в том числе:
- бикалутамид (например, Касодекс);
- флутамид (например, Дрогенил);
- ципротерона ацетат (например, Ципростат).
Гормонотерапия рака простаты при помощи эстрогенов используется не часто из-за повышенного риска образования тромбов, сердечного приступа и инсульта. Есть предположение, что пероральный прием эстрогенов влияет на печень, которая затем производит химические вещества, провоцирующие данные побочные эффекты.
Когда мужчинам дают эстроген для лечения рака предстательной железы, им, как правило, вводят синтетическую форму лекарственного средства — диэтилстильбэстрол.
Мозг человека интерпретирует присутствие диэтилстильбэстрола как тестостерон, так что гипоталамус прекращает вырабатывать гормон, высвобождающий лютеинизирующий гормон. Результат — значительное снижение уровня тестостерона.
Природные эстрогены и диетические аналоги эстрогена, как предполагают ученые, могут быть защитой против развития рака простаты, а не просто средством для лечения заболеваний предстательной железы.
Существует свидетельство защитного эффекта генистеина, выявленного в ходе исследований с использованием грызунов. В двух отдельных исследованиях, Ментор-Марсель и его коллеги исследовали влияние генистеина на прогрессирование рака простаты у мышей.
При поднятии в сыворотки крови мыши уровня генистеина до уровня, сравнимого с азиатскими мужчинами, часто употребляющих тофу, скорость слабо дифференцированной аденокарциномы снизилась в зависимости от дозы. В то же время улучшилось выживание подопытных мышей.
Недавние исследования с использованием гормональной модели канцерогенеза крысы показали, что смесь изофлавонов сои, которая включает в себя генистеин и диадзеин, способна защитить от канцерогенеза в дорсолатеральной и передней доле простаты. Исследования в пробирке показали, что генистеин по отдельности или в сочетании с селеном ингибирует рост раковых клеток простаты.
У терапии гормонами в отличие от оперативного метода антиракового лечения (простатэктомии) имеется значительное преимущество — отсутствие необходимости в госпитализации.
Все что нужно — в назначенное время приходить в больницу на процедуры.
В этом гормонотерапия схожа с лучевой терапией.
Однако, в отличие от лучевой терапии, гормональная не повреждает соседние, здоровые ткани.
К основным недостаткам использования гормонов больные относят изменение в большую сторону размера груди и снижение сексуального влечения.
Некоторые из опухолевых клеток не чувствительны к колебаниям уровня тестостерона, а это значит, что гормональная терапия при раке простаты не может остановить рак, она только замедляет его.

Однако большинство исследований, которые рассматривали вопрос эффективности и целесообразности гормональной терапии, пришли к выводу, что ее начало на ранней стадии болезни, сразу после обнаружения метастазов, позволяет достигнуть лучших результатов.
Это относится даже к мужчинам, у которых болезнь затронула только лимфатические узлы.
Для сравнения: только 18% мужчин, которые решили отказаться от гормональной терапии до распространения рака в кости или легкие были живы спустя 7 лет после начала болезни.
Тестостерон является основным мужским гормоном, и он играет важную роль в создании и поддержании типичных мужских характеристик, таких как рост волос на теле, мышечная масса, половое влечение и эректильная функция, а также способствует целому ряду других нормальных физиологических процессов в организме.
Гормональная терапия при раке простаты имеет ряд негативных эффектов, которые включают:
- приливы;
- изменения в сексуальной жизни, включая потерю либидо и проблемы с эрекцией;
- крайнюю усталость;
- увеличение веса;
- уменьшение мышечной массы и, следовательно, силы;
- набухание груди;
- потерю волос на теле;
- истончение костей;
- большую вероятность развития диабета, болезней сердца и инсульта;
- изменения настроения;
- проблемы с кожей.
Есть несколько изменений образа жизни, которые могут помочь улучшить настроение больного и облегчить чувство депрессии и тревоги. К ним относятся: регулярная физическая активность и занятие своими обычными увлечениями и общественной деятельностью.

Если мужчина, проходящий гормональную терапию при раке простаты, чувствует себя крайне подавленно, врач может прописать ему антидепрессанты.
Самостоятельно назначать их себе не следует, так как эти лекарства имеют ряд побочных эффектов, которые стоит учитывать при выборе подходящего препарата.
Набухание груди может заставить мужчину чувствовать себя некомфортно или стесняться своего тела.
Побочные эффекты, как правило, длятся до конца гормональной терапии. После ее прекращения уровень тестостерона будет постепенно расти, и большинство побочных эффектов исчезнут. Это может занять несколько месяцев.
Пациенту важно получать достаточное количество кальция и витамина D. Оба этих вещества играют важную роль для здоровья костей, на которое негативно влияет гормонотерапия.
Больному необходимо получать с едой 1200-1500 мг кальция каждый день.
Кальций содержится как в молочных продуктах (сыр, молоко и йогурт), так и в немолочных (например, в консервированных сардинах с костями, тофу и капусте).
Гормонотерапия рака простаты назначается на ранних стадиях заболевания, при рецидивах, а также молодым больным как в составе комбинированного лечения, так и в виде самостоятельного метода.
Ещё в 1941 г. установлена гормональная природа рака простаты (РПЖ), поскольку кастрация и введение эстрогенов замедляло течение метастазирующих опухолей. С этого времени антиандрогенную терапию считают основой лечения поздних стадий РПЖ. Однако режимы и схемы терапии чётко не определены.
Хотя гормонотерапия рака простаты приносит хороший симптоматический эффект, не доказано, что она влияет на продолжительность жизни.
