Рубрику ведет профессор, д.м.н. Алексеев Б.Я.,
ведущий научный сотрудник ФГУ МНИОИ им П.А. Герцена
Интермиттирующая гормональная терапия – режим, при котором подразумевается циклическое применение гормональных препаратов, когда после начального индукционного курса гормонального лечения производится отмена препаратов на фоне ремиссии и их повторное назначение при появлении первых признаков прогрессирования заболевания.
Восстановление уровня тестостерона в периоды отсутствия терапии способствует улучшению качества жизни больных, проявляющееся преимущественно в восстановлении потенции и общего хорошего самочувствия. Имеются также теоретические и экспериментальные предпосылки, указывающие на возможность увеличения продолжительности времени до развития гормонорефрактерного рака предстательной железы (ГРРПЖ) при применении интермиттирующей терапии по сравнению с непрерывной. При этом доказано, что эффективность интермиттирующей терапии сравнима с таковой при непрерывной.
Несмотря на ряд вопросов, остающихся открытыми, интермиттирующая гормональная терапия при раке предстательной железы больше не считается экспериментальным методом. Проведение интермиттирующей терапии возможно только лекарственными гормональными препаратами (аналогами ЛГРГ и антиандрогенами) и может быть рекомендовано при лечении больных в различных клинических ситуациях, в том числе у пациентов с наличием отдаленных метастазов.
В 2009 г. Европейское общество урологов в своих рекомендациях сформулировало основные принципы проведения интермиттирующей гормональной терапии РПЖ:
- Продолжительность индукционного курса должна составлять 6–9 месяцев, иначе восстановление уровня тестостерона маловероятно
- Терапию гормональными препаратами возможно прекратить только при наличии всех следующих критериев
- Больной должен быть полностью проинформирован обо всех аспектах предполагаемого лечения
- У больного не должно наблюдаться признаков клинического прогрессирования заболевания
- На проводимую терапию должен наблюдаться ответ в виде снижения уровня ПСА, установленного эмпирически как величина 4 нг/мл у больных с отсутствием отдаленных метастазов или > 10–15 нг/мл у больных генерализованным РПЖ)
- Такую же терапию необходимо проводить на протяжении по крайней мере 3–6 мес
- Последующие циклы терапии следует проводить по тем же правилам до появления первых признаков ГРРПЖ.
ИНТЕРМИТТИРУЮЩАЯ ГОРМОНАЛЬНАЯ ТЕРАПИЯ ДИССЕМИНИРОВАННОГО РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Онкологическое отделение ЮВАО г.Москвы
Рак предстательной железы — часто встречающееся заболевание мужчин пожилого и старческого возраста. Заболеваемость раком простаты в России за последние 10 лет возросла на 60%, по уровню летальности в течение первого года после установления диагноза это заболевание в 1999г занимало третье место после рака щитовидной железы и гипернефромы. На начальных стадиях заболевание не дает яркой клинической симптоматики, поэтому среди первичных больных более 60% составляют пациенты с диссеминированным процессом, когда невозможно проведение радикального хирургического или лучевого лечения. 26% больных раком предстательной железы в нашей стране умирает в течение первого года после установления диагноза. В Москве, где возможности диагностики и терапии значительно шире чем в России, в 1999 году на онкологическом учете находилось 3705 больных этим злокачественным заболеванием, из них более 5 лет наблюдались всего 829 пациентов, летальность от рака простаты в столице составила 14,4%.
Общепринятым в настоящее время методом лечения генерализованного рака предстательной железы является гормональная терапия. При проведении гормонотерапии примерно у 70% больных улучшается общее состояние, качество жизни и увеличивается ее продолжительность. Общий принцип гормональной терапии при раке предстательной железы состоит в депривации андрогенной стимуляции опухолевых клеток простаты. Это может быть достигнуто в результате кастрации или с помощью лекарственных средств блокирующих выработку андрогенов и/или взаимодействие андрогенов с их рецепторами в клетках мишенях.
Наиболее популярным режимом гормонотерапии в последние два десятилетия стала максимальная андрогенная блокада (МАБ). Суть метода сводится к торможению продукции андрогенов, т.е. выполнению хирургической или медикаментозной кастрации в сочетании с блокадой циркулирующих андрогенов. Концепция МАБ явилась очень привлекательной, что привело к многочисленным клиническим исследованиям у больных распространенным раком предстательной железы. Полученные результаты в некоторых исследованиях показывали преимущество МАБ по сравнению с «золотым стандартом» лечения распространенного рака предстательной железы — двусторонней орхэктомией, но это преимущество заметно у группы больных с минимальными проявлениями метастатической болезни (единичные костные метастазы, поражение регионарных лимфатических узлов). При длительной терапии антиандрогенами возникает гормонрефрактерная фаза заболевания, и в этот момент необходимо прекращение проведения МАБ, т.к. известно, что у 10-15% пациентов наступает временная стабилизация заболевания на фоне прекращения гормонотерапии. Отмечено, что терапия антиандрогенами связана с риском побочных эффектов, ухудшающих качество жизни больных. Различными токсическими эффектами на желудочно-кишечный тракт, зрение, нервную систему обладают применяемые в настоящее время препараты. Другая немаловажная проблема — стоимость лечения при максимальной андрогенной блокаде, т.к. требуется длительное применение дорогостоящих лекарств.
Учитывая перечисленные выше проблемы, связанные с применением гормональной терапии, изучается эффективность прерывистой или интермиттирующей блокады андрогенов. Предварительные данные показывают, что прерывистое назначение антиандрогенов может длительно сохранить чувствительность к гормональной терапии, улучшает качество жизни и снижает частоту возникновения осложнений. Кроме того, при таком подходе значительно снижается стоимость лечения. Интермиттирующая блокада андрогенов уже широко применяется в клинической практике в лечении распространенного рака предстательной железы, однако режим этой методики гормональной терапии до конца не отработан. Открытыми остаются вопросы, какова должна быть оптимальная длительность вводного курса, в какой момент и на какой промежуток возможен перерыв в проведении лечения и какие показатели служат основанием для возобновления гормонотерапии.
Сайт медицинского фонда «Онкологическая урология» посвящен проблемам онкологической урологии в России. На нашем сайте вы надете множество полезной информации: публикации по онкологической тематике, каталог медицинских ресурсов, рекомендации по лечению, информацию о лекарственных средствах, советы онкологическим больным, их родным и близким и многое другое.
Отделение онкоурологии МНИОИ им. П. А. Герцена является одной из ведущих в России клиник, занимающихся диагностикой и лечением онкоурологических заболеваний:
- Опухоли полового члена
- Рак предстательной железы
- Рак мочевого пузыря
- Рак почки
- Реабилитация онкологических больных
В 1966 году специалисты – онкологи США обратили внимание на важную социальную проблему – реабилитацию онкологических больных. Проведение четырех международных конференций по проблемам реабилитации онкологических больных организационно закрепили стремление специалистов, работающих в области онкологии, объединить свои усилия по оказанию помощи больным. Так был заложен фундамент новому мультидисциплинарному направлению в онкологии. >>> - Реимплантация мочеточника
Реимплантация мочеточника при лечении стриктур мочеточника: ретроспективное сравнение лапароскопической и открытой техники. Подробнее >>
- В сообщении Practice Committee of the American Society for Reproductive Medicine были опубликованы новые рекомендации по ведению пациентов с варикоцеле. Подробнее >>
- Урология – это большой раздел медицины, который занимается патологией мочевыводящей системы. Подробнее >>
- Красное вино – новое оружие против рака предстательной железы. Подробнее >>
- О вреде курения много написано и сказано. Все курильщики знают о раке легких и прочих заболеваниях, но все равно продолжают курить.Подробнее >>
- Физические упражнения снижают у мужчин риск возникновения рака предстательной железы. Подробнее >>
Чтобы справиться с весенним авитаминозом, нужно принимать витамины.
В последние годы отмечается рост заболеваемости хроническими инфекционно–;воспалительными заболеваниями урогенитального тракта.
Почему некоторые лекарственные препараты по-разному действуют на мужчин и женщин ?
Симптомами уретрита является в первую очередь жжение, боль и резь при мочеиспускании, и выделения из уретры.
Инсульт нередко сопровождается урологическими осложнениями, характер которых зависит от места и степени повреждения головного мозга вследствие церебро–васкулярной болезни.

Гормонотерапия при раке простаты
Гормонотерапия при раке простаты
Более 12% всех злокачественных опухолевых заболеваний у мужчин занимает рак предстательной железы (РПЖ), а после 70 лет процент заболевших значительно увеличивается и в среднем составляет до 1400 случаев на 100000. В 1977 году профессор А. Shelly был удостоен Нобелевской премии за исследовательские работы пептидных гормонов, которые дали возможность разработать эффективную методику терапии агонистами ЛГРГ для медикаментозной кастрации. На сегодняшний день гормонотерапия при раке простаты считается главным методом лечения болезни, который позволяет увеличивать показатель выживаемости.

Принцип действия гормональной терапии
Перерождение обыкновенных клеток предстательной железы происходит под воздействием тестостерона – мужского полового гормона, синтезируемого особыми клетками семенников и корой надпочечников, это продукт периферического метаболизма. Конкретный механизм возникновения патологии до сих пор до конца не изучен, но уже имеющиеся знания дают возможность рекомендовать довольно эффективные протоколы лечения.

Гормонотерапия уменьшает количество тестостерона и блокирует его физиологическое воздействие на мужские органы. Врачи назначают прием гормонов на основании имеющихся анализов обследования больного и только после получения его согласия. Курс терапии должен выполнить несколько задач.
- Уменьшить размеры предстательной железы. В результате заболевания ее объем увеличивается в несколько раз, в случае радиотерапии приходится облучать большую площадь и захватывать здоровые ткани. Чем меньше опухоль – тем точнее можно сфокусировать ионизирующий луч, тем незначительнее негативные последствия лучевой терапии.
- Заметно уменьшить боли, минимизировать количество приема анестетиков. Многие из них имеют противопоказания, вызывают нежелательные сопутствующие реакции. Уменьшение и локализация боли значительно повышает качество жизни больного.
- Сократить скорость роста раковых клеток – продлить длительность жизни пациентов даже на последних стадиях развития болезни.
Если гормональная терапия при раке простаты у больных вызывает резистентность, то принимаются специальные индивидуальные мероприятия для ее предотвращения.
Исследованием новых методов терапии онкологических патологий занимается огромное количество научных сотрудников в развитых странах мира, в результате появляются новые более эффективные методики.
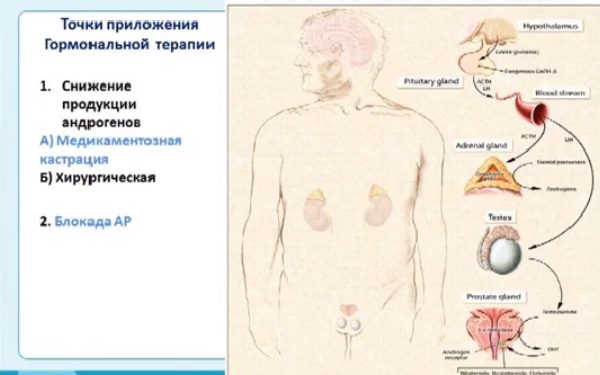
Используемые варианты гормональной терапии
Длительные наблюдения доказали эффективность андрогенной депривации примерно у 90% пациентов, в том числе и на поздних стадиях патологии. В последние несколько лет медики получили подтверждение эффективности и в качестве дополнения к лучевому или хирургическому методам лечения. Такие данные стали причиной интереса науки к интермиттирующей терапии – альтернативным протоколам гормональной терапии. Основными вариантами гормональной терапии являются следующие направления:
- монотерапия антиандрогенами, антиандрогены + ингибиторы;
- медикаментозная кастрация, Flare блокада + медикаментозная кастрация;
- интермиттирующая андрогенная депривация;
- альфаредуктазы, комбинированная андрогенная депривация;
- триплетная лекарственная терапия.
Таблица. Гормонотерапия при диссеминированном раке молочной железы: эффективность различных методов (неподобранные больные) [цит. по C. Henderson, 1991]
| Вид терапии | Число больных | Эффективность (%) |
| Антиэстрогены (тамоксифен)* | 1269 | 32 (16-52) |
| Овариэктомия** | 3380 | 33 (21-41) |
| Прогестины (МПА, мегестрол)* | 3479 | 31 (9-67) |
| Ингибиторы ароматазы (аминоглютетимид)* | 1153 | 32 (16-43) |
| LH-RH аналоги (золадекс)** | 293 | 40 (32-45) |
| Эстрогены* | 1683 | 26 (15-38) |
| Андрогены* | 2250 | 21 (10-38) |
| Адреналэктомия* | 3739 | 32 (23-46) |
| Гипофизэктомия | 1174 | 36 (22-58) |
Цель гормональной терапии состоит в том, чтобы положительно воздействовать на раковые клетки после хирургического вмешательства. Во всех случаях выживаемость после сложных хирургических вмешательств увеличилась с 62% до 71%.
Используемые типы гормонотерапии
Протоколы лечения допускают возможность использовать три вида терапии гормонами, окончательное решение принимается лечащим врачом на основании анализа состояния больного. Во время приема могут вноситься изменения с учетом реакции организма пациента.

Аналоги ЛГРГ
К ним относятся леупрорелина ацетат, трипторелин, гозерелин и бусерелин. Препараты подавляют продукцию тестостерона, не излечивают РПЖ, но заметно улучшают симптоматику и задерживают прогрессирование развития онкологических клеток. Гормональное лечение рака предстательной железы повышает качество жизни, врачи имеют время для использования полного комплекса существующих методик с целью минимизации последствий заболевания.
После первого приема препаратов агонисты провоцируют временный выброс ЛГ, что становится причиной увеличения плазменного уровня тестостерона (так называемый эффект вспышки). В клинических условиях такие ситуации предупреждаются путем назначения антиандрогенов. Через 3–4 недели наблюдается снижение чувствительности гипофиза больного, как следствие – уменьшение вырабатываемых гормонов тестостерона. Благоприятный профиль побочных эффектов позволяет рекомендовать прием препарата на различных стадиях заболевания.
Интермиттирующая гормональная терапия
ИГТ используется для задержки образования гормонорезистентных клеток РП, уменьшения риска появления негативных побочных явлений и понижения общей стоимости лечения. Гормональная терапия сопровождается до того времени, пока значение ПСА не опустится до исходного уровня. Затем прием препарата прекращается, а за больным выполняется постоянное наблюдение. Как только обнаружится повторное ухудшение состояния – прием препаратов возобновляется.
Используемые методы определения начала назначения агонистов ЛГРГ с учетом уровня тестостерона признаны безопасными, эффективными, дают возможность значительно уменьшить стоимость дальнейшего лечения.
Агонисты ЛГРГ в терапии распространенного рака

Таблица 2. Оптимальная последовательность различных методов гормонотерапии
| Линии гормональной терапия | Больные в репродуктивном
периоде и пременопаузе |
Больные в постменопаузе |
| I линия | Овариэктомия, лучевая кастрация или
агонисты рилизинг-гормонов (золадекс) |
Антиэстрогены (тамоксифен) |
| II линия | Антиэстрогены (тамоксифен) | Ингибиторы ароматазы |
| III линия | Ингибиторы ароматазы | Прогестины |
| IV линия | Прогестины | Эстрогены |
| V линия | Андрогены | Андрогены |
В зависимости от индивидуальных особенностей организма больного гормонотерапия при раке предстательной железы может вызывать те или иные побочные действия. Приливы наблюдаются у 50–70% пациентов, гинекомастия до 15%, тошнота и рвота у 0,13%, на импотенцию и снижение либидо жалуются до 100% больных. Серьезной проблемой для пациентов, длительное время принимающих препараты, является прогрессирующий остеопороз. Врачи должны внимательно наблюдать за ними и рекомендовать соответствующие поведение и лечебные препараты. Но во всех случаях эти симптомы нельзя считать критичными, по их показанием отменяется лечение лишь у 0–4% пациентов.
В зависимости от стадии развития болезни используется три протоколы гормонального лечения.
- Локализованная стадия. Для уменьшения объема железы, улучшения состояния здоровья больного перед хирургическим вмешательством и сужения поля облучения тканей при лучевой терапии назначается неоадъювантная гормонотерапия агонисты-ГнРГ ± антиандрогены. Такие же препараты рекомендовано принимать и при острой необходимости по клиническим показаниям отсрочить основное лечение. Продолжительность приема гормональных препаратов лечащий врач назначает индивидуально каждому пациенту на основании последних лабораторных анализов и с учетом его самочувствия.
- Распространенная стадия. Рекомендуется адъювантная гормонотерапия агонисты-ГнРГ ± антиандрогены одновременно с курсом лучевой терапии. Если уровень ПСА Вывод: Профилактика болезней во время гормонотерапии необходима
В результате приема гормональных препаратов повышаются риски заболевания диабетом и возникновения проблем с сердечно-сосудистой системой. Больному запрещается курение и употребление всех алкогольных напитков, рекомендуют препараты кальция и железа. Рекомендуется снизить вес до физиологической нормы, придерживаться сбалансированного здорового питания. Очень важную роль играют положительные эмоции, нацеленность на борьбу с болезнью. Если пациент не может самостоятельно управлять своим психическим состоянием, то надо обращаться врачам-психотерапевтам.
Текущий раздел: Урология
Интермиттирующая гормональная терапия рака предстательной железы
Павлов А.Ю., Гафанов Р.А.,Иванов С.А., Фастовец С.В., ФГУ “Российский научный центр рентгенорадиологии ” Минздравсоцразвития России, г. Москва
Статья опубликована 07 декабря 2010 года.
Идентификационный номер статьи в ФГУП НТЦ “ИНФОРМРЕГИСТР”: 0421000015\0046
Рабочий адрес: 117997, г . Москва, ул. Профсоюзная, д. 86
Павлов Андрей Юрьевич тел. (495)333-41-80 E-mail: pavlovdetur@mail.ru
Гафанов Рустем Айратович тел. (495)334-70-62 E — mail : docgra @ mail . ru
Фастовец Сергей Владимирович тел. (495)334-70-62 E-mail: sega14@mail.ru
Агонисты ЛГРГ доказали свою эффективность в лечении рака простаты. Хотя при гормональной терапии имеются побочные эффекты, большинство из них обратимы после прекращения терапии. За прошедшие годы интермитирующая гормонотерапия была оценена в нескольких клинических исследованиях II фазы. Эти испытания показали возможности интермитирующей гормонотерап ии и ее преимущество по показателям качества жизни и уменьшении побочных эффектов. Эти исследования подтвердили преимущество качества жизни у пациентов, получающих гормональную терапию в интермиттирующем режиме и низкое количество побочных явлений связанных с терапией. Однако , не было продемонстрировано, что интермитирующая гормонотерапия продлевает время до развития гормонорефрактерного рака простаты. Таким образом, необходима разработка руководства по использованию интермитирующей гормонотерапии в клинической практике, определяющие время для остановки и начала терапии, а также различные режимы терапии.
Ключевые слова: рак предстательной железы, интермитирующая гормональная терапия, максимальная андрогенная блокада.
Intermittent hormone therapy for prostate cancer.
Pavlov , Andrey Y ., Gafanov Rustem A ., Ivanov Sergey A ., Fastovets Sergey V .
Federal State Establishment “Russian Scientific Center of Roentgenoradiology of Russian Health and Social Development Ministry”, Moscow
LHRH agonists have proven effective in the treatment of prostate cancer.Although the hormone therapy has side effects, most of them are reversible after discontinuation of therapy. Over the years, intermittent hormone therapy has been evaluated in several clinical phase II trials. These tests showed the possibility of intermittent hormone therapy and its advantage on indicators of quality of life and reducing side effects. These studies confirmed the advantage of quality of life in patients receiving hormone replacement therapy in the intermittent mode and the low number of adverse events associated with therapy. However, it was demonstrated that intermittent hormonal therapy prolongs the time before the development of hormone-refractory prostate cancer. Thus, the need for guidance on the use of intermittent hormone therapy in clinical practice, determining the time to stop and start of therapy, as well as different modes of therapy.
Key words: prostate cancer, intermittent hormone therapy, maximum androgen blockade.
В настоящее время гормональная терапия (ГТ) используется в большинстве случаев для лечения пациентов раком предстательной железы (РПЖ). Эффективность гормонотерапии доказана, за что и была признана основным видом лечения рака простаты, в особенности с метастатическим поражением, на протяжении многих лет [1]. Цель ГТ у пациентов с метастатическим РПЖ состоит в том, чтобы уменьшить риск осложнений, распространения болезни, и по возможности улучшить показатель общей выживаемости [1]. ГТ также, все чаще проводится в более ранних стадиях РПЖ, к примеру, перед радикальной терапией у пациентов локализованным и местнораспространённым РПЖ, при биохимическом рецидиве (повышение уровня ПСА) после предшествующего радикального лечения. Однако , все еще остается неясным целесообразность и длительность ГТ в этих клинических случаях [1,2].
Общепринятым является проведение ГТ до развития прогрессирования болезни или смерти пациента. В результате чего, большинство пациентов, длительное время получают гормонотерапию, ценой которой могут стать побочные эффекты проводимого лечения. Первоначально проведение ГТ связано с развитием приливов, слабости, потери либидо, и усталостью 3. Более длительное использование ГТ может привести к деминерализации костей, анемии, уменьшению мышечной массы, нарушению жирового обмена — ожирению, изменению настроения и снижению конгестивной функции. Также может возрастать риск заболеваемости сердечно-сосудистой системы и смертность от неё 6. При долгосрочной терапии побочные эффекты возникают чаще, что оказывает отрицательное воздействие на качество жизни пациентов. Хотя у ГТ есть побочные эффекты, большинство из них обратимы после отмены терапии [5,9]. Другой аспект непрерывной ГТ — развитие гормональной резистентности . Было показано, что у большинства пациентов метастатическим РПЖ непрерывно получающих ГТ, гормональная резистентность рака простаты (ГРРП) развивалась в пределах 1,5-2,5 лет [9,10]. Кроме того, доклинические исследования показали, что возобновление антиандрогенной терапии усиливало процесс апоптоза андрогензависимых опухолевых клеток, которые выжили при Г T и задерживало развитие андрогенной резистентности 13. При интермиттирующей гормональной терапии (ИГТ) опухолей ( андрогензависимые карциномы и рак простаты) время до развития гормонорезистентности увеличивалось в 3 раза. Авторы заключили, что ИГТ может вызвать многократное снижение апоптоза в этих опухолях [11,14-16]. Преимущества и недостатки непрерывной Г T должны быть тщательно уравновешены и проанализированы. ИГТ исследуется как альтернатива непрерывной ГТ, с целью уменьшения побочных эффектов, для поддержания или улучшения качества жизни и продления периода до развития ГРРП. Кроме того, ИГ T дополнительно подразумевает сокращение затрат на лечение [3].
Интермиттирующая гормональная терапия, показания к назначению
ИГТ — циклическая терапия, состоящая из периодов лечения, сопровождаемых перерывами [3]. Период лечения цикла должен длиться до максимальной индукции гормонотерапевтического апоптоза и должен быть остановлен до периода перехода опухолевого процесса в стабильную фазу. Лечение длится от 6 до 9 месяцев, по некоторым данным от 2 до 3 месяцев. Некоторые авторы предлагают длительность лечения напрямую связывать с достижением низшей точки ПСА ( нг /мл).
Период без ГТ является переменным, и его продолжительность определяется уровнем ПСА пациента. Если повышение уровня ПСА наблюдается во время перерыва, начинают следующий цикл терапии. В настоящее время проводятся исследования для установки порогового уровня ПСА для повторной терапии, основанные на продолжающихся испытаниях 3 фазы клинических исследований. Так у пациентов с локализованными формами уровень ПСА составляет 6-15 нг /мл, тогда как у пациентов с метастатическим процессом пороговый уровень составляет 10-20 нг /мл. У пациентов с локализованными формами РПЖ с биохимическим рецидивом после радикальной простатэктомии или лучевой терапии пороговый уровень ПСА составляет более 3 нг /мл и более 6-10 нг /мл у пациентов с генерализованными формами РПЖ [3]. ИГТ можно назначать пациентам, которые отвечают на ГТ снижением уровня ПСА до нормальных значений [3]. У нелеченых пациентов нормальным значением считают уровень ПСА менее 4 нг /мл, для пациентов у которых был рецидив после радикальной простатэктомии или лучевой терапии порог уровня ПСА считается менее 0,5 нг /мл [3,9].
(анализ II фазы клинических исследований)
В мире проведено более 20 клинических исследований II фазы, которые включили в себя лечение около 2000 пациентов. В них оценивалась целесообразность, эффективность и безопасность ИГТ [3,9]. В эти исследования были рандомизированы пациенты с различными стадиями заболевания: пациенты с локализованными, местнораспространенными и генерализованными формами РПЖ, биохимическим рецидивом после радикальных методов лечения [3,9,17]. Большинство исследований, оценивающих ИГТ применяли максимальную андрогенную блокаду (МАБ) — комбинацию аналога лютеинизирующего гормона рилизинг гормона ЛГРГ и антиандрогена . Некоторые исследования использовали монотерапию аналогами ЛГРГ или монотерапию антиандрогенами . При метаанализе 10 испытаний II фазы, которые включили данные по 1446 пациентам, было установлено, что пациенты всех этих исследований в среднем около 39 % времени провели без терапии. Анализ показал, что инициальный уровень ПСА и низшая точка ПСА были важными прогностическими признаками клинического результата пациентов с РП, получающих ИГТ [17].
В целом, испытания II фазы продемонстрировали, что проведение ИГТ перспективно. Пациенты имели лучшие показатели качества жизни как во время периодов вне ГТ, так и во время ГТ. Кроме того, испытания II фазы показали, что ИГТ уменьшало общее количество побочных эффектов и осложнений, удлиняла период стабилизации и повышала показатели выживаемости. Однако , из-за того что эти исследования проводились в различных условиях, в небольших и гетерогенных популяциях, эти результаты должны быть подтверждены в хорошо разработанных клинических исследований III фазы. III фаза исследований должна дать ответ на основные вопросы об эффективности ИГТ: о влиянии на время до развития ГРРП и на общую выживаемость пациентов [3].
В настоящее время проходят несколько рандомизированных исследований III фазы по оценке ИГТ в Соединенных Штатах, Канаде, Японии, и Европе. Эти исследования проводятся пациентам с местнораспространенным или метастатическим P ПЖ и пациентам с рецидивом уровня ПСА после радикальной простатэктомии и лучевой терапии.
Таб. 1. Клинические исследования III фазы интермиттирующего ГТ при РП

