Предстательная железа представляет собой андрогензависимый непарный орган мужской репродуктивной системы. Функцией простаты является поддержание сперматогенеза в семенных канальцах яичек, обеспечение транспортировки сперматозоидов по семявыносящим протокам и эякуляции, а также формирование полового влечения.
Форма и размер. Простата имеет форму неправильного шара, напоминающую каштан, основание которого обращено вверх. Величина предстательной железы значительно варьируется в зависимости от возраста мужчины. Вертикальный размер простаты в среднем составляет 30 мм, фронтальный – 40 мм, сагиттальный – 20 мм. Масса железы у половозрелых мужчин до 30 лет составляет около 16 грамм. В норме простата имеет эластичную консистенцию.
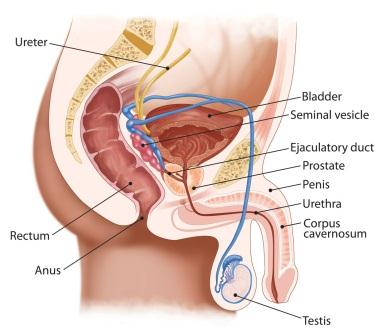
Расположение. Предстательная железа находится ниже мочевого пузыря между лобковым симфизом и прямой кишкой. Основание простаты, которое наклонено немного вперед и книзу, почти полностью сращено с дном мочевого пузыря. Задний отдел железы прикрыт семявыносящими протоками и семенными пузырьками. На границе между задней поверхностью органа и его основанием расположена фронтальная борозда. Через нее в простату входят два семявыносящих протока, которые открываются в просвет предстательной части уретры по бокам семенного бугорка. Снизу железа фиксирована волокнами переднего отдела мышечной ткани, поднимающей прямую кишку. Спереди простата соединяется с лобковым симфизом посредством лобково-предстательной связки.
Кровоснабжение. В предстательной железы расположены артерии, которые являются ответвлениями средних прямокишечных нижних пузырных кровеносных сосудов. Вокруг простаты расположено сплетение широких вен, которое связано с аналогичными сплетениями мочеиспускательного пузыря и концевого отдела кишечника.
Лимфооток. Лимфатические сосуды предстательной железы расположены вдоль семявыносящих протоков. Они проходят по боковым стенкам таза к внутренним и наружным подвздошным лимфатическим узлам, а также вдоль передней поверхности крестца по направлению к крестцовым лимфатическим узлам.
Иннервация. В предстательной железе расположены нервы, которые состоят из постганглионарных чувствительных парасимпатических и симпатических волокон. Нервы идут к простате от нижнего подчревного сплетения. На поверхности железы волокна образуют предстательное нервное сплетение.

Афала — новый подход к лечению заболеваний предстательной железы
Импаза — лекарственный препарат, который помогает устранить причину нарушения потенции (дисфункция эндотелия сосудов)
Импаза позволяет восстановить эректильную функцию мужчины в рамках физиологической нормы, в отличие от препаратов, обладающих лишь разовым стимулирующим эффектом.
Всё о простатите
Телефон горячей линии: +7 495 681-93-00
Предстательная железа (prostata) – непарный железисто-мышечный орган, состоящий из отдельных ацинусов, выделяющий вещества, являющиеся компонентом спермы. Предстательная железа имеет массу до 25 г и следующие размеры: толщину – до 2 см, поперечный размеры – до 4 см и продольный размеры – до 3 см.
Расположена железа в малом тазу под мочевым пузырем. Через простату проходит мочеиспускательный канал, входя в основание железы и выходя через ее верхушку. Простату прободают семявыносящие протоки.
В простате различают основание (basis prostatae), переднюю (facies anterior) и заднюю поверхности (facies posterior), нижнебоковые поверхности (facies inferlateralis) и верхушку предстательной железы (apex prostatae). От простаты идут связки – срединная и боковые лобково-предстательные связки (lig puboprostaticae) и лобково-предстательная мышца (m. Puboprostaticus), фиксирующие железу к лобковому симфизу.
Задняя поверхность простаты отделена от ампулы прямой кишки прямокишечно-пузырной пластинкой (septum rectovesicale).
Снаружи простата покрыта плотной капсулой, от которой внутрь железы отходят перегородки.
Простата имеет дольчатое строение, количество долек достигает 50. Дольки преимущественно располагаются в боковых и заднем отделах простаты. Железистые протоки ацинусов попарно сливаются и образуют предстательные протоки (duktuli prostaci), которые открываются в мочеиспускательный канал. В передней части простаты находится гладкая мышечная ткань, располагающаяся вокруг мочеиспускательного канала и участвующая в образовании непроизвольного сфинктера.
Кровоснабжение простаты осуществляется мелкими ветвями нижней мочепузырной и средней прямокишечной артерий. Венозный отток происходит в венозное сплетение простаты, из которого – во внутренние подвздошные вены.
Лимфатический отток осуществляется во внутренние подвздошные лимфатические узлы.
Иннервация осуществляется из простатического сплетения.
2. Строение, кровоснабжение и иннервация яичек и их придатков
Яичко (testis) является парной половой железой смешанной секреции; образует сперматозоиды и выделяет гормоны в кровь.
Яички расположены в мошонке. Яички разделены перегородкой, имеют овальную форму и гладкую поверхность. Масса яичка – около 25 г, размеры следующие: длина – 4 см, ширина – до 3 см, толщина – до 2 см. В яичке выделяют верхний и нижний концы (extremitas superior et inferior), два края – задний и передний, а также две стороны – медиальную и более выпуклую латеральную (facies medialis et lateralis). На верхнем конце можно обнаружить привесок яичка (appendix testis).
Яичко покрыто плотной белочной оболочкой (tunika albuginea), под которой расположена паренхима яичка (parenchyma testis).
Внутренняя поверхность белочной оболочки на задней стороне образует небольшой вырост – средостение яичка, от которого отходят тонкие соединительнотканные перегородочки (septula testis), делящие паренхиму яичка на дольки (lobuli testis), количество которых достигает около 300. Каждая долька имеет несколько извитых канальцев (tubuli seminiferi contorti), которые, сливаясь, образуют прямые канальцы (tubuli seminiferi recti). Прямые канальцы впадают в сеть яичка (rete testis), откуда выходит до 15 выносящих канальцев яичка (ductuli efferentes testis), впадающих в проток придатка яичка. Только в извитых канальцах образуются сперматозоиды, входящие в состав спермы, остальные канальцы являются семявыносящими.
Придаток яичка (epididymis) расположен по заднему краю яичка. В придатке различают головку (caput epididymidis), тело (corpus epididymidis) и хвост (cauda epididymidis). У детей имеется хорошо выраженный придаток привеска яичка (paradidymis), расположенный рядом с головкой придатка яичка. Белочная оболочка яичка переходит на придаток яичка. Выносящие канальцы яичка формируют конусы придатка яичка (coli epididymidis), которых насчитывается около 15—20.
Кровоснабжение осуществляется из яичковой артерии и артерии семявыносящего протока. Венозный отток идет в лозовидное венозное сплетение (plexus venosus pampiniformis).
Лимфатический отток происходит в поясничные лимфатические узлы.
Иннервация осуществляется из яичкового сплетения.
1. СТРОЕНИЕ, КРОВОСНАБЖЕНИЕ И ИННЕРВАЦИЯ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Предстательная железа (prostata) – непарный железисто-мышечный орган, состоящий из отдельных ацинусов, выделяющий вещества, являющиеся компонентом спермы. Предстательная железа имеет массу до 25 г и следующие размеры: толщину – до 2 см, поперечный размеры – до 4 см и продольный размеры – до 3 см.
Расположена железа в малом тазу под мочевым пузырем. Через простату проходит мочеиспускательный канал, входя в основание железы и выходя через ее верхушку. Простату прободают семявыносящие протоки.
В простате различают основание (basis prostatae), переднюю (facies anterior) и заднюю поверхности (facies posterior), нижнебоковые поверхности (facies inferlateralis) и верхушку предстательной железы (apex prostatae). От простаты идут связки – срединная и боковые лобково-предстательные связки (lig puboprostaticae) и лобково-предстательная мышца (m. Puboprostaticus), фиксирующие железу к лобковому симфизу.
Задняя поверхность простаты отделена от ампулы прямой кишки прямокишечно-пузырной пластинкой (septum rectovesicale).
Снаружи простата покрыта плотной капсулой, от которой внутрь железы отходят перегородки.
Простата имеет дольчатое строение, количество долек достигает 50. Дольки преимущественно располагаются в боковых и заднем отделах простаты. Железистые протоки ацинусов попарно сливаются и образуют предстательные протоки (duktuli prostaci), которые открываются в мочеиспускательный канал. В передней части простаты находится гладкая мышечная ткань, располагающаяся вокруг мочеиспускательного канала и участвующая в образовании непроизвольного сфинктера.
Кровоснабжение простаты осуществляется мелкими ветвями нижней мочепузырной и средней прямокишечной артерий. Венозный отток происходит в венозное сплетение простаты, из которого – во внутренние подвздошные вены.
Лимфатический отток осуществляется во внутренние подвздошные лимфатические узлы.
Иннервация осуществляется из простатического сплетения.
Данный текст является ознакомительным фрагментом.
Иннервация простаты осуществляется симпатическими, парасимпатическими и соматическими нервами. Симпатические нервы исходят из Th11—L2 и представляют собой верхнее гипогастральное сплетение, откуда нервные волокна направляются к нижнему гипогастральному сплетению.
Парасимпатическая иннервация осуществляется зоной S2—S4, которая формирует нижнее гипогастральное сплетение. Последнее содержит как парасимпатические, так и симпатические нервы и располагается сбоку и спереди от прямой кишки. Нейроваскулярный пучок локализуется постлатерально, у основания простаты, иннервируя фасции Денонвиллье и тазовую. Соматические нервы также исходят из S2-S4 и иннервируют поперечно-полосатую мускулатуру таза и уретрального сфинктера (рис. 13, 14).

Рис. 13. Пространственное изображение нейроанатомии таза, мочевого пузыря и предстательной железы (по A.Tewari et al., 2003)
Таким образом, строма и гладкая мускулатура простаты покрываются сетью холинергических и адренергических нервов. На границе между латеральной и задней поверхностями простаты перипростатическая фасция включает два-три нервных пучка, проходящих параллельно простате и заканчивающихся в кавернозных телах полового члена. Разветвленные верхние и нижние пучки нервов распространяются в латеральных отделах фасции Денонвиллье. Большая часть самой простаты иннервируется верхним нервным пучком, отдающим дорсолатерально три ветви в области основания простаты от сосудисто-нервного пучка.

Рис. 14. Половой нерв и его ветви, осуществляющие иннервацию полового члена и наружного сфинктера
Отдельные маленькие ветви обеспечивают иннервацией верхушку простаты. Автономные ганглии расположены непосредственно вблизи сосудисто-нервных пучков либо в перипростатической жировой ткани, где образуют цепочку на поверхности предстательной железы, проникают сквозь капсулу и заканчиваются в ее паренхиме.
Особого внимания заслуживают нейроваскулярные пучки, проходящие симметрично вдоль нижнебоковых поверхностей предстательной железы и тесно с ней связанные. Значение этих структурных образований важно в двух аспектах:
Гормональная регуляция роста и функции предстательной железы
Нормальная функция предстательной, равно как и других мужских половых желез, обеспечивается андрогенами яичкового и надпочечникового происхождения. Многогранность взаимодействия андрогенов с эпителием простаты, ее стромальным компонентом, нейроэндокринными клетками, одновременно циркулирующими другими гормонами (в частности эстрогенами), факторами роста представляет сложную систему, осуществляющую регуляцию как роста самой простаты, так и баланс относительного количества и функции эпителиальных и стромальных клеток. Однако этим не исчерпываются их взаимоотношения, поскольку оптимальный баланс возможен только при определенных соотношениях в продукции факторов роста.

Рис. 15. Схематическое изображение роли гипоталамо-гипофизарно-гонадной оси при росте простаты
Первый из них — лютеинизирующий — активизирует и стимулирует секрецию лютеинизирующего гормона передней доли гипофиза. Продукция тестостерона непосредственно происходит именно под воздействием лютеинизирующего гормона в яичках. Тестостерон, в свою очередь, также оказывает регулирующее действие на продукцию лютеинизирующего гормона путем отрицательного обратного воздействия на гипоталамус и гипофиз. Другой гормон гипофиза — фолликулостимулирующий — оказывает специфическое действие, стимулируя сперматогенез.
Рецепторы для этих гормонов найдены и в простате. Самостоятельная линия стимуляции мужского полового гормона осуществляется под влиянием адренокортикотропного гормона на синтез в надпочечниках андростендиона и дигидроэпиандрестерона, которые последовательно превращаются в тестостерон путем локальной и периферической конверсии. Более 95% циркулирующего тестостерона находится в крови либо с глобулином, связывающим половой гормон (секс-гормонсвязывающий глобулин), либо с альбумином. Только несвязанная фракция — около 3 % свободно циркулирующего тестостерона — может попасть в клетки мишени простаты путем диффузии, где и включается в разнообразные стероидные метаболические этапы, которые совершаются в ходе активной регуляции (J. Е. Damber et al., 1983).
Наиболее важный шаг — это конверсия в дигидротестостерон (ДГТ). Оба вида параллельных андрогенов (яичковые и надпочечниковые) проникают в цитоплазму клеток предстательной железы, где под воздействием 5а-редуктазы, ферментативной системы, локализованной на ядерной мембране, превращаются в дигидротестостерон, который соединяется со специфическими рецепторами, и образовавшийся комплекс проникает в ядро клетки, активизируя синтез ДНК (рис. 16). Дигидротестостерон, связанный с внутриклеточными андрогенорецепторами, приобретает выраженную активность, что способствует ядерному перемещению (транслокации) сформировавшегося стероид-рецепторного комплекса (W. I. Mainwaring, 1977). Последний контролирует регуляцию клеточного цикла, клеточный рост и дифференциацию.

Рис. 16. Тестостероновая поддержка функции простатических клеток и стимуляция клеточного роста
Рецептор человеческого андрогена — это 110 кДа-протеин, который расшифровывается однокопийным геном, расположенным на Х-хромосоме. Активированный стероид представляет собой рецепторный комплекс, который имеет домен (область) высокого сродства с избирательными хроматиновыми сайтами является модулятором генной экспрессии в клетках предстательной железы (W. Т. Schrader, 1984).
Предстательная железа находится не только под эндокринным контролем, гомеостаз органа поддерживается и другими регуляторными факторами. Существующие нейроэндокринные клетки по своей природе секреторные, могут оказывать аутокринно-паракринное действие. Это разновидность эпителиальных клеток простаты, которые могут взаимодействовать паракринным образом со стромой (G.Aumuller et al., 1999). Паракринная коммуникация по сути является локальной, ограниченной связью с рецепторами прилежащих клеток.
Аутокринные секреции стимулируют сами клетки, которые и секретируют их. В нормальных условиях аутокринные секреты не попадают в общую циркуляцию (P.A.Abrahamsson, 1999). Считается, что через разнообразные секреторные продукты они формируют коммуникационную сеть, участвующую в клеточной регуляции.
Важное значение имеет также выяснение роли андрогенов в реакциях роста, его факторах и рецепторах факторов, клеточных протоонкогенов. К настоящему времени накоплены убедительные доказательства, подтверждающие вовлечение тканевых факторов роста в процесс прогрессирования рака простаты (G.O.Hellawell, S.F.Brewster, 2002). Факторы роста регулируют развитие клеток, их дифференциацию и апоптоз (программированную клеточную смерть). Их семейство довольно многочисленно, а функциональное приложение разнообразно и нередко является прямо противоположным как в нормальной предстательной железе, так и при развивающемся в ней раке (табл.1).
Факторы роста действуют на прилежащие стромальные клетки паракринным образом и связаны с регуляцией эпителиальной пролиферации. Примером разнонаправленного действия факторов роста могут служить две группы. Так, группа факторов роста фибробластов (FGF), в которую входят инсулиновый фактор роста IGF, эпидермальный EGF и трансформирующий фактор роста TFG-а, а также факторы эндотелиального роста (фактор роста, извлеченный из тромбоцитов, — PDGF и фактор сосудисто-эндотелиального роста — VEGF), — главные стимулирующие регуляторы пролиферации в простате. Группа TGF-В является ведущим ингибитором пролиферации. Факторы роста оказывают аутокринный и паракриннный эффекты на стромальные и эпителиальные клетки, взаимодействуют с другими факторами и связующими протеинами для регуляции роста простаты (рис.17).

Рис. 17. Факторы роста и их рецепторы, вовлеченные в нормальное развитие простаты (по R. Byrne etal., 1996)
В. Djayan et al. (1999) показали, что высокий уровень инсулиноподобного фактора роста IGF-1 сочетается с большим риском развития рака простаты. Они подтвердили, что увеличение уровня IGF-1 на 7-8% отмечается у больных раком простаты. Хотя эти значения не зависят от уровня ПСА, вычисляемое отношение IGF-1/ПСА повышает специфичность установления рака предстательной железы, причем основным параметром является уменьшение соотношения.
Таблица 1. Факторы роста в нормальной простате и при раке (по G. О Hellawell и S.F.Brewster. 2002)

R. Kurek et al. (1998) относя IGF-1 к новым диагностическим параметрам, провели сравнительную оценку количественных показателей у пациентов с гиперплазией и раком предстательной железы. В первой группе среднее значение IGF-1 составило 62,5 мг/л, в то время как во второй оно было 110 мг/л. Наиболее высокие значения (до 350 мл/л) констатировались у больных раком простаты в стадии рТЗ с N+, МО. Авторы поддерживают тезис о каузальной связи между высоким содержанием IGF-1 в сыворотке крови и достоверностью рака простаты.
Механизм такой закономерности объясняется отчетливым пролиферативным влиянием IGF-1 на эпителиальные клетки. Интересен и лечебный подход основанный на тепловом воздействии, что вызывает уменьшение уровня IGF-1 и 60%-ную редукцию раковых клеток (W.E.Sonntagetal.,1999).
Нельзя не отметить и роль эстрогенов в процессах гормональной регуляции клеточных взаимоотношений предстательной железы. Концентрация плазматических эстрогенов у мужчин более низкая, чем тестостерона, значительная часть их аккумулируется в жировой ткани. Установлено, что 75-90% плазматических эстрогенов у молодых здоровых мужчин — это продукты периферического метаболизма (ароматизации) андростендиона и тестостерона в эстрон и эстрадиол. Суточная продукция эстрадиола у мужчин составляет 40мкг. Помимо периферического синтеза, источником секреции эстрогенов в мужском организме являются яички, что подтверждается признаками феминизации мужчин при опухолях клеток Сертоли и указывает на их участие в синтезе эстрогенов.
Взаимодействие двух гормонпродуцирующих клеток яичка — Лейдига и Сертоли — обеспечивает синтез эстрогенов, поскольку клетки Сертоли в противоположность клеткам Лейдига не утилизируют прегненолон как субстрат для ароматизации эстрогенов. У здоровых мужчин пожилого возраста и пациентов с аденомой предстательной железы происходят усиление секреции эстрогенов и параллельно морфо-функциональные изменения в клетках Сертоли, гистохимическая характеристика которых отражает их повышенную секреторную активность. Процесс протекает под контролем фолликулостимулирующего гормона (ФСГ), по отношению к которому клетки Сертоли являются мишенями, что подтверждается присутствием специфических ФСГ — рецепторов на мембранах клеток Сертоли.
Предполагается, что ФСГ регулирует синтез спектра стероидов, находящихся в канальцах, и путем изменения концентрации андрогенсвязывающих протеинов оказывает влияние на превращение тестостерона в эстрадиол. В связи с этим получила разработку концепция единой тестостерон-эстрогенной секреторной системы яичек, морфофункциональную основу которой составляют оба типа гормонпродуцирующих клеток яичка. Некоторые морфологические и функциональные изменения в предстательной железе удается наблюдать у орхиэктомированных лабораторных животных при введении им эстрогенных препаратов, что указывает на их чувствительность. Об этом же свидетельствует присутствие эстрогенных рецепторов в отдельных клеточных кланах с преобладанием в центральной части железы — так называемой мужской маточке.
У пожилых мужчин возрастает тестикулярная продукция эстрогенов. На фоне умеренного снижения уровня андрогенов в системной циркуляции это приводит к сдвигу андроген-эстрогенного баланса в сторону женских половых гормонов. При достаточной выраженности таких сдвигов они могут стать причиной возрастной склеротической атрофии предстательной железы.
В физиологических концентрациях эстрогены не оказывают непосредственного влияния на клетки рака предстательной железы. Первичное действие эстрогенов при лечении этого вида опухоли основано на их системном действии и заключается в подавлении эстрогенами синтеза и высвобождения ЛГРГ в гипоталамусе, что ведет к понижению секреции лютеинизирующего гормона (ЛГ) и, таким образом, к резкому уменьшению продукции тестостерона в яичках (A. A.Sandberg 1980). In vitro был продемонстрирован непосредственный ингибирующий эффект эстрогенов на высвобождение тестостерона из клеток Лейдига в яичках (L.Daehlin et al., 1985).
Последние, вероятно, необратимо повреждаются после долгосрочного лечения эстрогенами, что приводит к нарушению продукции тестостерона, которое продолжается и после отмены эстрогентерапии (R.Tomic et al., 1988). Оральные эстрогены вызывают повышение уровня глобулина, связывающего половой гормон в крови, что обусловливает снижение биологически активного свободного тестостерона в сыворотке крови (G.E.Damber et al., 1983). При этом проявляется эффект, сходный с действием максимальной андрогенной блокады. Эстрогены обладают также некоторым действием на адренальный стероидогенез, понижая уровни адренальных андрогенов предположительно путем изменения печеночной функции (R.Stege et al., 1988).
Кроме влияния тестостерона на простату, эстрогены и прогестины взаимодействуют также с этой железой. Эстрогены конкурируют за участки контакта с секс-глобулинсвязывающим гормоном, с которым тестостерон как доминантный стимул роста простаты, весьма активно связывается, хотя тестостерон проявляет благосклонность к этому протеину. Из-за их взаимодействий у мужчин в возрасте 50-60 лет констатируется 40%-ное повышение в соотношении свободного эстрадиола к свободному тестостерону. Основное влияние эстрогенов на предстательную железу может осуществляться через систему гипоталамус-гипофиз, которая является конечным органом, оказывающим подавляющее действие на тестикулярный синтез тестостерона.
В эксперименте показано, если эстрогены и тестостерон вводятся кастрированным животным одновременно, то у них происходит нормальный рост предстательной железы, а значит эстрогены не блокируют эффект замещения введенного тестостерона. Возможен и такой вариант: пролактины играют особую роль в росте и метаболизме предстательной железы. Рецепторы пролактина обнаружены в предстательной железе, яичках и могут выступать посредниками пролактина при поглощении тестостерона и метаболизме в простате.
В какой-то мере эффект воздействия эстрогенов подобен аналогам лютеинизирующего гормона рилизинг-гормона, хотя первые подавляют образование лютеинизирующего гормона, а вторые препятствуют его выделению. Тонкости этих процессов недостаточно выяснены, но зато четко обрисовывается токсичность эстрогенов с выраженным негативным эффектом для сердечно-сосудистой системы. Эстрогены могут также подавлять функцию клеток Лейдига. Эффект кастрации весьма существенен, поскольку приводит к резкому снижению уровня тестостерона плазмы, обычно от первоначального диапазона (500—600 нг/мл) до менее чем 50 нг/мл, что вызывает ощутимое подавление роста нормальной и раковой ткани простаты.
