Фотодинамическая терапия рака простаты

Есть определенные ограничения для активного наблюдения и эффективные методы лечения в Израиле локализованного рака простаты. Поскольку большинство случаев рака простаты имеют низкий риск и опухоль клинически локализована, многие мужчины сталкиваются с вопросом, как лучше управлять своим заболеванием.
Минимально инвазивный метод лечения рака простаты — сосудистая целевая фотодинамическая терапия может вылечить или контролировать болезнь, исключая риски более активного наблюдения, радикальной простатэктомии и лучевой терапии. Vascular Targeted Photodynamic Therapy WST-09 VTP представляет собой новую стратегию для достижения целей минимально инвазивного лечения рака предстательной железы — хороший прогноз и качество жизни пациента.
Сосудисто-целевая фотодинамическая терапия для пациентов с локализованным раком простаты — этот новая, минимально инвазивная процедура, которая, для того чтобы разрушить клетки рака простаты, посредством лазерного волокна использует активированный препарат. Технология имеет высокий потенциал уничтожить рак, не делая разрезы или причиняя любые разрушительные побочные эффекты сексуального, мочевого или репродуктивного характера. Эта процедура лечит только раковые части предстательной железы, подобно тому, как удаление опухоли может быть сделано для рака молочной железы.

Рекомендации по применению фотодинамической терапии определяются результатами биопсии и передовых методов визуализации. Некоторые пациенты выбирают активное наблюдение, также известное как бдительное ожидание. Но лучшую альтернативу предлагает целевая сосудистая фотодинамическая терапия локализованного рака простаты. Во время процедуры лазерные волокна расположены над предстательной железы, где были идентифицированы раковые клетки.
Пациенту внутривенно вводят фотосенсибилизирующий препарат под названием WST11, который циркулирует по всей крови в течение десяти минут. Затем лазерные волокна в области опухоли простаты активируют препарат светом конкретной длины волны в течение двадцати минут. Когда свет входит в контакт с препаратом, это разрушает кровеносные сосуды вокруг опухоли парализуя кровоснабжение рака. После лечения рака простаты пациенты проходят профилактическую диагностику в течение года: измеряется уровень PSA, проводится МРТ, а биопсия выполняется раз в шесть месяцев.
Фотодинамическая терапия представляет собой активацию светочувствительных соединений в тканях для получения желаемого терапевтического эффекта, в том числе апоптоза и некроза, а также является методом эффективно используют при различных доброкачественных и злокачественных условиях с целью абляции ткани.
Тукада ® WST-09 и растворимый Тукада WST-11, два производных бактериохлорофилла — фотосинтетический пигмент (Bchl), представлянт собой новое поколение фотосенсибилизаторов. Исследования механизма действия, оптимизация параметров лечения и ряд перспективно спланированных клинических процедур демонстрируют большие перспективы для этого класса терапевтических средств при лечении злокачественных опухолей человека.
Фотодинамическая терапия рака простаты
Фотодинамическая терапия (ФДТ) — новое направление в лечении опухолей различного генеза. Внутривенное или местное введение нетоксичных веществ, называемых фотосенсибилизаторами, и воздействие на пораженный орган светом определенной длины волны, вызывают гибель патологически измененных клеток в результате апоптоза или некроза ткани, вследствие прогрессирующего абактериального воспалительного процесса.
Фотодинамическая терапия может оказывать воздействие на ткань опухоли через фотосенсибилизатор двумя способами:
-
путем передачи электронов молекулам кислорода, с образованием OH, O2-, R+ и R — радикалов; путем передачи энергии с образованием молекулярного кислорода.
Эти короткоживущие продукты кислорода обладают цитотоксическим действием, приводящим к повреждению сосудов и клеток опухоли, особенно в случае гиперваскулярных новообразований. Таким образом, ФДТ вызывает преимущественное поражение железистой ткани предстательной железы, не оказывая существенного влияния на соединительную ткань органа.
Противоопухолевая эффективность ФДТ была продемонстрирована экспериментами на линиях злокачественных клеток in vitro, ксенотрансплантатах клеток рака простаты и in situ моделях in vivo. Эффективность и хорошая переносимость лечения, показанная на крупных животных (свиньи, обезьяны, собаки), позволила предложить метод для использования в клинике.
Методика ФДТ при РПЖ состоит из следующих этапов:
-
введение фотосенсибилизатора (минуты); его накопление в ткани-мишени (дни); облучение опухоли лазером через введенные трансперинеально в ткань предстательной железы оптоволоконные световоды (минуты).
Планирование ФДТ процедуры осуществляется с помощью специальной компьютерной системы, позволяющей на основе трехмерного моделирования оптимально разместить в ткани предстательной железы лазерные световоды, в зависимости от объема и конфигурации органа.
Фотодинамическая терапия при лечении рака простаты
Когда можно спать на стороне прооперированного глаза после операции катаракта
А. с. пушкин суровый был в науке славы ей дан учитель: не один урок нежданный и кровавый задал ей шведский паладин
Спондилеза шейного отдела позвоночника фото
Фотодинамическая терапия при лечении рака простаты


Фотодинамическая терапия – это современный подход в лечении онкологических заболеваний. Принцип данной терапии заключается в том, что источник света активирует локальное действие неактивного препарата. Данный препарат нетоксичен, вводят его внутривенно. Лазер с определенной длиной волны облучает область воздействия, при этом оказывая минимальное воздействие на окружающие ткани, и приводит к высвобождению реактивных кислородсодержащих веществ, из-за которых возникает некроз опухоли и повреждение клеток.

Бактерильно-хлорофильный препарат для фотодинамической терапии (ФДТ) рака простаты на основе растительного палладия называется Тукад. Его изобрел доктор Авигдор Шерц в Израиле в 1999 году. Производство данного препарата осуществляется STEBA BIOTECH NV во Франции. После внутривенного введения Тукада фотоактивацией, оптиковолоконным излучением происходит окислительное повреждение сосудов опухоли. Данные испытания были проведены на лабораторных животных и клеточных культурах. После ФДТ через 90 дней эффективность Tукада составляет 73% при подкожных опухолях у животных и 50% при костных опухолях.
На лабораторных собаках было продемонстрировано, что фотодинамическая терапия с Тукадом в терапевтических целях не вызывают функциональных или структурных нарушений прямой кишки и уретры.
На сегодняшний день ФДТ с Тукадом в основном применяют у пациентов с раком простаты, который прогрессирует, даже, несмотря на проведенную лучевую терапию. Скорее всего, в будущем будут расширены данные показания. Лишь после проведения клинических рандомизированных испытаний можно будет говорить о безопасности и эффективности ФДТ с Тукадом
С 2004 года началось клиническое испытание использования Тукада в лечении рака простаты в Великобритании, Канаде, Израиле, Франции и США. Вероятно, в будущем фотодинамичексая терапия станет главным методом в лечении пациентов с раком простаты.
Language





































Рак предстательной железы (РПЖ) сегодня в Российской Федерации относится к числу самых быстрорастущих злокачественных новообразований. С каждым годом растет число больных с локализованным РПЖ − в прошлом году их было 44% от числа всех пациентов с впервые выявленным диагнозом опухоли предста-
тельной железы (Чиссов В.И., 2010). К основным или стандартным методам лечения сегодня относятся радикальная простатэктомия (РПЭ), брахитерапия (БТ), дистанционная лучевая терапия (ДЛТ), гормональная терапия (ГТ). Известны как хорошие отдаленные результаты этих методов, так и те осложнения, которые имеет каждый из этих методов:
- возможные осложнения РПЭ: недержание мочи, импотенция, стриктуры уретры, тромбоэмболические осложнения, лимфостаз и др.;
- возможные осложнения ДЛТ: ректиты, циститы, энтероколиты, стриктуры, импотенция, недержание мочи и др.;
- возможные осложнения БТ: ирритативные симптомы, стриктуры уретры, кишечные симптомы, импотенция и др.;
- возможные осложнения ГТ: приливы, импотенция, гинекомастия, остеопороз, сахарный диабет, кардиоваскулярные, гастроинтестинальные осложнения и др.
Новые взгляды на лечение РПЖ
В связи с наличием осложнений лечения именно у больных локализованным РПЖ с низким риском прогрессирования достаточно популярна – пока не в России, а за рубежом – тактика отсроченного лечения или тщательного наблюдения. Отсроченное лечение (Wirth M. et al., 2010) возможно при:
- ПСА ≤ 10 нг/мл;
- показателе Глисона ≤ 6;
- сТ1с-Т2а;
- числе позитивных биоптатов ≤ 2;
- ≤ 50% опухоли в биопсийном столбике.
Однако, риск прогрессирования заболевания, который иногда сложно оценить, несмотря на существующие номограммы, таблицы и группы прогноза, и психологический дискомфорт пациента с установленным диагнозом, но не получающим лечения, серьезно затрудняют применение этого метода в клинической практике.
При проведении динамического наблюдения очень сложно определить момент, когда следует переключиться с активного наблюдения на активное лечение. Перед урологом встают трудные вопросы: надо ли учитывать период удвоения ПСА менее 3 лет, снижение степени дифференцировки, увеличение градации по Глисону более 6 при повторных биопсиях, появление симптоматики (Wirth M. et al., 2010). Не всем из этих больных можно в последующем применить радикальное лечение ввиду по- жилого возраста и наличия сопутствующих заболеваний. После применения методов радикального лечения (РПЭ и ДЛТ) у части больных может развиться местный рецидив заболевания.
По нашему мнению, именно в этих двух группах пациентов с локализованным процессом и низким риском прогрессирования, и у больных с местным рецидивом опухоли после радикального местного лечения, показаны методы фокальной (аблятивной) терапии.
Применение методов фокальной терапии обеспечивает и радикальное излечение, и минимизацию побочных эффектов, которыми характеризуются стандартные радикальные методики, а именно – РПЭ и лучевая терапия (Lecornet et al., 2010).
Фотодинамическая терапия рака предстательной железы
В основе метода фотодинамической терапии лежит применение фотосенсибилизаторов, с последующим проведением светового облучения ткани предстательной железы через оптические световоды. Под воздействием лазерного излучения фотосенсибилизатор, введенный в ткань предстательной железы, вызывает ряд реакций, которые ведут к активизации процесса перекисного окисления, что, в свою очередь, приводит к:
- прямому некрозу опухолевых клеток за счет высвобождения свободных радикалов кислорода;
- нарушению микроциркуляции в капиллярах и развитию ишемического некроза;
- развитию местного иммунного воспаления, которое также потенциально может приводить в последующем к эффекту абляции опухоли (Moore CM et al., 2008).
В таблице 1 приведено несколько клинических наблюдений по проведению фотодинамической терапии у больных РПЖ.
| Автор, год | Moore et al., 2006 |
Zaak et al., 2003 |
Pintus et al., Verigos et al., Patel et al., 2008 |
Weersink et al., 2005 Trachtenberg et al., 2008 Haider et al., 2007 |
|---|---|---|---|---|
| Препарат, доза |
Temoporfin (0,5 мг/кг,в/в) |
ALA-inducted protoporfirin IX (20 мг/кг, в/в) |
Motexafin- Lutetium (0,50 или 2,0 мг/кг, в/в) |
Padoporfin (0,10-2,0 мг/кг, в/в) |
| Время экспозиции ФС | 2-5 дней | 4 часа | 3,6 или 24 часа | 10 мин. |
| Зоны облучения | > 50% объема всей ПЖ | 50-100% объема ПЖ | Весь объем ПЖ | Весь объем ПЖ |
| Характеристика больных |
Глисон 3+3, ПСА 1,9-15 нг/мл, 6 больных – первичное лечение, 4 больных – повторное лечения | Глисон 5-8, уровень ПСА 4,9-10,6 нг/мл, первичные больные |
После ЛТ 8 больных ДЛТ, 9 больных – после брахитерапии | Рецидив после ДЛТ |
| Количество больных | 6 | 6 | 17 | 24 больных – с 2 волокнами 28 больных – до 6 волокон |
| Результат биопсии, ПСА |
Результат биопсии, ПСА |
До 51 см3 некроза Некроз и фиброз при биопсии Снижение ПСА в 8 из 10 лечений |
Некроз после РПЭ Снижение уровня ПСА до 55% | Негативная биопсия у 3 из 14 больных, снижение уровня ПСА после высоких доз ФДТ |
| Осложнения | Сепсис (n = 1) Дизурия (n =6) Недержание мочи (т = 1) Ухудшение эректильной функции (n = 1) |
Не было | Необходимость катетеризации (n = 14) Дизурия |
Ректоуретральный свищ (n = 2) Интраоперацион- ная гипотензия (n = 1) Дизурические явления до 6 месяцев (n = 10) |
Moore CM et al. (2008) Photodynamic therapy for prostate cancer—areview of current status and future promise
Первое поколение фотосенсибилизаторов отличалось длительным периодом экспозиции. Механизм действия второго поколения сенсибилизаторов, которые применяются в настоящее время, основан на сосудистых эффектах, поэтому время экспозиции исчисляется минутами. В разных исследованиях лазерному облучению подвергался различный объем (половина, вся железа, резидуальные ткани после ТУР) предстательной железы. Период наблюдения в этих работах очень небольшой, в основном, авторы исследовали токсичность данного метода, переносимость различных доз вводимых препаратов и доз мощности подводимого лазерного излучения.
Несмотря на то, что в некоторых публикациях осложнений вообще не наблюдалось (Zaak, 2003), у ряда авторов описаны достаточно серьезные осложнения, вплоть до развития ректоуретральных свищей, острой задержки мочеиспускания, и даже сепсиса (Weersink, 2005, Trachtenberg, 2008). Такие различия связаны с применением различных доз препаратов и мощности светового воздействия.
Собственный опыт
Методика фотодинамической терапии состоит во введении фотосенсибилизатора за несколько часов или за несколько минут досле операции. Интра — и послеоперационных осложнений зафиксировано не было. Дозы, которые мы использовали, пока еще, наверное, не достигли оптимальных значений.
Снижение уровня ПСА больше чем на 50% отмечено у 10 больных – по 5 в каждой группе при рецидивных опухолях и при перви чно выявленных. Средний уровень ПСА до начала лечения составлял 7,5 нг/мл, через шесть месяцев после фотодинамической терапии средний уровень был 3,4 нг/мл, через год – 3,1 нг/мл; медиана – чуть больше 2-х лет наблюдения.
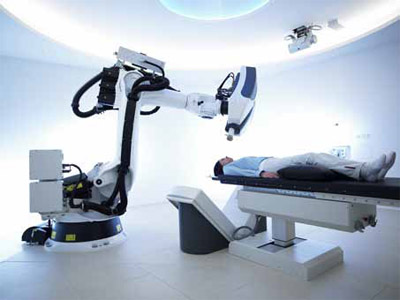
Рисунок 1. Кибер-нож
Ремиссия, которая определяется в виде отсутствия признаков как клинического, так и биохимического прогрессирования, наблюдалась у 37,5% больных. Биохимический рецидив или биохимическое прогрессирование диагностировано нами у 50% больных, но этих больных мы пока наблюдаем, т.к. скорость удвоения ПСА у них небольшая, имеется только биохимическое прогрессирование без развития клинического рецидива, и поэтому немедленную гормональную терапию мы пока не назначаем. Клинический рецидив, выявленный методами
лучевой диагностики, диагностирован только у 2-х пациентов. Один пациент умер от неопухолевой патологии.
Таким образом, сегодня фотодинамическая терапия является перспективным малоинвазивным методом лечения, который может быть проведен как у больных с низким риском прогрессирования, так и с местным рецидивом после лучевой терапии. Необходимы дальнейшие исследования токсичности и эффективности этой методики для более точного позиционирования ее в клинической практике.
Другие методы лечения РПЖ
Кибер-нож. Это высокоточная радиохирургическая система, которая представляет собой компактный линейный ускори-
тель с системой позиционирования и контроля изображения, что позволяет подводить более высокие дозы на минимальные объемы ткани. Сегодня этот аппарат используется, в основном, для лучевой терапии опухолей головного мозга – как первичных, так и метастатических (рисунок 1). Клинических данных по применению этого метода у больных РПЖ пока очень мало, они недостаточно изучены и отдаленные онкологические результаты отсутствуют.
Тем не менее, в 2011 г. опубликованы данные исследования, в
которое включены 67 больных локализованным РПЖ. При применении методики Кибер-ножа к опухоли подводилась большая доза излучения – пять фракций по 36 грей – всего 180 грей. Медиана наблюдения пока составляет 2,7 года – (King C., 2011). В конце 2,5-годичного периода наблюдения средний уровень ПСA составил всего лишь 0,5 нг/мл. Таким образом, безрецидивная выживаемость равнялась 94%.
Еще одна работа, с включением 55 больных локализованным РПЖ (Т1с-Т2с), касающаяся Кибер-ножа, была опубликована в 2011 г. (таблица 2).
Таблица 2. Распределение больных раком предстательной железы по стадии (ТNM), дифференцировки опухоли и степени прогноза
| Стадия | Т1с | Т2а-b | T2c |
|---|---|---|---|
| n | 23 (41,8%) | 17 (30,9%) | 15 (27,3%) |
| Глисон | 4-5 | 6 | 7 (3 + 4) |
| n | 4 (7,2%) | 44 (80%) | 7 (12,8%) |
| Группа риска (по D’Amico) | низкий | промежуточный | |
| n | 4 (7,2%) | 44 (80%) | |
Однако в данном исследовании токсичность второй степени встречалась чаще, а токсичность третьей степени (те реакции, которые заставляют прибегать к интервенции) наблюдалась реже.
Радиочастотная абляция (РЧА) – пока является экспери ментальным методом лечения РПЖ (рисунок 3). Мы рекомендуем его применение только в эксперименте и только в крупных центрах. В 2005 г. опубликовано исследование, в котором участвовали 11 больных, которым проводили РЧА предстательной железы трансперитонеально. Период наблюдения составил 20 месяцев. Были получены неплохие результаты – у 90% пациентов было отмечено снижение уровня PSA более чем на 50%. Более чем у 50% больных биопсия через 1 год показала отрицательные результаты.
Однако, были получены неудовлетворительные результаты по числу осложнений (Shariat S. et al., 2005), которые были обусловлены трудностями контроля температуры вне зоны воздействия. Сомнительные онкологические результаты, высокий риск осложнений сдерживают наше отношение
к этому методу у больных РПЖ, хотя, вероятно, его изучение продолжится.
Ключевые слова: рак предстательной железы, отсроченное лечение, ФДТ, Кибер-нож.
Keywords:prostate cancer, scrining of prostate cancer, prostatectomy, brachytherapy, delayed treatment, photodynamic therapy, CyberKnife.

-
Содержимое:
- Фотодинамическая терапия – что это
- Показания и противопоказания к ФДТ
- Как проводится ФДТ Тукад
- Где можно пройти курс терапии
- Результативность и отдаленный прогноз после ФДТ
Малоинвазивные методы терапии онкологии на ранней стадии заболевания показали себя наиболее эффективными способами лечения. Минимальный вред для организма сочетается с высокой результативностью.
Фотодинамическая терапия при раке простаты отличается избирательностью поражения тканей, возможностью, в случае необходимости, повторного проведения операции.
Фотодинамическая терапия – что это
Фотодинамический метод лечения рака простаты (Vascular Targeted Photodynamic Therapy), основан на способности организма накапливать фотосенсибилизаторы – вещества, которые при облучении провоцируют высвобождение синглентного кислорода.
Уничтожение злокачественных клеток осуществляется в несколько этапов:
- Введение фотосенсибилизаторов — вводятся через вену или инъекциями непосредственно в область предстательной железы. После накопления вещества переходят ко второму этапу лечения.
- Облучение — выполняется лазером или инфракрасным излучателем. Во время воздействия луча разного спектра интенсивности, фотосенсибилизаторы вступают в реакцию и наносят повреждения злокачественному образованию.
Эффективность метода во многом зависит от используемого вещества. Перед назначением фотодинамической терапии, лечащий врач выберет сенсибилизаторы по нескольким критериям:
- Избирательность в поражении раковых клеток.
- Токсичность и скорость выведения из организма.
- Накопление в коже и т.п.
Наибольшее распространение получило применение растительного палладия, более известного под названием: Tookad. Препарат был разработан израильскими учеными, ведущими исследователями проблем онкологии.
Были разработаны несколько версий фотосенсибилизаторов:
- WST-09.
- WST-11.
Между собой препараты отличаются интенсивностью воздействия и скоростью выведения из организма. Так, WST-11 можно облучать уже через 20 минут после введения, что снижает токсичность препарата для организма.
Растительный палладий относится к лекарственным средствам последнего поколения. Были снижены негативные последствия применения веществ, включая кожную сенсибилизацию.
Метод фотодинамической терапии при раке предстательной железы использует вещества, которые после преобразования отличаются токсичностью. Все противопоказания связаны с негативным действием препаратов.
Проведение ФДТ запрещается при наличии нескольких патологических процессов и заболеваний:
- Воспалительные процессы мочеполовой системы.
- Заболевания сердца.
- Патологические изменения печени.
- Аллергия на один из активных компонентов бактерильно-хлорофильного препарата.
Эффективность ФДТ была доказана для:
- Злокачественные образования не чувствительные к воздействию химиотерапии, облучению и приему гормональных средств.
- Рецидив ракового заболевания.
- Наличие метастазирования.
- Отказ пациента от хирургического иссечения опухоли.
ФДТ — это не исключительно израильский метод борьбы с онкологией. Хорошие результаты показали разработки российских специалистов.

Как проводится ФДТ Тукад
Принцип проведения фототерапии, независимо от места выполнения операции (зарубежные и отечественные клиники), идентичен. Отличаются только используемые для воздействия на раковые опухоли препараты. Методика не требует проведения наркоза, отсутствуют надрезы и постоперационные швы.
Отзывы больных показывают эффективность лечения. Результативность (до 70%) существенно улучшилась со времени изобретения сенсибилизаторов нового поколения. После проведения фототерапии, с целью предотвращения рецидива, пациент регулярно обследуется и сдает анализы на уровень ПСА.
Выбор клиники полностью зависит от предпочтений пациента и его финансовых возможностей. Фототерапия — метод с постоянно увеличивающейся популярностью.
В крупных онкологических клиниках России и Украины постоянно задумываются об открытии ФДТ отделений. В Израиле фотодинамическая терапия проводится практически в каждом медицинском центре.
Обратиться можно в следующие онкологические клиники:
- МЦ Tel Aviv CLINIC (Израиль) — прием проходит по адресу Тель-Авив, ул. Вайцман 14.
- МЦ Волшебный Луч (Россия) — клиника расположена в Москве, по ул. Талманской д1, корп.3.
- МЦ Ассута (Израиль) — клиника находится в городе Тель-Авив, ул. Ха-Берзель 20.
Стоимость лечения рака предстательной железы ФДТ в Израиле с полным обследованием организма обойдется в среднем от 25-30 000$. На цену терапии влияет выбранная клиника и используемые фотосенсибилизаторы.
Опыт применения фотодинамической терапии при лечении рака предстательной железы показал, что метод по своей эффективности превосходит облучение и прием гормональных препаратов, и приблизительно равен хирургическому удалению опухоли. При этом пациент быстрее восстанавливается и начинает вести полноценную жизнь.
Положительные результаты фотодинамической терапии наблюдаются у трех из четырех пациентов. Методика не ограничивается раковыми новообразованиями и может применяться даже после появления метастазирования.
Изобретение и последующее внедрение фотосенсибилизаторов Тукад в лечении рака простаты, было существенным прорывом и полностью изменило подход к онкологическим заболеваниям. Побочные эффекты были сведены к минимуму, а время госпитализации уменьшилось.
Первенство по количеству излечившихся пациентов занимают клиники Израиля, имеющие богатейший опыт помощи больным, в том числе на 3-4 стадии онкологии. В российских и украинских клиниках динамическая фототерапия не получила повсеместного применения.
