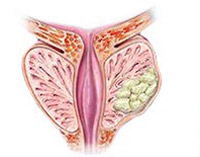
Хотя финастерид и дутастерид снижают общий риск развития рака простаты, они также увеличивают вероятность развития рака высокой степени злокачественности, что было опубликовано FDA (Федеральная служба по контролю над качеством пищевых продуктов и лекарств). Авторы добавляют, что, хотя риск невысокий, врачи должны знать о нем. В FDA указывают, что теперь в аннотациях всех препаратов данной группы в разделе Предостережения должна быть информация о риске развития рака простаты высокой степени злокачественности.
Препараты данного класса включают финастерид, дутастерид, туростерид и т.д. Они обладают антиандрогенной активностью и применяются для лечения аденомы простаты и андрогенной алопеции.
В FDA оценили два рандомизированных исследования – PCPT, в котором сравнивали финастерид по 5 мг на фоне плацебо в течение 7 лет, и REDUCE, в котором сравнивали дутастерид по 0,5 мг и плацебо в течение 4 лет. В обоих исследованиях показано снижение риска развития рака простаты у мужчин старше 50 лет, с одновременным повышением риска рака простаты высокой степени злокачественности. Данный тип рака простаты (сумма баллов по Глисону 8-10) вызывает наибольшую летальность, так как обладает агрессивным ростом и быстро прорастает капсулу простаты. Клетки рака большого размера, а сама опухоль плохо поддается лечению и часто рецидивирует. Другой особенностью рака высокой степени злокачественности является то, что его рецидив после лечения в некоторых случаях не сопровождается ростом уровня ПСА, что делает затруднительным его раннюю диагностику. В FDA подчеркивают, что врачи должны обсуждать с пациентами вопрос о смене или прекращении приема ингибиторов 5-а редуктазы.
Антиандрогены действуют локально в пределах простаты, блокируя ее рост дигидротестостероном. Антиандрогены весьма эффективны, но, к сожалению, их первичный механизм действия может самоограничиваться при блокировании действия андрогенов. Как класс лекарственных средств антиандрогены влияют на рецепторы андрогенов не только на уровне простаты, но и на уровне гипоталамо-гипофизарной системы. На этом уровне андрогены обычно испытывают саморегулирующее влияние отрицательной обратной связи. В результате центральной блокады рецепторов андрогенов секреция LH растет, а биосинтез тестостерона увеличивается.
Эстрогены, особенно диэтилстильбзстрол, блокируют выработку GnRH гипоталамусом, сокращая LH и FSH и уменьшая производство тестостерона. DES оказывает значительное токсическое воздействие на сердечно-сосудистую систему, вызывает эректильную дисфункцию и гинекомастию. В настоящее время DES больше не является препаратом первой линии при лечении рака предстательной железы.
Финастерид — конкурентный ингибитор 5а-редуктазы, фермента, катализирующего синтез DHT из тестостерона в простате (см. ранее). Препарат используют в лечении ДГПЖ, но его эффективность при раке предстательной железы остается спорной. Финастерид блокирует только 5а-редуктазу 2-го типа, но чтобы достичь максимальной клинической эффективности при раке предстательной железы и при ДГПЖ, необходимо блокировать обе изоформы. Дутастерид (препарат, способный ингибировать обе изоформы 5а-редуктазы) сейчас находится на стадии разработки.

В течение последнего десятилетия в лечении эректильной дисфункции был достигнут значительный прогресс в связи с появлением эффективных лекарственных средств. Эректильная дисфункция (половое бессилие) — неспособность достигать и/или поддерживать эрекцию, достаточную для удовлетворительного полового акта. Причинами эректильной дисфункции могут быть физиологические, неврогенные, эндокринные, сосудистые и травматические факторы. Эректильную дисфункцию подразделяют на психогенную, органическую или смешанную.
Потенциальные факторы риска развития этого нарушения: пожилой возраст, курение, гипертензия, ожирение, диабет, болезни сосудов, депрессия и применение некоторых лекарственных средств. Эректильная дисфункция может оказывать существенное влияние на качество жизни многих людей. Вероятность наличия той или иной формы эректильной дисфункции для людей старше 40 лет составляет около 55%.
При эрекции происходит расслабление гладких мышц кавернозных тел и наполнение их кровью, уровень эрекции определяется степенью кровенаполнения. Процесс эрекции — это сложный цикл взаимосвязанных сосудистых процессов, достигающих высшей точки при накоплении крови в половом члене под давлением, обеспечивающем его упругость. Эрекция может происходить только при расслаблении гладких мышц артерий и кавернозных тел и заполнении тканей кровью. Увеличение давления расширяет эластичные трабекулярные стенки. Артерии посредством вено-окклюзирующего механизма снижают венозный отток, что увеличивает давление и делает половой член твердым. Расслабление происходит после сокращения гладких мышц сосудов полового члена.
Эрекция зависит от местных сосудистых процессов, но регуляция реализуется через интеграцию нейрональных и гормональных механизмов на различных уровнях. Тонус гладких мышц кавернозных тел зависит от работы многих систем и проводящих путей, которые делятся на внешние (спинальные или супраспинальные проводящие пути классической нейротрансмиссии) и внутренние, определяемые пара- и аутокринными контролирующими системами с различными нейромодуляторными субстанциями.
Нормальная эрекция происходит, когда эти механизмы работают скоординированно. Эрекцию также обеспечивают симпатическая нервная система и NO-содержащие нервные волокна (система НАНХ), осуществляющие местную регуляцию. Однако для нормальной функции необходима регуляция и со стороны ЦНС.
Особенно интересна система НАНХ. При сексуальном возбуждении высвобождается NO, активизирующий внутриклеточный ферментный каскад. NO синтезируется из предшественника L-аргинина, который конвертируется ферментом NO-синтазой. В пределах кавернозного тела NO вызывает увеличение синтеза цГМФ, он, в свою очередь, уменьшает внутриклеточную концентрацию ионов кальция, что ведет к расслаблению гладких мышц сосудов и развитию эрекции. цГМФ разрушается ФДЭ-5, которая частично участвует в процессе расслабления (в этом процессе более значима роль СНС). Норадреналин вызывает сокращение гладких мышц кавернозного тела, что приводит к расслаблению.
Рак предстательной железы
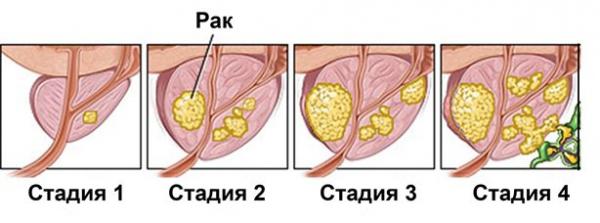
Рак предстательной железы (РПЖ) в РФ составил в 2011 г. – 11,9% (второе место после рака легкого), прирост в год – 8%, 4 место в структуре онкологической смертности – умерло 10 555 больных РПЖ в США с 2007 г. РПЖ – стоит на первом месте.
РПЖ более чем в 80% случаев развивается на фоне доброкачественной гиперплазии предстательной железы (ДГПЖ). В 3% случаев РПЖ находят при операции ДГПЖ. В то же время установлено, что ДГПЖ не повышает риск РПЖ.
Диагностика РПЖ – значение ПСА
ПСА – простат — специфический антиген – секретируется простатой, протеаза.
- 40% с нормальным уровнем ПСА (
- 65% лиц с повышенным уровнем ПСА – не имеют РПЖ, а страдают другими заболеваниями ПЖ.
- 35-45% пациентов с уровнем ПСА > 10 нг/мл – имеют отрицательный баланс биопсии ПЖ.
Известно более 220 биохимических маркёров РПЖ (Аннексии III, РСА 3, про ПСА и др.). В настоящее время достоверного метода серологической диагностики РПЖ – НЕТ.
Факторы риска РПЖ
Возраст: частота РПЖ увеличивается с возрастом на 15-20 лет позже ДГПЖ.
Раса: у мужчин черной расы больше объем простаты и выше риск ДГПЖ и РПЖ.
Генетика: известны специфические мутации, связанные с риском РПЖ.
Питание:
- Ожирение, избыточное потребление жира, насыщенных жирных кислот, мяса, молока, кальция, дефицит овощей и фруктов.
- Продукты животноводства и глюкоза. Потребление мяса вызывает экспрессию ИФР (инсулиноподобного фактора роста).
- Избыточное потребление углеводов вызывает увеличение секреции инсулина, который стимулирует пролиферативную активность клеток предстательной железы.
- Андрогены – высокий уровень тестостерона.
- Линолевая омега-6 ПНЖК.
- Витамин D. Увеличивает риск РПЖ: низкий ( 80 нмоль/л) уровень витамина D в крови.
- Курение – повышает риск ДГПЖ и смертность от РПЖ.
Рак простаты: что делать?
Лекарственные препараты
Торможение образования 5 а–дигидротестостерона (ДТС) из тестостерона (ТС)
Ингибиторы 5а-редуктазы – блокируют фермент I типа – дугастерид, II типа – финастерид.
Результаты применения ингибиторов
- Снижают содержание ДТС, активируют апоптоз в простате, уменьшают ее объем.
- Снижают задержку мочи на 57-59%, уменьшают прогрессирование ДГПЖ.
- Финастерид снижал риск РПЖ на 25%.
- Финастерид предупреждал индуцированный РПЖ у крыс.
- Дугастерид в исследовании REDUCE вызывал регресс ДГПЖ и снижал риск РПЖ.
Побочные эффекты: эректильная дисфункция, увеличение ЛГ (лютинезирующих гормонов), гинекомастия.
АЛЬФА-АДРЕНОБЛОКАТОРЫ блокируют адренорецепторы простаты, что расслабляет мышцы и уменьшают обструкцию (закупорку каналов) – феноксибензамин , альфузозин , доксозазин , индорамин .
АЛЬФА-АДРЕНОБЛОКАТОРЫ оказывают симптоматическое действие.
- тамсулозин снижал частоту предраковых изменений.
Эффективно совместное применение ингибиторов 5а-редуктазы и а-адреноблокаторов.
Фитопрепараты и БАДы
Наиболее изучены экстракты плодов Serenoa repens (сереноа) Со Пальметто и Pygeum africanum (пиджеум) – Африканская слива . Данные препараты продемонстрировали эффективность, аналогичные ингибиторам 5а-редуктазы и а1 – адреноблокаторам.
- Экстракт сереноа и экстракт пиджеум предупреждали развитие РПЖ у тирансгенных мышей TRAMP.
- Экстракт сереноа снижал частоту предраковых изменений в предстательной железе, индуцированную фенилэфрином у крыс.
- В обзоре 18 рандомизированных исследований установлено, что экстракт сереноа улучшал мочевую и эректильную функцию.
- Назначение 320 мг экстракта экстракт сереноа в течение 6 месяцев достоверно улучшал функцию мочеотделения и показатели теста IPPS (состояние предстательной железы).
- Назначение 320 мг экстракта экстракт сереноа в течение 3 месяцев достоверно улучшал скорость мочеиспускания, индекс теста IPPS, уменьшался размер простаты.

Ликопин оказывает лечебное действие на ДГПЖ в экспериментальных и клинических исследованиях.
- Ликопин ( содержится в красных овощах, фруктах ) снижал уровень ПСА и патологическую симптоматику ДГПЖ, тормозил увеличение простаты.
- У мужчин, потребляющих ежедневно томатный сок или соус (ликопин), риск РПЖ снижается на 50%.
Полифенолы
- Апигенин (сельдерей, петрушка, орехи, фрукты), гинестеин (соя) – оказывали лечебное действие на ДГПЖ в клинике и в эксперименте.
- Апигенин тормозит канцерогенез простаты у трангенных мышей.
- Изофлавоны сои (60-900 мг) снижали уровень ПСА у больных РПЖ.
- Гинестеин предупреждал развитие РПЖ у трансгенных крыс.
- Смесь изофлавонов сои (гинестеин и дайджеин) предупреждали РПЖ, индуцированный тестостероном у крыс.


