К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2].
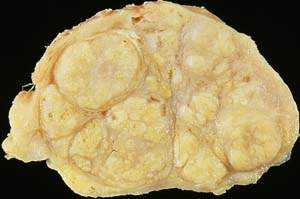 |
| Рисунок 1. Доброкачественная гиперплазия предстательной железы (макропрепарат) |
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2]. Около 80% мужчин старше 80 лет страдают этим заболеванием. Другая статистика свидетельствует, что из всех заболеваний, которым подвержены мужчины старше 50 лет, на долю доброкачественной гиперплазии простаты приходится 36% [1]. Эти сведения настолько общеизвестны, что ухудшение качества мочеиспускания часто рассматривается как естественное явление.
Клинически данное заболевание проявляется различными симптомами, связанными с нарушением пассажа мочи по нижним мочевым путям. При значительно выраженной инфравезикальной обструкции, как правило, прибегают к хирургическому вмешательству. Оперативное лечение по поводу ДГПЖ показано 30% больных в возрасте от 50 до 80 лет [4]. Однако в последние годы все большую популярность завоевывает медикаментозная терапия доброкачественной гиперплазии предстательной железы. Это, с одной стороны, объясняется вполне логичным желанием врача и пациента по возможности избежать операции, с другой — развитием представлений о патогенезе расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы.
До недавнего времени патогенез расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы рассматривали с позиции классических представлений о механической инфравезикальной обструкции и развитии вторичных структурно-функциональных изменений детрузора (компенсация, декомпенсация). За последние два десятилетия получены принципиально новые данные о природе повышенного внутриуретрального сопротивления. Его перестали отождествлять исключительно с механическим сдавлением шейки мочевого пузыря и задней уретры. Обнаружен динамический компонент обструкции, который состоит в повышении тонуса указанных анатомических структур за счет активности a-адренорецепторов. Появились также иные трактовки происхождения ирритативных симптомов. Их считают проявлением первичного нестабильного мочевого пузыря и не связывают напрямую с обструкцией [5].
Результаты нашей работы свидетельствуют, что при ДГПЖ клиническая симптоматика развивается вследствие недостаточности энергетического метаболизма и гипоксии детрузора в условиях повышенного уретрального сопротивления [3]. Об этом свидетельствуют:
- уменьшение артерио-венозной разности парциального напряжения кислорода и метаболический ацидоз;
- снижение активности ферментов в ткани детрузора, участвующих в ключевых реакциях аэробного окисления;
- повышение активности гликолитических ферментов и ферментов пентозофосфатного шунта, свидетельствующих о преобладании в детрузоре гликолиза;
- ферментативная недостаточность, в том числе энергетического метаболизма, обусловленная как минимум гиповитаминозом В6;
- достоверная положительная динамика основных функций мочевого пузыря под влиянием гипербарической оксигенации.
Причины нарушений энергетического метаболизма и функций детрузора крайне многообразны. В частности, к таким нарушениям могут привести повышение активности симпатической нервной системы, расстройства органного кровообращения, авитаминоз (группа В), хронические заболевания дыхательной и сердечно-сосудистой систем, влияние приема ряда фармакологических препаратов, угнетающих дыхательную цепь, и, естественно, обструктивные нарушения уродинамики и т. д. Весьма важно, что нарушения гипоксического характера в гладкомышечной ткани могут иметь и первичный митохондриальный генез (первичные нарушения энергетического метаболизма детрузора [3].
Необходимо отметить, что у больных ДГПЖ в нижнем отделе мочевого тракта протекают два параллельных процесса — формирование уретральной обструкции и нарушение энергетического метаболизма детрузора (митохондриальная недостаточность).
Подобное представление патогенеза расстройств мочеиспускания открывает широкие возможности для фармакотерапии. Сокращения и расслабления детрузора можно достичь с помощью средств метаболической терапии, прямого улучшения снабжения детрузора кислородом и т. д. Наиболее значимые расстройства основных функций мочевого пузыря все же опосредованы расстройствами кровообращения. И если процесс обратим, то до или после хирургического вмешательства можно существенно влиять на функциональное состояние мочевого пузыря с помощью вазоактивных препаратов, к которым в первую очередь относятся a1-адреноблокаторы.
При определении критериев отбора пациентов для медикаментозной терапии ДГПЖ мы воспользовались рекомендациями IV Международного консультативного комитета по ДГПЖ.
Основу настоящего исследования составили собственные клинические наблюдения за 1724 пациентами (средний возраст 61,4 года), страдающими ДГПЖ и получавшими различные варианты медикаментозного лечения. Нами применялись препараты всех групп, использующихся в настоящее время для лечения ДГПЖ: a-адреноблокаторы, блокаторы 5-a-редуктазы, препараты растительного происхождения и их комбинации. Схемы проведенного лечения и характеристика групп пациентов приведены в табл. 1.
Из наиболее многочисленной и популярной сегодня группы препаратов для медикаментозного лечения ДГПЖ — селективных a-адреноблокаторов мы использовали альфузозин, теразозин, доксазозин и тамсулозин. Общее число пациентов, получавших a-адреноблокаторы, составило 1408. Финастерид был взят нами как классический представитель блокаторов 5-a-редуктазы. Из препаратов растительного происхождения мы использовали пермиксон и таденан.
В пяти группах общей численностью 1305 человек проводилась терапия селективными a-адреноблокаторами в течение длительного периода времени по стандартным схемам и в стандартных дозах. Результаты лечения приведены в табл. 2.
Улучшение качества мочеиспускания отметили в среднем 86,74% пациентов. Суммарный балл I-PSS сократился на 38,68% к окончанию первого года лечения и на 43,4% к окончанию курса терапии. Балл QOL уменьшился на 29,04% и 35,58% соответственно. Максимальная скорость потока мочи увеличилась на 45,25% к окончанию первого года лечения и стабилизировалась на достигнутом уровне. Количество остаточной мочи сократилось в среднем на 57,6%. Процент пациентов, по тем или иным причинам выбывших из исследования, был тождествен во всех группах и равнялся 14,38%.
Особо следует остановиться на препарате тамсулозин (омник, Yamanouchi) — пока единственном простатселективном a1А-адреноблокаторе на отечественном рынке. Этот препарат обладает рядом свойств, которые позволяют его использовать в различных функциональных тестах. Прежде всего это возможность назначения единой терапевтической дозы (один раз в сутки по 0,4 мг). А отсутствие выраженного влияния на артериальное давление и сердечную деятельность избавляет от необходимости титрования дозы. Мы согласны с рядом авторов, которые считают возможным применение коротких курсов терапии тамсулозином в качестве прогностических тестов эффективности лечения a1-адреноблокаторами, что может иметь решающее значение при выборе того или иного метода медикаментозного лечения ДГПЖ [4].
Части больных (группа А5) проведена проверка возможности разрешения острой задержки мочеиспускания (ОЗМ) приемом альфузозина по 5 мг два раза в сутки. Эта терапия проводилась пациентам с впервые возникшей ОЗМ и отсутствием симптомов нарушения мочеиспускания в анамнезе. Положительный эффект был достигнут у 8 из 14 пациентов (57,1%), которым параллельно приему альфузозина производилось кратковременное (трое суток) дренирование мочевого пузыря катетером. Единовременный прием суточной дозы альфузозина (10 мг) способствовал восстановлению самостоятельного мочеиспускания лишь у одного из четырех пациентов, которым проводилась подобная терапия. Вероятно, это объясняется гипотонией детрузора, усугубляющейся в ситуации длительного перерастяжения мочевого пузыря на фоне задержки мочеиспускания.
Для изучения эффективности и безопасности комбинированной медикаментозной терапии ДГПЖ препаратами разных групп, а также для уточнения целесообразности проведения терапии нами были созданы три группы.
В первой группе (К1) пациенты получали проскар по 5 мг/сут. параллельно с приемом теразозина по 5-10 мг/сут. Обращало на себя внимание значительное повышение показателей максимальной скорости потока мочи (+40%), характерное для группы монотерапии a-адреноблокаторами, и постепенное, на протяжении курса лечения, снижение объема предстательной железы (-20,4%), характерное для группы монотерапии финастеридом. Очевидно, что положительные изменения показателей мочеиспускания в этой группе являются следствием воздействия обоих препаратов. Тем не менее процент выбывших пациентов в этой группе был крайне высоким — 32,3%. Основной причиной прекращения комбинированной терапии ДГПЖ пациенты называли неприемлемо высокую стоимость лечения.
Во второй группе (К2) мы произвели попытку снизить стоимость лечения. Первый год терапия проводилась по той же схеме, что и в группе К1. У 10 пациентов (83,3%), у которых была отмечена значительная регрессия обструктивной симптоматики (повышение Qmax более чем на 25%), после года комбинированной терапии мы отменили теразозин и продолжили монотерапию финастеридом. При сравнении эффективности терапии в первой и второй группах обращает на себя внимание тождественность результатов в течение первого года лечения. В последующие два года объем остаточной мочи и максимальная скорость потока мочи претерпевают более заметные положительные изменения в группе К1, чем в группе К2 (-36,8% против -24,7% и +40% против +27,3% соответственно). В целом, оценивая результаты лечения пациентов в группе К2, можно отметить явно выраженные положительные изменения качества мочеиспускания при более низкой стоимости лечения по сравнению с группой К1.
В третьей группе комбинированной терапии (К3) лечение проводилось финастеридом по 5 мг/сут. в сочетании с пермиксоном по 160 мг два раза в сутки. Через два года после начала лечения 50% пациентов покинули группу, приводя причиной отказа от дальнейшей терапии высокую стоимость лечения при отсутствии быстрого улучшения качества мочеиспускания. При сравнении полученных данных с результатами в других группах очевидно, что эффективность лечения в третьей существенно ниже.
Таким образом, эффективность медикаментозной терапии больных ДГПЖ при соблюдении показаний и противопоказаний к ее назначению, правильном выборе препарата и схемы его назначения высока и достигает в среднем 80,2%. При этом эффективность монотерапии a-адреноблокаторами составляет 86,7%, блокаторами 5a-редуктазы — 69,4%, препаратами растительного происхождения — 69,3% и при комбинированной терапии — 95,45%. Комбинированная медикаментозная терапия a-адреноблокаторами в сочетании с блокаторами 5a-редуктазы эффективнее монотерапии этими препаратами. С целью снижения стоимости лечения возможен переход на монотерапию блокаторами 5a-редуктазы после достижения выраженного регресса обструктивной симптоматики. Медикаментозная терапия a-адреноблокаторами является эффективным способом консервативного лечения острой задержки мочеиспускания. Терапия должна проводиться на фоне кратковременного (трое суток) дренирования мочевого пузыря уретральным катетером.
1. Гориловский Л. М. Эпидемиология и факторы риска развития доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 10-18.
2. Лопаткин Н. А., Перепанова Т. С. Клинический опыт лечения больных доброкачественной гиперплазией предстательной железы a1-адреноблокатором альфузозином // Урол. и нефрол., 1997, № 5, с. 14-17.
3. Лоран О. Б., Вишневский Е. Л., Вишневский А. Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты a-адреноблокаторами. Монография. М., 1998.
4. Сивков А. В. Медикаментозная терапия доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 67-83.
5. McConnell J. D. Prostatic growth: new insights into hormonal regulation // Br. J. Urol. 1995. Vol.76.(suppl.1). P. 5-10.
О причинах возникновения аденомы простаты медики спорят до сих пор. В качестве предпосылок к тому, что в предстательной железе образуются узелки, которые затем давят на мочеиспускательный канал, называют снижение уровня тестостерона, воспалительные процессы в мочеполовых путях и почках, малоподвижный образ жизни, наследственность, изменение ритма интимной жизни, травмы половых органов и другие. Определить, что именно стало причиной опухоли предстательной железы, может только уролог. В зависимости от поставленного диагноза врач также определит схему лечения. И, вопреки расхожему мнению, речь, скорее всего, пойдет не о хирургическом вмешательстве.
Как лечить аденому предстательной железы без операции
Чтобы подтвердить первичный диагноз и назначить лечение, необходим целый спектр исследований: анализы крови и мочи, ректальное обследование, УЗИ, при необходимости — рентген таза. Если заболевание обнаружено на ранней стадии, может быть достаточно медикаментозного лечения.
Медикаментозное лечение аденомы простаты
Безусловно, лечение аденомы простаты без хирургического вмешательства является более щадящим, однако самостоятельно подобранные препараты могут не только не улучшить состояние здоровья, но в некоторых случаях даже ухудшить его. Выбирать пероральные лекарства (таблетки, микстуры) или ректальные (свечи) должен только уролог.
Как правило, вышеописанные препараты принимаются комплексно, врач подбирает их индивидуально для пациента, однако многое зависит и от самого мужчины, в частности от того, насколько аккуратно он будет соблюдать график приема выписанных ему лекарств.
В некоторых случаях — и только тогда, когда аденома простаты находится в первой, или начальной, стадии, — уролог может предложить пациенту воспользоваться препаратами с действующим веществом природного происхождения (БАДами).
Фотодинамическая терапия
Лечение, при котором в организм пациента вводятся фотосенсибилизаторы. Помогает бороться с несколькими проблемами в организме: тканевыми патологиями, воспалениями, а также злокачественными и доброкачественными опухолями, в том числе с аденомой простаты.
Озонотерапия
Основой данной терапии являются свойства озона. Активный кислород в составе последнего помогает наладить микроциркуляцию витаминов и минеральных веществ в клетках, а также улучшает обмен веществ. Озон также имеет хорошие дезинфицирующие свойства, процедура практически лишена побочных эффектов, сочетается с физиотерапией и лечением медикаментами.
Физиотерапия
Физиотерапия используется либо на самых ранних стадиях заболевания, либо для предотвращения рецидивов и осложнений после лечения. Физиопроцедуры в лечении аденомы простаты подразделяются на два вида:
- первый, в который входят магнито-, лазеро- и индуктотерапия, помогает активировать кровоток и стимулировать защитные силы организма;
- второй, включающий в себя криотерапию, термоабляцию, трансуретральную игольную абляцию и трансуретральную микроволновую термотерапию, локально борется с воспалением простаты, устраняя симптомы и не допуская регресса.
Диетотерапия
Даже самые современные терапевтические средства окажут лишь временный эффект без помощи со стороны самого пациента. Ему необходимо будет придерживаться диеты, которую подберет и назначит врач. Аденома простаты — это доброкачественная опухоль, влияющая на процесс мочеиспускания. Для того чтобы не допустить увеличения железы в размерах, нужно соблюдать основные принципы питания: рацион должен быть легким и сбалансированным, чтобы не спровоцировать набор веса, обеспечивать организм необходимыми витаминами и микроэлементами, ограничивать количество потребляемой жидкости и не вызывать запоров.
ЛФК
В лечении аденомы предстательной железы лечебная физкультура (ЛФК) занимает особое место. Ее назначают как на ранних стадиях заболевания, так и после оперативного вмешательства — в качестве реабилитации пациента.
Пересмотр образа жизни
Изменение образа жизни само по себе не является терапевтической мерой, однако помогает не допускать усиления симптомов заболевания. Так, пациентам рекомендуется:
- избегать переохлаждения;
- уменьшить прием жидкости за два часа до сна;
- сократить употребление кофе и алкоголя, мочегонных, антигистаминных и противоотечных средств;
- добавить ежедневные физические упражнения.
Народные средства
Фитотерапия является альтернативным вариантом лечения аденомы простаты, но по большому счету отвечает и за профилактику заболевания. Пациентам предлагается принимать, например, настой луковой шелухи, смешанной с медом, или семена тыквы, смешанные с медом и грецким орехом, — эти народные средства помогают нормализовать работу мочевыводящих путей.
Существует несколько способов малоинвазивного вмешательства в организм при аденоме предстательной железы.
Трансуретральная резекция (ТУР)
Наиболее распространенная операция, равноценная по результатам хирургическому вмешательству или аденомэктомии. Однако она имеет ряд ограничений. Аденома не должна превышать в объеме 60 мл, а количество остаточной мочи — 150 мл. Кроме того, ТУР нельзя применять в случае, если пациент страдает от почечной недостаточности.
Во время этой операции части простаты, выступающие в уретру, удаляются введенным трансуретральным методом резектоскопом (эндоскоп диаметром не более одного см, оснащенный камерой, источником освещения, электрической петлей для удаления опухоли и системой подачи жидкости для орошения места удаления). После чего срезанные фрагменты опухоли удаляются струей воды. Таким образом освобождается путь для оттока мочи.
Лазерная деструкция
Удаление выступающего участка простаты также производится неинвазивно, однако в данном случае используется не скальпель, а лазер с длиной волны 532 нм. Во время прижигания лазером опухоль практически мгновенно переходит в газообразное состояние, что позволяет избежать кровотечения и удалить практически весь воспаленный участок простаты. Эта процедура задействует сложное оборудование и является одной из самых дорогостоящих.
Это важно
Аденомэктомия — радикальный метод вмешательства. Врачи-урологи, имеющие в своем распоряжении целый арсенал медикаментозных и малоинвазивных средств, а также несколько видов профилактической и поддерживающей терапии, прибегают к открытому хирургическому вмешательству в крайних случаях. В Интернете достаточно статей, рассказывающих о том, что оперативное вмешательство является самым эффективным способом избавления от аденомы простаты.
Это не так. Во-первых, как вы могли убедиться выше, существует немало альтернативных способов возвращения мужчине качества жизни, а во-вторых, ни один врач не направит пациента на операционный стол, не убедившись в том, что опухоль невозможно купировать другим способом. Однако на поздних стадиях, когда заболевание слишком запущено, аденомэктомия может оказаться единственным выходом.
Удаление узлов аденомы производится врачом через открытый разрез. После операции пациенту необходимо провести несколько дней в стационаре, а в последующие недели соблюдать реабилитационную программу.
Чтобы избежать хирургического вмешательства, доктора настаивают не только на немедленном обращении в поликлинику при появлении первых симптомов, например прерывистом мочеиспускании, но и на регулярных профилактических осмотрах. Эти простые меры помогут выявить аденому простаты на ранней стадии.
Показания к лечению аденомы простаты препаратами
Сроки лечения могут быть достаточно длительными, особенно при положительном результате лечения – стабилизации патологического процесса.
Как правило, препараты принимаются комплексно, врач подбирает их индивидуально для каждого отдельного пациента, однако эффект от медикаментозного лечения на 50% зависит от самого мужчины – в частности, от того, насколько аккуратно он будет соблюдать график приема выписанных ему лекарств.

Большинство медикаментов, назначаемых при аденоме простаты, – сильнодействующие. Только тогда, когда болезнь находится в первой, начальной, стадии, уролог может предложить пациенту препараты с действующим веществом природного происхождения.
Альфа-блокаторы
Первая группа медикаментов, назначаемых при аденоме простаты, – это альфа-адреноблокаторы. Данные лекарственные препараты снижают артериальное давление за счет уменьшения спазма мелких артерий, предшествующих капиллярам.
Альфа-блокаторы помогают лечить аденому простаты, расслабляя ткани гладких мышц, простаты и шейки мочевого пузыря, что позволяет увеличить ток мочи из мочевого пузыря. Как правило, принимаются перорально 1-2 раза в день. Альфа-блокаторы используются пациентами при симптомах средней тяжести, которые доставляют беспокойство.
Альфа-блокаторы более эффективны в уменьшении симптомов, чем Финастерид.
