Аннотация научной статьи по клинической медицине, автор научной работы — Данилов Вадим Валерьевич, Борисов Владимир Викторович, Остобунаев Василий Васильевич, Данилов Валерий Вадимович, Борщенко Сергей Александрович
Под наблюдением находилась группа пациентов (35 случаев, средний возраст 62 года), имеющих аденому предстательной железы в сочетании с нейрогенным мочевым пузырем . Для объективизации динамики клинической симптоматики использовались методы уродинамического мониторинга, в частности домашней урофлоуметрии. В основе комбинированной терапии, назначенной на периода времени (30 месяцев), был нетитруемый альфа-1-адреноблокатор силодозин, в сочетании с Л-карнитином и финастеридом. Анализ полученных результатов позволил сделать вывод о том, что вышеуказанное лечение позволяет длительно, эффективно и безопасно вести пациентов, имеющих аденому предстательной железы (АПЖ) и нарушения уродинамики нижних мочевых путей, обусловленные нейрогенным мочевым пузырем (НМП).
Похожие темы научных работ по клинической медицине , автор научной работы — Данилов Вадим Валерьевич, Борисов Владимир Викторович, Остобунаев Василий Васильевич, Данилов Валерий Вадимович, Борщенко Сергей Александрович
Peculiarities of a long-term therapy among patients with prostatic adenoma and neurogenic bladder
We observed a group of patients (35 cases, mean age 62) with an adenoma of the prostate in combination with neurogenic bladder. In order to object the dynamics of clinical symptoms there were used urodynamic monitoring methods particularlt the method of domestic urofluometry. Based on the combined therapy that lasted for 30 monthsthere was used a netitruemy alpha-1-blocker silodosin in combination with L-carnitine and finasteride. Analysis of the results led to the conclusion that the above-mentioned long-term treatment can effectively and safely guide patients with adenoma of the prostate (BPH) and violation of urodynamics of lower urinary tract caused by neurogenic bladder (NMP).
В.В. Данилов, В.В. Борисов, В.В. Остобунаев, В.В. Данилов,
С.А. Борщенко, В.В. Данилов
особенности длительной терапии у пациентов с аденомой предстательной железы и нейрогенным
Под наблюдением находилась группа пациентов (35 случаев, средний возраст 62 года), имеющих аденому предстательной железы в сочетании с нейрогенным мочевым пузырем. Для объективизации динамики клинической симптоматики использовались методы уродинамического мониторинга, в частности домашней урофлоуметрии. В основе комбинированной терапии, назначенной на периода времени
DANILOV Vadim Valer’evich — Professor of the Department of surgery and urology of Pacific National Medical University. Address: 690000, Vladivostok, Ostryakova St. 2. Tel: 8(914)7040999. E-mail: vadim_ danilov@list.ru
BORISOV Vladimir Viktorovich — Professor of the Department of nephrology and hemodialysis of vocational education of I.M. Sechenov First Moscow State Medical University. Moscow, Rossolimo St, 11a, block 4. Tel: 8(499)2485608. E-mail: vvb56@yandex.ru
DANILOV Vitaliy Vadimovich — a 6th year student of Pacific National Medical University. Address: 690000, Vladivostok, Ostryakova St., 2. Tel: 8(914)7040999. E-mail: vadim_danilov@list.ru
(30 месяцев), был нетитруемый альфа-1-адреноблокатор силодозин, в сочетании с Л-карнитином и фи-настеридом. Анализ полученных результатов позволил сделать вывод о том, что вышеуказанное лечение позволяет длительно, эффективно и безопасно вести пациентов, имеющих аденому предстательной железы (АПЖ) и нарушения уродинамики нижних мочевых путей, обусловленные нейрогенным мочевым пузырем (НМП).
Ключевые слова: нейрогенный мочевой пузырь, аденома предстательной железы, хроническая микцион-ная недостаточность, уродинамика, инфравезикальная обструкция, домашний урофлоумониторинг, альфа-1-адреноблокаторы, Л-карнитин, ингибиторы 5-альфа редуктазы, микционные показатели, объемный скоростной профиль, простат специфический антиген, трансректальное ультразвуковое исследование.
V.V. Danilov, V.V. Borisov,VV Ostobunaev, V.V. Danilov, S.A. Borshenko,V.V. Danilov
Peculiarities of a long-term therapy among patients with prostatic adenoma and neurogenic bladder
We observed a group of patients (35 cases, mean age 62) with an adenoma of the prostate in combination with neurogenic bladder. In order to object the dynamics of clinical symptoms there were used urodynamic monitoring methods particularlt the method of domestic urofluometry. Based on the combined therapy that lasted for 30 monthsthere was used a netitruemy alpha-1-blocker silodosin in combination with L-carnitine and finasteride. Analysis of the results led to the conclusion that the above-mentioned long-term treatment can effectively and safely guide patients with adenoma of the prostate (BPH) and violation of urodynamics of lower urinary tract caused by neurogenic bladder (NMP).
Keywords: neurogenic bladder, prostate adenoma, chronic voiding failure, urodynamics, bladder outlet obstruction, home urofloumonitoring, alpha-1-blockers, L-carnitine, inhibitors of 5-alpha reductase, voiding performance, volume speed profile, prostate specific antigen, transrectal ultrasonography.
Актуальность. Увеличение продолжительности жизни населения приводит к изменению демографической структуры, а вместе с этим меняется и характер самой патологии [1, 2, 3, 4]. Влияние факта относительно большего удельного веса пожилого населения в сравнении с двумя предыдущими десятилетиями проявляется уже в настоящее время в том, что растет число больных с нейроурологической патологией, сопровождающей и без этого такое распространенное заболевание, как аденома предстательной железы (АПЖ) [5, 1, 4]. Выражается это также в том, что начинают играть заметную роль нейрогенный мочевой пузырь (НМП), а также такое явление, как хроническая микционная недостаточность, усугубляющие течение инфекций мочевой системы, почечной недостаточности, заболеваний сердечно-сосудистой системы и т.д. [5, 6]. С другой стороны, в настоящее время появилось большое число лекарственных средств (ЛС), позволяющих эффективно восстанавливать уродинамику нижних мочевых путей и существенно снижать оперативную активность, при этом улучшая отдаленные результаты лечения [5, 7, 8].
Цель исследования: изучение возможности длительного ведения пациентов с аденомой предстательной железы и нейрогенным мочевым пузырем при назначении комбинированной терапии нетитруемыми суперселективными альфа-1-адреноблокаторами и препаратами Л-карнитина.
Материалы и методы. Под нашим наблюдением находилась группа мужчин с аденомой предстательной железы (35 пациентов, средний возраст 62 года), длительность ведения составила в среднем 30 месяцев (от 12 до 48 месяцев). Особенностью дизайна исследования было то, что в группу вошли пациенты только после исключения злокачественного заболевания простаты и предварительного проведения 3-месячной терапии в связи с расстройствами мочеиспускания. В последующем, с момента назначения ингибиторов 5-альфа редуктазы, пациенты включались в группу наблюдения. На протяжении всего периода наблюдения в схеме терапии использовались альфа1-адреноблокаторы (силодозин, УРОРЕК), препараты группы Л-карнитина и витамины. Для оценки клинической симптоматики использовались таблицы IPSS, функциональное
состояние нижних мочевых путей определялось с помощью домашнего урофлоумониторинга, исследование предстательной железы проводилось методом ТРУЗИ, помимо этого были задействованы методы лабораторной диагностики, включая биохимические показатели, ПСА.
Результаты. Исходно суммарный балл по таблице IPSS в группе наблюдения составил 7,91, после терапии — 3,4. Изменения коснулись всех симптомов, но наиболее значимой была динамика 1, 4 и 5 симптомов. Именно эти характеристики фазы опорожнения характеризуют НМП как функциональную патологию нижних мочевых путей (рис. 1).
Рис. 1. Динамика симптомов по таблице ШББ, слева — до, справа — после лечения.
Симптомы обозначены соответственно нумерации в таблице IPSS
Качество жизни пациентов улучшилось, что вполне закономерно: 2,7 в начале лечения, в конце периода наблюдения — 1,5. Но интересен другой факт. Размеры предстательной железы, полученные методом ТРУЗИ исходно и после окончания наблюдения, в среднем уменьшились с 67,8 до 61,6 гр. Но в 40 % случаев (14 наблюдений), наоборот, отмечено увеличение с 54 до 67 гр., а в 60 % (21 наблюдение) объем простаты уменьшился с 78 до 53 гр. Анализ тех случаев, когда зафиксировано увеличение простаты, показал, что имели место факты отмены назначения И5АР на сроки от 3 месяцев до 1 года. За период отмены происходил рост объема, при этом динамика была довольно выражена.
Единственный показатель, практически не изменившийся, — ночная поллакиурия. Если в начале ведения в среднем по группе показатель составлял 1,14, то через 30 месяцев уже снижался до 0,89. Изменения недостоверны, что, в принципе, естественно для данной возрастной подгруппы.
Рис. 2. Объемный (слева) и скоростной (справа) профили мочеиспускания.
Обозначения синим цветом — в начале наблюдения, красным — по окончании длительного ведения
Однако здесь следует отметить, что даже такой метод, как ДФМ, не позволяет заявлять о том, что объективные изменения уродинамики существенны. Практически все показатели недостоверно отличаются от тех, которые были приняты за исходные с момента подключения И5АР в терапию. Можно уверенно говорить лишь о положительной тенденции изменений в уродинамике нижних мочевых путей, но не более того (0,5 Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
2. Рекомендации совещания Совета экспертов по лечению аденомы предстательной железы. — М., 2009. — 17 с.
3. Kirby, R., Bratish, G., Lepor, H. The Role of Alpha Blockers in Benign Proststic Hyperplasia, Montreal 1997. — 55 p.
4. Данилов, В.В. и соавт. Патогенетические основы одновременной коррекции эректильной дисфункции и расстройств мочеиспускания / В.В. Данилов и соавт. // Тихоокеанский медицинский журнал. — 2011. — № 1. — С. 36-40.
5. Вишневский, А.Е. Роль гипоксии детрузора в патогенезе расстройств мочеиспускания у больных доброкачественной гиперплазией предстательной железы и обоснование методов их консервативного лечения: автореф. дис. . канд. мед. наук / А.Е. Вишневский. — М, 1998. — 25 с.
6. Данилов, В.В., Данилова, Т.И., Данилов, В.В. Клинико-уродинамическое подтверждение нейрофизиологической модели гиперактивного мочевого пузыря / В.В. Данилов, Т.И. Данилова, В.В. Данилов // Урология. — 2010. — № 4. — С. 15-20.
7. Говоров, А.В., Пушкарь, Д.Ю. Применение силодозина для лечения больных аденомой предстательной железы / А.В. Говоров, Д.Ю. Пушкарь // Урология. — 2012. — № 3. — С. 15-18.
8. Лоран, О.Б., Вишневский, Е.Л., Вишневский, А.Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты альфа-адреноблокаторами / О.Б. Лоран, Е.Л. Вишневский, А.Е. Вишневский. — М.: ТЕРРА. 1998. — 124 с.
9. Вишневский, Е.Л., Лоран, О.Б., Вишневский, А.Е. Клиническая оценка расстройств мочеиспускания / Е.Л. Вишневский, О.Б. Лоран, А.Е. Вишневский. — М.: ТЕРРА, 2001. — 96 с.
10. Вишневский, Е.Л. и соавт. Урофлоуметрия / Е.Л. Вишневский и соавт. — М.: Печатный город, 2004.
11. Данилов, В.В. и соавт. Клинико-уродинамическая оценка эффективности консервативной терапии расстройств мочеиспускания у больных АПЖ / В.В. Данилов и соавт. // Урология. — 2013. — № 5. — С. 55-58.
12. Леонова, М.В., Белоусов Ю.Б. Селективный постсинаптический блокатор а1-адренорецепторов тонокардин. — ПЛИВА, 1997. — 28 с.
2. Rekomendacii soveshhaniya Soveta Ekspertov po lecheniyu adenomy predstatel’noyi zhelezy. — M., 2009.
3. Kirby, R., Bratish, G., Lepor, H. The Role of Alpha Blockers in Benign Proststic Hyperplasia, Montreal.
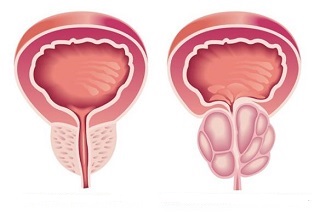
Гиперплазия предстательной железы (доброкачественная гиперплазия простаты, аденома простаты) – доброкачественное увеличение размеров простаты (в норме объем простаты не превышает 30 см 3 ) является одним из самых распространенных заболеваний у мужчин пожилого возраста. В возрасте около 50 лет оно встречается практически у каждого второго. К 80 годам гиперплазия простаты встречается у 80% мужчин.
Этиология и патогенез
Простата расположена под мочевым пузырем и мочеиспускательный канал (уретра) проходит сквозь ее толщу. Предстательная железа имеет три основные функциональные зоны: центральную (25 %), периферическую (70 %) и переходную, или транзиторную (5 %). C современной точки зрения суть патологического процесса заключается в формировании множественных узлов гиперплазии в переходной зоне. По мере увеличения гиперплазированная ткань сдавливает простатический отдел уретры и его просвет приобретает щелевидную форму. В результате развивается инфравезикальная обструкция (или подпузырное сдавливание уретры), препятствующая нормальному опорожнению мочевого пузыря. Увеличивающиеся в размерах доброкачественные узлы аденомы отдавливают к периферии собственную ткань простаты. На границе между ними образуется фиброзный слой ткани, получивший название хирургической капсулы.
С возрастом повышается активность фермента 5 альфа-редуктазы, под воздействием которого внутриклеточный тестостерон превращается в более активный метаболит 5 альфа-дегидротестостерон, который воздействуя через андрогенные рецепторы активизирует факторы роста, что приводит к гиперплазии.
Симптомы
Клинические проявления гиперплазии простаты делятся на: обструктивные — задержка перед началом мочеиспускания, тонкая и вялая струя мочи, затрудненное мочеиспускание, прерывистое и длительное мочеиспускание, чувство неполного опорожнения мочевого пузыря, задержка мочеиспускания и парадоксальная ишурия (непроизвольное выделение мочи по каплям при переполненном мочевом пузыря);
Ирритативные — учащенное дневное и ночное мочеиспускание, неудержимые позывы к мочеиспусканию.
Частым и опасным осложнением аденомы простаты является острая задержка мочеиспускания – состояние, при котором пациент испытывает сильный позыв, но не может помочиться. Часто она связана с отеком простаты вследствие нарушения кровообращения в малом тазу на фоне приема алкоголя, переохлаждения или нарушения функции кишечника (запоров). Этим больным требуется неотложная помощь в виде установки катетера в мочевой пузырь через мочеиспускательный канал (катетеризация) или через переднюю брюшную стенку (цистостомия). Еще одним частым осложнением и симптомом аденомы простаты является примесь крови в моче, видимая или не видимая на глаз — микро- и макрогематурия. Она возникает при повышении венозного давления в сосудах малого таза из варикозно расширенных вен шейки мочевого пузыря и может быть весьма значительным с формированием сгустков в полости мочевого пузыря вплоть до невозможности мочеиспускания. Наряду с этим, на фоне и по причине аденомы простаты возможно формирование камней и дивертикулов мочевого пузыря, нарушение оттока мочи из почек (уретерогидронефроз) и хроническая почечная недостаточность.
Выбор метода лечения пациентов с гиперплазией предстательной железы осуществляется индивидуально с учетом возраста, сопутствующих заболеваний, выраженности симптомов болезни, размера и характера роста гиперплазированной ткани, наличия осложнений и других факторов.
В зависимости от вышеизложенных критериев лечение делится на консервативное (медикаментозное) и хирургическое.
Выделяют несколько основных групп лекарственные средств, используемых для консервативного лечения аденомы простаты:
- Альфа-1- адреноблокаторы (тамсулозин, доксазозин, альфузозин, теразозин, силодозин).
- Ингибиторы 5 альфа — редуктазы (финастерид, дутастерид).
- Комбинированные средства (тамсулозин+дутастерид).
- Препараты растительного происхождения (препараты Serenoa repens).
Положительное влияние данных лекарственных средств на мочеиспускание обусловлено расслаблением шейки мочевого пузыря и простатического отдела уретры, а также некоторым уменьшением размера предстательной железы. Данная терапия является безопасной, хотя не лишена ряда побочных явлений (ретроградная эякуляция, снижение либидо и эректильной функции) и может быть назначена на длительное время (пожизненно). В случае неэффективности консервативного лечения и/или нежелании пациента продолжать ее, встает вопрос о необходимости хирургического, то есть оперативного лечения.
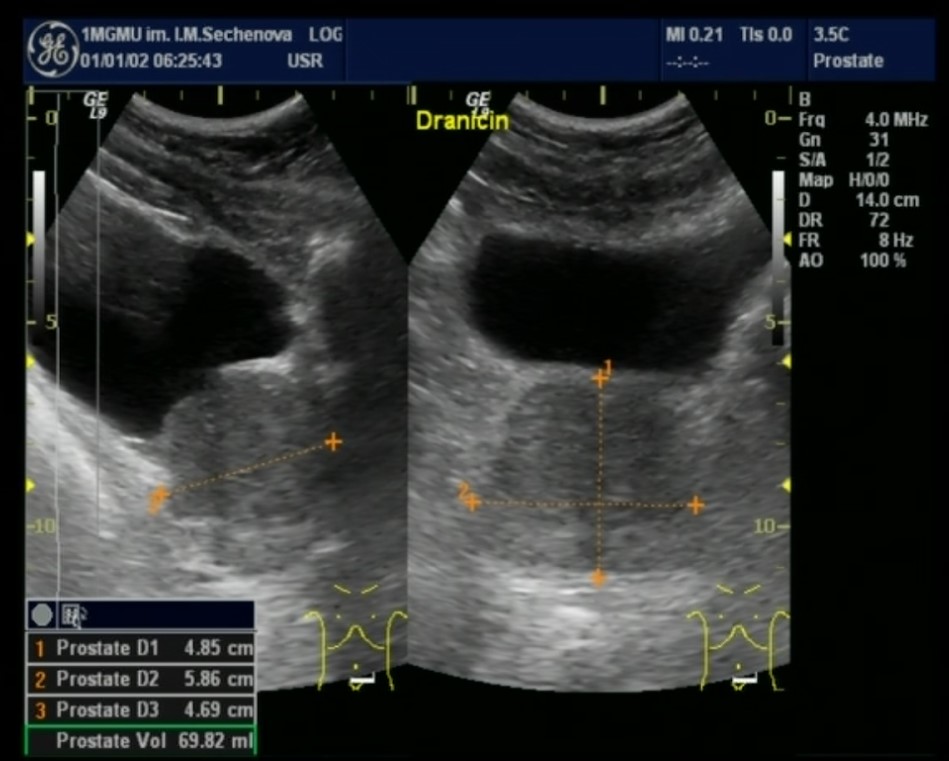
Диагностика
Выявление гиперплазии (аденомы) простаты основано на результатах клинического (врачебного) осмотра и инструментальных методов обследования. Пальцевое ректальное исследование предстательной железы позволяет оценить размер простаты (в норме она имеет размер грецкого ореха или каштана), ее консистенцию (однородная, плотно-эластическая, когда при раке она бугристая), болезненность (при гиперплазии простата безболезненна).
Основным методом диагностики гиперплазии предстательной железы сегодня является ультразвуковое исследование (УЗИ), которое позволяет определить точный размер и объем простаты, характер ее роста (в полость мочевого пузыря с формированием средней доли или за счет преимущественно боковых долей), объем остаточной мочи после мочеиспускания, наличие или отсутствие таких осложнений как камни мочевого пузыря, дивертикулы мочевого пузыря, а также оценить состояние почек и верхних мочевыводящих путей. Для полной оценки простаты выполняют трансабдоминальное (через переднюю брюшную стенку — ТАУЗИ) и трансректальное (через прямую кишку — ТРУЗИ) ультразвуковое исследование. Последнее крайне важно для выявления изменений в структуре простаты, подозрительных в отношении рака.
Для объективной оценки качества мочеиспускания и уточнения степени его нарушения выполняется специальное исследование – урофлоуметрия. Она заключается в том, что пациент, испытывающий адекватный позыв на мочеиспускание, мочится в специальный прибор — урофлоуметр. При этом определяется ряд показателей, наиболее важными из которых являются максимальная объёмная скорость мочеиспускания (Qmax, мл/сек) и средняя скорость мочеиспускания (Qavg, мл/сек). Значение Qmax больше 15 мл/сек указывает на адекватное качество мочеиспускания.
Всем пациентам с данным заболеванием выполняется анализ крови для определения уровня так называемого простатспецифического антигена (ПСА, PSA) значение которого может повышаться при различных заболеваниях предстательной железы (аденома, простатит, рак). В норме уровень общего ПСА находится в промежутке от 0 до 4 нг/мл. В большинстве случаев повышение уровня общего ПСА требует выполнения трансректальной биопсии простаты с целью исключения наличия злокачественного процесса.
В сложных и неоднозначных клинических ситуациях, когда причина плохого мочеиспускания не столь очевидна, возможно выполнение дополнительных исследований: ультразвуковой микционной цистоуретроскопии (тарнсректальное УЗИ простаты во время мочеиспускания), уретрографии, комплексного уродинамического исследования.

| Опорожнения | Накопления |
|
|
- выявление заболевания, определение характера и степени дисфункции мочевого пузыря и сопутствующих осложнений;
- дифференциальную диагностику с другими заболеваниями предстательной железы и состояниями, проявляющимися симптоматикой расстройства мочеиспускания;
- выбор оптимального метода лечения.




Симптомы (по шкале IPSS)
Качество жизни (по шкале QOL)
Максимальная скорость потока мочи
Qmax _____ (в мл/с)
Объем (масса) простаты
V____ (в см 3 или г)
Степень инфравезикальной обструкции
PQ ___ PdetCM вод. ст при Qmax______ (в мл/с)
- инфекция мочевых путей, констатируемая в настоящее время или в анамнезе;
- гематурия (макроскопическая или микроскопическая);
- мочекаменная болезнь, диагностируемая в настоящее время или в анамнезе;
- предшествующие операции на мочевых путях и половых органах.
Высокие показатели смертности от рака предстательной железы в России объясняются низким качеством диагностики. Несмотря на возрастающие темпы внедрения в клиническую практику современных методов диагностики, в последнее десятилетие число локализованных форм рака предстательной железы не только не ув.
Эпидемиология. Частота рака предстательной железы (РПЖ) неоднородна в разных странах. В США он занимает 2-е место среди злокачественных заболеваний у мужчин, составляет 18% от вновь выявленных опухолей и 10% от всех летальных исходов среди этих больных [Flanders W., 1984]. Выявлена э.
Клиническая картина аденомы простаты определяется тремя компонентами: симптомами нижних мочевых путей, увеличением предстательной железы и дисфункцией мочевого пузыря. Последняя может проявляться инфравезикальной обструкцией, нестабильностью или гипотонией (рис. 1). В клинической картине доброкачест.
К лечению пациентов приступают только тогда, когда патологические изменения достигают стадии клинических проявлений. Вопрос о показанности профилактической терапии сегодня остается открытым, а его целесообразность недоказанной. Если еще 10 лет назад реальной альтернативы операции при аденоме простат.
Наблюдение за больными в послеоперационном периоде является неотъемлемой частью процесса лечения онкоурологических больных. Это обусловлено в первую очередь тем, что у незначительной части больных после операции возникают ранние или отдаленные осложнения (стриктуры, недержание мочи, импотенция и.
До недавнего времени ведущей клинической классификацией доброкачественной гиперплазии предстательной железы являлась классификация Гюйона (Guyon), основанная на характеристиках функционального состояния мочевого пузыря и как следствие изменении количества остаточной мочи.
быстрый переход
Что такое аденома простаты
Заболевание, обусловленное гиперпластическим (то есть таким, когда объем ткани увеличивается за счет роста числа клеток) увеличением предстательной железы, называется аденома простаты (ДГП, доброкачественная гиперплазия предстательной железы, простаты узловая гиперплазия, ДГПЖ, простаты доброкачественная гиперплазия, аденома предстательной железы). Довольно распространенное мнение, что аденома представляет собой опухоль, — ошибочно.
Данная урологическая патология часто встречается в старшем возрасте у мужчин. Аденоматозная гиперплазия проявляется у 25% мужчин, достигших 50-летнего возраста и у 50% — 65-тилетнего. Далее заболевание поражает до 85% представителей мужского пола, причем микроскопические признаки патологии определяются, начиная с возраста 30– 40 лет.
Аденома приводит к значительному снижению качества жизни больного, когда приходится:
- вставать ночью для совершения акта мочеиспускания;
- ограничивать питье;
- ограничивать половую и социальную активность.
Причины
Достоверно причинные факторы заболевания не установлены, тем не менее, высказывается предположение о полиэтиологичности патологии (зависимость от нескольких причин).
- Повышение в аденоматозных клетках активности фермента 5-альфа-редуктазы. Данный фермент ответственен за превращение в клетках тестостерона в 5-альфа-дигидротестостерон, который активирует определенные гены ядра путем связывания с последним. В результате стимулируется продуцирование факторов роста (специфических веществ), ускоряющих процессы клеточного деления и созревания.
- Возрастное изменение в организме мужчины соотношения уровней андрогенов и эстрогенов.
Доброкачественная гиперплазия простаты представляет собой вовлечение в процесс как железистой, так и соединительной, и мышечной тканей, что обуславливает не только ее аденоматозный (железистый) характер, но также миоматозный (мышечный) или фиброзный (рубцовый). Патологические узелки, как правило, содержат больше соединительной ткани, чем здоровой железистой. По мере прогрессирования заболевания здоровая ткань железы вытесняется и замещается узлами гиперплазии.
Симптомы
Различают симптомы наполнения и опорожнения. Симптомы наполнения являются следствием поражения нервно-мышечного аппарата мочевого пузыря и включают:
- ночное мочеиспускание;
- частое мочеиспускание;
- повелительные (неотложные, императивные) мочеиспускательные позывы.
В результате сужения увеличенной простатой просвета мочеиспускательного канала развиваются симптомы опорожнения:
- затруднение мочеиспускания;
- слабый напор мочевой струи;
- прерывистость мочевого потока;
- необходимость для начала мочеиспускательного акта напряжения мышц передней брюшной стенки;
- чувство неполного опорожнения;
- в конце мочеиспускательного акта ‑ длительное капельное выделение мочи.
ДГП отличается медленным прогрессированием заболевания и на начальных этапах зачастую не имеет проявлений. По мере разрастания железы симптоматика усиливается.
Еще одним характерным моментом гиперплазии служит волнообразное течение процесса с попеременным усилением и ослаблением симптомов даже в отсутствии лечения.
Усиливают симптоматические проявления провоцирующие факторы:
- стресс;
- употребление алкоголя;
- переохлаждение;
- обострение хронического простатита.
Определяет степень мочеиспускательных нарушений не только объем простаты, но и выраженность дисфункции мочевого пузыря.
Выраженное нарушение мочеиспускания может вызвать нависающая в виде клапана над уретрой увеличенная средняя доля предстательной железы (если разрастанию подверглась задняя группа желез). Если же рост большой аденомы осуществляется в направлении прямой кишки (назад) из боковых периуретральных желез, то клинические признаки заболевания могут отсутствовать довольно долго.
Важно! Не всегда выраженность симптомов аденомы определяется степенью увеличения железы!
Стадии ДГПЖ
Стадия I (аденома простаты 1 степени). Отмечаются вялость мочевой струи, сильные позывы на мочеиспускание (с наибольшей выраженностью в ночное время), мочеиспускание учащенной и несколько затрудненное.
Стадия II. Присутствуют истончение и выраженная вялость мочевой струи, развивается чувство неполного опорожнения из-за образования остаточной мочи, возможны нарушения почечной функции и острая задержка мочи.
Стадия III. Возникает парадоксальная ишурия: мышечный тонус мочевого пузыря отсутствует, у больного не получается помочиться, что обуславливает переполнение мочевого пузыря, но при этом моча самопроизвольно постоянно выделяется в виде капель. Нарушение почечной функции становится более выраженным, расширяются верхние мочевые пути.
Осложнения
- Длительное задерживание мочеиспускания, стресс, поносы, запоры, диетические погрешности, прием алкоголя, переохлаждение, катетеризация мочевого пузыря провоцируют на первых двух стадиях заболевания острую задержку мочи.
- Повреждение шеечной области мочевого пузыря из-за присутствия в нем конкрементов (особенно после физической нагрузки, ходьбы) или повышенного давления варикозно расширенных вен обуславливает появление в моче крови (гематурию).
- Застой мочи, цистит (воспаление мочевого пузыря), обуславливающий наличие остаточной мочи, провоцируют образование конкрементов мочевого пузыря.
- Атрофия мышечного слоя в мочевом пузыре, обусловленная высоким давлением в последнем, выдавливание наружу слизистой мочевого пузыря между мышечными истонченными волокнами, так называемый ложный дивертикул мочевого пузыря (как правило, множественного характера).
- Заброс в мочеточник из мочевого пузыря мочи, являющийся следствием хронической или острой задержки мочи, который носит название пузырно-мочеточниковый рефлюкс. Попадание мочи в почки из мочевого пузыря также является причиной пиелонефрита, гидронефроза, хронической почечной недостаточности.
- Развитие в мочевом пузыре инфекционного процесса, обусловленное благоприятствующим воздействием остаточной мочи (появляется со II стадии заболевания) на размножение бактерий, которое называется цистит.
- Развитие хронического простатита из-за нарушений секреторного оттока и кровоснабжения простаты, связанных с разрастанием железы.
Диагностика аденомы
Опрос пациента, заполнение им анкеты со шкалой (принятой на международном уровне) оценки простатических симптомов (IPSS).
Клинические данные.
- Пальцевое ректальное исследование выявляет симметричное увеличение безболезненной железы плотно-эластической консистенции (хотя бывает и незначительная асимметрия), сглаженную срединную бороздку.
- Лабораторные аналитические методы (общие анализы крови и мочи, ПСА, биохимический анализ крови).
- Увеличение размеров железы, наличие аденоматозных узлов хорошо визуализируется на УЗИ, проводимом трансректально (ТРУЗИ).
- Для оценки скорости мочевого потока осуществляется урофлоуметрия.
- Рентгенологические методы проводятся только при наличии инфекций путей мочевыделения, дивертикулах и камнях мочевого пузыря, предшествующих операциях, гематурии. Экскреторной урографией выявляется расширение мочеточников, а также ЧЛС (чашечно-лоханочной системы) почек. На цистографии аденома имеет вид выступающего в просвет мочевого пузыря холма.
- МРТ (для выявления злокачественных поражений предстательной железы).
Дифференциальный диагноз следует проводить между доброкачественной гиперплазией и такими патологиями, как:
- стриктура уретры;
- гиперактивный или нейрогенный мочевой пузырь;
- стеноз или склероз шейки мочевого пузыря;
- рак простаты.
Лечение аденомы простаты
Терапевтический подход зависит от стадии процесса, выраженности эффекта от консервативных мероприятий, выраженности нарушений качества жизни больного.
Так, на I стадии лечение обычно проводится консервативно. II стадия предполагает консервативную терапию, а в отсутствие эффекта показано хирургическое лечение. На III стадии осуществляется проведение исключительно оперативных вмешательств.
- Препараты растительного происхождения, обладающие противовоспалительным действием, и также ингибирующие воздействие 5-альфа-редуктазы. Такие средства уступают в эффективности синтетическим лекарственным препаратам.
- Альфа-Адреноблокаторы, обладающие симптоматическим действием, расслабляющие мышечный компонент уретры и простаты. Такие средства снижают выраженность проявлений, улучшают мочевой отток. Побочными эффектами действия альфа-адреноблокаторов являются ретроградная эякуляция и уменьшение артериального давления.
- Ингибиторы 5-альфа-редуктазы применяются, если объем простаты превышает 40 мл и редко у продолжающих половую жизнь мужчин. Последнее связано с тем фактом, что подобные вещества уменьшают объем спермы, провоцируют эректильную дисфункцию (и даже импотенцию), снижают либидо, иногда могут спровоцировать увеличение грудной железы (гинекомастию).
В отсутствие эффекта от проводимой консервативной терапии осуществляют инвазивное лечение ДГПЖ. Подобные методы также показаны в случае:
- неустранимой консервативно острой задержки мочеиспускания;
- гидронефроза;
- рецидивирующих ИМП (инфекций мочевых путей);
- почечной недостаточности;
- дивертикула мочевого пузыря значительного размера;
- рецидивирующей гематурии, которая связана с венами шейки мочевого пузыря варикозно расширенными;
- наличия конкрементов в мочевом пузыре.
На данный момент предпочтительными являются эндоскопические методы лечения, включающие методики с применением лазера и трансуретральные:
- инцизию (ТУИП);
- резекцию (ТУР; ТУРП);
- электровапоризацию (ТУВП; ТУВ);
- игольчатую абляцию (TUNA).
К не эндоскопическим минимально инвазивным методам лечения относятся:
- ТУМП (трансуретральная микроволновая терапия);
- криодеструкция (разрушение разрастаний холодом);
- фокусированный высокоинтенсивный ультразвук;
- установка уретрального стента;
- балонная дилатация;
- инъекции этилового спирта;
- микроволновая гипертермия (применяемая при отсутствии риска опухолевой малигнизации (озлокачествления) термальная терапия).




