К прогестинам (гестагенам) относят препараты, обладающие свойствами гормона желтого тела (прогестерона). Они способны влиять на пролиферацию слизистой оболочки полости матки. Kistner (1959, 1962) показал, что производные прогестерона могут вызывать обратное развитие аденоматозной гиперплазии эндометрия или карциномы in situ. В 1960 г. Kelly и Bekker сообщили о возможности
Оксипрогестерон-капронат (Oxyprogesteronum capronicum) — прегнен-4-ол-17а-дион-3,20-капронат. Является синтетическим аналогом гормона желтого тела — прогестерона, отличаясь от него большой стойкостью в организме и соответственно более медленным действием и способностью к пролонгированию эффекта.

Препарат выпускают в ампулах, содержащих 1 мл масляного 12,5% (125 мг) или 25% (250 мг) раствора оксипрогестерон-капроната.
Обычно вводят препарат по 1 г (4 ампулы 25% масляного раствора) внутримышечно, ежедневно или через день в течение 1—2 мес. При эффекте или стабилизации болезни лечение продолжают длительно по 1 г 1 — 2 раза в неделю. Лечебный эффект достигается у 30— 40% больных.
БАД «Фотостим» предназначен для:
- онкологических больных, имеющих злокачественные опухоли разных стадий;
- лиц с риском перерождения доброкачественных дерматозов (родинок, бородавок, папиллом) и предраковых состояний (лейкоплакий, дисплазивных очагов) в онкологические заболевания;
- лиц пожилого возраста для повышения сопротивляемости организма онкологическим заболеваниям;
- лиц, перенесших тяжелые хирургические, лучевые, химиотерапевтические* воздействия, в реабилитационный период для скорейшего восстановления организма;
- кроме того, «фотостим» рекомендуется к применению лицами с ослабленным иммунитетом.
Показания к применению фотостима.Существует несколько показаний для применения «Фотостима» : Механизм действия фотостима.«Фотостим» усиливает гуморальный иммунитет в 60-70% случаев за счет роста популяции лимфоцитов, а в 30-40% случаев — популяции нейтрофилов в крови. Стимуляция клеточного иммунитета при употреблении «Фотостима» достигается за счет роста абсолютного количества фагоцитов а у 35% лиц также и за счет роста активности фагоцитов и NK-клеток. NK-клетки активируются под влиянием дисплазивных (аномальных) клеток, бактерий, их токсинов или продуктов метаболизма. В целом, » Фотостим» специфически стимулирует пролиферацию клонов В-клеток костного мозга и продукцию вилочковой железы. «Фотостим» стимулирует формирование антител к опухолевым клеткам, активирует регенерацию пораженных тканей и, таким образом, увеличивает продолжительность жизни (или предотвращает ее сокращение) и значительно улучшает качество жизни онкологических больных. Кроме того, во многих случаях тормозится рост первичного очага опухоли и предотвращается появление метастазов. «Фотостим» способен не только тормозить рост опухолей и вызывать их разрушение, усиливать и активировать имеющиеся механизмы защиты организма, но и уничтожать предшественников раковых клеток — дисплазивные (аномальные) клетки. Образно выражаясь, фотостим является «разведывательно-диверсионной группой», задачей которой является обнаружение врага — клеток, отличающихся от нормальных, передача информации в центр (в мозг) и осуществление скоординированных мероприятий по их уничтожению. Клинические исследования фотостима.Клинические исследования показали, что «Фотостим» :
«ФОТОСТИМ» Его уникальность заключается в том, что 1) Онкологическая клетка поглощает фотосенсибилизатор, например, «ФОТОСТИМ».
2) Орган освещается светом. Онкологическая клетка погибает.
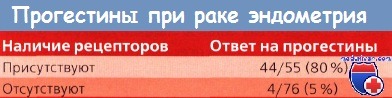
Заключение института Геронтологии. Анализ полученных результатов свидетельствует о том, ВЫВОДЫ (фрагмент из заключения института геронтологии): «Фотостим» оказывает положительное влияние Несмотря на то что смертность от рака эндометрия (РЭ) ниже, чем при злокачественных опухолях шейки матки и яичников, она все же остается высокой, особенно если принять во внимание подавляющее число больных с первично диагностированной I стадией. Некоторые рецидивы, например, в культе влагалища можно успешно лечить с помощью хирургического вмешательства, ЛТ или комбинированным методом. Прогноз для многих больных благоприятный, и они живут достаточно долго. К сожалению, во многих случаях рецидивы возникают за пределами верхней части влагалища и поэтому не подлежат ни хирургическому лечению, ни ЛТ. У некоторых пациенток ЛТ имеет ограниченное значение, особенно если ее применяли как этап первичного лечения. Следовательно, для многих пациенток с рецидивом рака эндометрия (РЭ) терапией выбора остается гормональная или химиотерапия. Прогестины назначают в качестве адъювантной терапии, направленной на профилактику рецидива заболевания. В рамках рандомизированного исследования Lewis и соавт. при раке эндометрия (РЭ) применяли медроксипрогестерона ацетат (МПА) или плацебо в послеоперационный период. В обеих группах 4-летняя выживаемость была одинаковой. Kauppila и соавт., описав более 1100 больных раком эндометрия (РЭ), получавших адъювантную терапию прогестинами в течение 2 лет после операции и ЛТ, обнаружили, что рецидивы возникали даже при высокодифференцированных аденокарциномах I стадии; по их мнению, профилактическое применение прогестинов у этих пациенток было неэффективным. В проспективном исследовании DePalo и соавт. не обнаружили разницы в выживаемости 363 больных раком эндометрия (РЭ) I стадии, получавших МПА в течение 12 мес, и 383 пациенток с той же стадией, которые не получали этот препарат. По данным британского исследования, в котором 429 пациенток с I и II стадиями рака эндометрия (РЭ) были рандомизированы для послеоперационной терапии МПА или наблюдения, разницы в показателях выживаемости через 5 лет выявлено не было. Прогестины применяют более 30 лет; чувствительность рецидивных опухолей рака эндометрия (РЭ) к этим гормонам доказана. Имеющиеся данные свидетельствуют о том, что приблизительно 1/3 всех больных с рецидивами рака эндометрия (РЭ) реагирует на гормональную терапию, причем частота ответов при высокодифференцированных аденокарциномах значительно выше, чем при умеренно и низкодифференцированных. Эксперты GOG назначали МПА по 50 мг 3 раза в сутки 420 больным с выраженными стадиями или рецидивами рака эндометрия (РЭ). Из 219 пациенток с объективно измеряемыми опухолями было всего 17 (8%) с полным ответом на терапию и 13 (6 %) — с частичным. Более чем у 1/2 пациенток заболевание оставалось стабильным, а у 1/3 — прогрессировало. Медиана выживаемости составила 10,5 мес. При высокодифференцированных аденокарциномах частота ответов на терапию прогестинами выше, чем при низкодифференцированных. GOG в рамках рандомизированного клинического исследования III фазы провела сравнительную оценку эффективности МПА в дозе 1000 и 200 мг/сут у 300 пациенток. Различий между показателями ответа на лечение и выживаемостью между двумя терапевтическими группами не отмечено. Lentz сообщил о другом клиническом исследовании GOG, в котором больным с распространенным или рецидивным раком эндометрия (РЭ) назначали высокие дозы (800 мг/сут) мегестрола ацетата. Из 58 пациенток прореагировали на лечение 13 (24%); у 6 (11 %) пациенток ответ был частичным, причем в 4 случаях он длился более 18 мес. и наблюдался при умеренно и высокодифференцированных аденокарциномах. Позднее стали определять специфические ЭР и ПР в клетках злокачественных опухолей матки. Нет сомнений в наличии этих рецепторов, но их концентрация варьирует в различных опухолях. В высокодифференцированных опухолях по сравнению с низкодифференцированными содержится больше как ЭР, так и ПР. В небольшой группе пациенток было установлено, что примерно в 1/3 рецидивных опухолей содержались ЭР и ПР. Следовательно, рецепторный статус опухоли может коррелировать с клиническими данными чувствительности к прогестерону у больных с рецидивным раком эндометрия (РЭ). Предварительные результаты весьма убедительно свидетельствуют об этом. Очевидно, что для подтверждения этих данных необходимо получить дополнительную информацию; во всяком случае, перспективы в этом направлении весьма обнадеживающие. Если подтвердится прямая корреляция, то анализ рецепторного статуса опухоли позволит подбирать ту или иную схему гормональной или химиотерапии при рецидивах рака эндометрия (РЭ). Если результат анализа на наличие ЭР и ПР положительный, то у пациентки хорошие шансы на достижение ремиссии при лечении прогестинами, даже если у нее низкодифференцированная опухоль. С другой стороны, при отрицательных результатах ответ на терапию прогестинами может оказаться настолько низким, что проведение XT сэкономит время и будет более эффективным. Kauppila, анализируя данные 5 исследований, описанных в литературе, подсчитал, что 89% опухолей с ПР проявили чувствительность к гормональной терапии по сравнению с чувствительностью всего лишь 17 % у опухолей, не содержащих эти рецепторы. По данным GOG, 4 (40%) из 10 опухолей, имеющих ЭР и ПР, реагировали на проводившуюся терапию прогестинами по сравнению с 5 (12%) из 41 опухоли без ПР. Терапию прогестинами можно проводить несколькими способами. Мы предпочитаем использовать МПА (Депо-Провера) по 400 мг в/м с недельным интервалом. Другие рекомендуемые прогестины: пероральный МПА (Провера) 150 мг/сут и мегестрола ацетат (Мегейс) 160 мг/сут. Если достигнут объективный ответ, терапию прогестинами продолжают неопределенно долго. При прогрессировании заболевания прогестины отменяют и назначают XT. detector |