Бесплатная консультация по лечению в Москве.
Звоните 8 (800) 350-85-60 или заполните форму ниже:
Химиотерапия при раке эндометрия является одной из методик лечения онкообразования. Перед началом сеансов врач занимается подбором противоопухолевых препаратов, список которых в каждом случае индивидуален. Прием цитостатиков может быть как самостоятельным вариантом противораковой терапии, так и выполняться после резекции матки.

Если вам или вашим близким нужна медпомощь, свяжитесь с нами. Специалисты сайта посоветуют клинику, в которой вы сможете получить эффективное лечение:
Виды и схемы лечения химиотерапией при раке эндометрия вариабельны и зависят от разновидности онкообразования, особенностей организма пациентки и истории развития патологии.
Могут применяться следующие разновидности химиотерапевтического воздействия:
- • монохимиотерапия — применение одного противоопухолевого препарата;
- • полихимиотерапия — применение нескольких медикаментов одновременно либо последовательно.
В современной онкопрактике используется также:
- • адьювантная — проводится после гистэроктомии;
- • неоадьювантная — назначается до операции.
Медикаментозная схема зависит от стадии рака и текущего диагноза. Химиотерапевтический протокол содержит различные комбинации противоопухолевых препаратов.
Противопоказания
Каких-либо специфических противопоказаний к выполнению химиотерапии при раке эндометрия нет. Методика не может использоваться при обнаружении следующих состояний:
- • Нарушение функций почечной и печеночной систем. Лекарства могут спровоцировать серьезную недостаточность.
- • Болезни крови. Химиопрепараты будет запрещены при выявлении отклонений в составе крови.
- • Желчнокаменная патология.
- • Заболевания сердца.
- • Тяжело протекающая астма.
От применения цитостатиков потребуется отказаться при выраженном истощении, когда масса тела не превышает 40 кг.
Подготовка
О том, как проходит подготовка к химиотерапии при раке эндометрия, пациенту рассказывает ведущий заболевание онкотерапевт.
Мероприятия не зависят от выбранной схемы: они стандартны и направлены на уменьшение неприятных состояний. Рекомендации простые:
- • человек должен питаться правильно, отказавшись от вредной пищи;
- • необходимо отказаться от курения и употребления алкоголя;
- • днем требуется выпивать как можно больше чистой воды;
- • необходима посильная физическая нагрузка;
- • требуется соблюдать режим дня, чередуя периоды сна и бодрствования: организму нужно полноценно отдыхать.
Для укрепления иммунной защиты назначается прием иммуномодулирующих медикаментов.
Также женщине назначается медицинское обследование, в частности, расширенный биохимический анализ крови. Ориентируясь на полученные результаты, онколог сможет контролировать процесс химиолечения и при необходимости изменять дозировки лекарств.
Как делают (проводят) химиотерапию при раке эндометрия
Формат химиолечения индивидуален. Современное клиническое оборудование позволяет выполнять продолжительные по времени инфузии, не ограничивая возможности передвижения человека. После завершения курса больная возвращается домой.
В случае непродолжительного сеанса приема цитостатиков — 3-4 часа — он проводится в условиях пребывания в дневном стационаре.
Последствия и побочные эффекты при химиотерапии рака эндометрия
Главный недостаток химиолечения — возникновение побочной симптоматики. Развитие неприятного, а иногда тяжелого ответа организма обусловлено негативным воздействием цитостатиков на все клетки организма. Стоит отметить, что побочные эффекты развиваются не во всех случаях либо проявляется не столь интенсивно. Все зависит от особенностей организма женщины.
Чаще всего после химиотерапии при раке эндометрия развиваются следующие состояния:
- • временное снижение числа лейкоцитов и понижение иммунной защиты;
- • нарушение процессов продуцирования эритроцитов и следующая за ним анемия;
- • снижение показателя тромбоцитов, проявляющееся склонностью к появлению внезапных синяков и кровоподтеков;
- • воспаление слизистых рта (язвенный стоматит) и раздражения ЖКТ;
- • диспепсические расстройства — тошнота, рвота, диарея;
- • нарушение репродуктивной функции (чаще всего обратимо).
Реабилитация
Реабилитация после химиотерапии при раке эндометрия помогает женщине восстановиться и подготовиться к следующему курсу. В этот период очень важно правильно питаться. В меню должны обязательно присутствовать следующие группы продуктов:
- • овощи и фрукты;
- • мясо, рыба — они являются источниками белка;
- • морепродукты;
- • хлеб, каши, картофель, макароны;
- • молочная продукция — главный поставщик кальция.
Необходимы ежедневные прогулки и посильная физическая нагрузка. Требуется много отдыхать, не позволяя себе переутомляться.

Сколько стоит химиотерапия при раке эндометрия
На стоимость курса химиотерапии при раке эндометрия в клиниках и медцентрах Москвы влияют многие показатели, в частности цены используемых цитостатических средств и статус учреждения.

Лечение рака эндометрия в Израиле
Лечение рака эндометрия в Израиле — это комплекс медицинских манипуляций, направленных на верификацию диагноза, избавление от.

Лечение рака эндометрия
Лечение рака эндометрия — это комплекс консервативных и хирургических мероприятий, которые направлены на удаление онкоопухоли и.

Рак эндометрия — это злокачественное новообразование, происходящее из внутреннего слоя матки. В ряде других онкопроцессов.

Облучение при раке эндометрия
Лучевая терапия при раке эндометрия — терапевтическое мероприятие, цель которого — купирование атипичного процесса: первичного и.
Бесплатная консультация по лечению в Москве.
Звоните 8 (800) 350-85-60 или заполните форму ниже:
При диагностированном раке эндометрия химиотерапия может проводится до операции и после нее. Обычно к приему химиопрепаратов до хирургического вмешательства прибегают, если опухоль является неоперабельной.
Химиотерапия проводится для уменьшения размеров опухоли и получения возможности проведения операции. Во многих случаях прием химиопрепаратов комбинируется с лучевым облучением. Такой подход дает более ощутимый результат, новообразование уменьшается в размерах и становится операбельным. Самостоятельно химиотерапия проводится, если рак рецидивировал после выполненного ранее хирургического лечения. Также прием химиопрепаратов назначается при обнаружении в организме метастазов.
После хирургического вмешательства химиотерапия проводится для предотвращения рецидива болезни. Это обязательная мера для пациенток, у которых диагностирован рак эндометрия третьей и четвертой стадий. Также прием химиопрепаратов назначается женщинам с первой стадией светлоклеточного и серозного рака.
Чаще всего химиопрепараты вводятся внутривенно. Наиболее эффективными препаратами являются Паклитаксел, Доксорубицин, Цисплатин, Карбоплатин. Они могут применяться как самостоятельно, так и комбинироваться друг с другом. Препараты имеют побочные эффекты, поэтому их подбор должен осуществляться исключительно специалистом и с учетом состояния здоровья пациентки.
В зарубежных клиниках применяют новейшие протоколы химиотерапии, подбирают подходящую схему для любого случая. Ведущие специалисты в этом направлении — профессора Моше Инбар и Эльке Йегер.











Химиотерапия рака эндометрия
В статье приведен обзор актуальной литературы по проблеме химиотерапии рака эндометрия (РЭ). Анализированы имеющиеся данные относительно применения адъювантной химиотерапии при комбинированном лечении РЭ, демонстрирующие ее эффективность в сочетании с лучевой терапией при РЭ I–III стадий и высоком риске рецидива заболевания. Приведены последние рекомендации ESMO, ESGO, ESTRO, NCCN и RUSSCO по адъювантной, системной и паллиативной химио-
терапии РЭ.
Рак эндометрия (РЭ) – наиболее распространенная локализация гинекологического рака и занимает 3–4-е места среди всех злокачественных новообразований у женщин в экономически развитых странах, в т.ч. и в России [1]. При этом РЭ является наиболее благоприятной локализацией гинекологического рака по уровню показателя 5-летней наблюдаемой выживаемости. Так, по данным популяционного ракового регистра Санкт-Петербурга и Национального ракового института США, общая 5-летняя выживаемость больных РЭ при I стадии в первом десятилетии нашего века превышает 90% [2, 3]. Такие показатели при I стадии РЭ достигаются при использовании радикального хирургического лечения. Тем не менее общая наблюдаемая и относительная 5-летняя выживаемость независимо от стадии сохраняется на уровне 70% [2, 3]. Таким образом, не менее 30% больных РЭ умирают в течение 5-летнего периода наблюдения от рецидивов и метастазов, что определяет актуальность комплексного подхода к лечению заболевания. По данным FIGO (International Federation of Gynecology and Obstetrics), более 60% больных раком тела матки (РТМ) подвергаются различным видам адъювантного лечения даже при ранних стадиях заболевания [4, 5].
Согласно данным проспективных рандомизированных исследований, адъювантное лечение показано больным РТМ с неблагоприятными факторами прогноза, у которых повышен риск развития рецидива заболевания [6, 7]. Пациентки, относящиеся к группе риска развития рецидива заболевания, определяются на основе клинико-морфологических прогностических факторов [8]. К доказанным клинико-морфологическим факторам прогноза относятся возраст, стадия заболевания, глубина инвазии в миометрий, дифференцировка и гистологический тип опухоли. Раньше к низкому риску относили случаи только высокодифференцированной эндометриоидной аденокарциномы стадии I и поверхностной инвазии или умереннодифференцированные без инвазии, а к высокому риску при стадии I – низкодифференцированные с глубокой инвазией. Позже проспективные исследования, посвященные роли лучевой терапии при РТМ (PORTEC-1, GOG99, ASTEC/EN5), модифицировали эту классификацию и определили следующие группы риска для назначения адъювантной лучевой терапии, а именно группу низкого, промежуточного, высокого промежуточного и высокого рисков [9–11]. Помимо этого показано, что некоторые молекулярные факторы (р53, L1CAM, MMR-D) также имеют прогностическое значение, но окончательно их роль не определена и в настоящее время они не применяются в клинической практике [12–14].
На основании трех проспективных рандомизированных исследований (ASTEC/EN5, PORTEC-1, GOG99) и мета-анализа Kong показано, что применение адъювантной терапии при низком риске РЭ (I стадия, G1-2, глубина инвазии 50% и стадия III) после операции были рандомизированы в зависимости от вида адъювантной терапии: химиотерапия по схеме CAP (цисплатин 50 мг/м2, доксорубицин 45 мг/м2, циклофосфамид 600 мг/м2) каждые 28 дней в течение пяти циклов или дистанционная лучевая терапия на малый таз (суммарная общая доза 45–50 Гр). Не обнаружено статистически значимых различий в 3-, 5- и 7-летней общей выживаемости (рис. 1). Аналогичное исследование с аналогичными результатами было проведено в 2008 г. японской группой JGOG (Japan Gynecologic Oncology Group) [21].
В 2004 г. американская группа Radiation Therapy Oncology Group 9905 представила первые обнадеживающие результаты применения комбинированной адъювантной терапии: дистанционная лучевая терапия на малый таз и два цикла цисплатина (50 мг/м2 в дни 1 и 28), за которым следовали 4 дополнительных курса с 28-дневными интервалами цисплатина (50 мг/м2) и паклитаксела (175 мг/м2) в виде 24-часового вливания [22]. Исследование было проведено с участием 46 больных эндометриальной карциномой I–III стадий, G 2, 3, с инвазией миометрия >50%. В результате 4-летняя общая выживаемость составила 85% для всей группы и 77% – для пациенток с III стадией, а безрецидивная выживаемость составила 77 и 72% соответственно. У пациенток со стадиями IC, IIA или IIB рецидивов не наблюдалось [23].
В 2010 г. были опубликованы результаты комбинированного анализа двух рандомизированных исследований (NSGO 9501/EORTC 55991 и Mango-ILIADE III) [24]. Как показал анализ, добавление адъювантной химиотерапии (4 цикла химиотерапии на основе платины либо до, либо после адъювантной дистанционной лучевой терапии) привело к значительному повышению 5-летней беспрогрессивной выживаемости (78 против 69%; р=0,009, рис. 2), а также обнаружена тенденция к повышению общей выживаемости (82 против 75%; р=0,07, рис. 3).
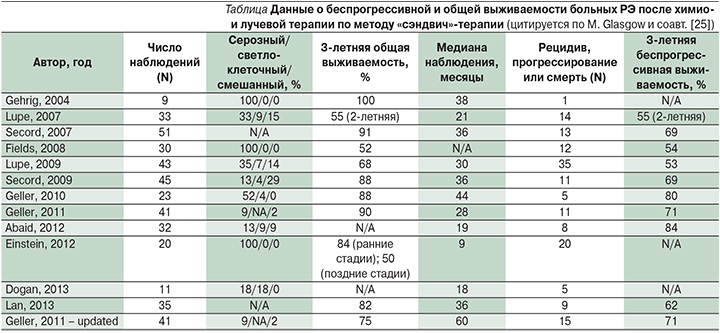
Анализ подгрупп по гистологическим типам рака эндометрия показал, что преимущество адъювантной химиотерапии было ограничено в отношении пациенток с эндометриоидными опухолями, тогда как при серозных и светлоклеточных опухолях выживаемость не превысила 36% [24].
Согласно консенсусу ESMO, ESGO, ESTRO (2016) [15] и рекомендациям NCCN (National Comprehensive Cancer Network, 2017) [28], больным РТМ IVA–IVB-стадий на первом этапе предлагается хирургическое стадирование и циторедуктивная операция, после которых проводится системная химиотерапия. Выбор между гормональной и химиотерапией зависит от нескольких факторов, в т.ч. гистологических и клинических параметров, от индивидуальных особенностей пациентки. При местных вагинальных рецидивах или рецидивах в тазовых лимфатических узлах рекомендуется применение химиотерапии с лучевой терапией [15]. При большем распространении опухоли рекомендовано применение системной химиотерапии перед лучевой терапией [15].
Схемы химиотерапии, применяемые при системном лечении распространенного РЭ, приведены в рекомендациях NCCN (2017) [28] и RUSSCO (Российское общество клинической онкологии) [29]. Для монотерапии РТМ применяют следующие препараты: цисплатин, карбоплатин, доксорубицин, липосомальный доксорубицин, паклитаксел, топотекан. Для полихимиотерапии рекомендованы следующие схемы: цисплатин/паклитаксел, цисплатин/доксорубицин, цисплатин/доксорубицин/паклитаксел, карбоплатин/доцетаксел.
Согласно консенсусу ESMO, ESGO, ESTRO (2016) [15], стандартом паллиативной терапии РТМ является 6 циклов карбоплатина с паклитакселом с 3-недельным интервалом, что основано на рандомизированном исследовании, показавшем одинаковую эффективность со схемой цисплатин/доксорубицин/паклитаксел при меньшей токсичности.
Что касается химиотерапии второй линии при прогрессировании РЭ после химиотерапии первой линии, то она значительно ограничена в большинстве случаев в связи с развитием резистентности опухоли к химиотерапевтическим препаратам. В проводившихся нерандомизированных исследованиях не получено доказательств, подтверждающих эффективность использования химиотерапии второй линии после того, как платиносодержащая терапия пациенток с РТМ перестала быть эффективной [30, 31].
Приведенные данные свидетельствуют о том, что химиотерапия в сочетании с лучевой терапией является эффективным методом адъювантного лечения РЭ при высоком риске рецидива заболевания, поздних стадиях РЭ и при рецидивах заболевания.
1. Злокачественные новообразования в России в 2015 году (заболеваемость и смертность) / Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М., 2017. 250 с.
2. Злокачественные новообразования в Санкт-Петербурге и других административных территориях Северо-Западного федерального округа России (заболеваемость, смертность, контингенты, выживаемость, больных). Экспресс-информация. Второй выпуск / Под ред. А.М. Беляева, Г.М. Манихаса, В.М. Мерабишвили. СПб., 2016. 208 с.
4. Нечушкина В.М., Морхов К.Ю., Кузнецов В.В. Комбинированное лечение рака тела матки ранних стадий. Cиб. онкол. журн. 2013;3(57).
5. Creasman W.T., Odicino F., Maisonneuve P., Quinn M.A., Beller U., Benedet J.L., Heintz A.P., Ngan H.Y., Pecorelli S. Carcinoma of the Corpus Uteri. Int. J. Gynaecol. Obstet. 2006;95(Suppl. 1):105–44.
6. Blake P., Swart A.M., Orton J., Kitchener H., Whelan T., Lukka H., Eisenhauer E., Bacon M., Tu D., Parmar M.K., Amos C., Murray C., Qian W. Adjuvant external beam radiotherapy in the treatment of endometrial cancer (MRC ASTEC and NCIC CTG EN.5 randomised trials): pooled trial results, systematic review, and meta-analysis. Lancet. 2009;373:137–46.
7. Kong A., Johnson N., Kitchener H.C., Lawrie T.A. Adjuvant radiotherapy for stage I endometrial cancer: an updated Cochrane systematic review and meta-analysis. J. Natl. Cancer Inst. 2012;104:1625–34.
8. Bendifallah S., Canlorbe G., Raimond E., Hudry D., Coutant C., Graesslin O., Touboul C., Huguet F., Cortez A., Daraï E., Ballester M. A clue towards improving the European Society of Medical Oncology risk group classification in apparent early stage endometrial cancer? Impact of lymphovascular space invasion. Br. J. Cancer. 2014;110:2640–46.
9. Keys H.M., Roberts J.A., Brunetto V.L., Zaino R.J., Spirtos N.M., Bloss J.D., Pearlman A., Maiman M.A., Bell J.G. A phase III trial of surgery with or without adjunctive external pelvic radiation herapy in intermediate risk endometrial adenocarcinoma: a Gynecologic Oncology Group study. Gynecol. Oncol. 2004;92:744–51.
10. Blake P., Swart A.M., Orton J., et al. Adjuvant external beam radiotherapy in the treatment of endometrial cancer (MRC ASTEC and NCIC CTG EN.5 randomised trials): pooled trial results, systematic review, and meta-analysis. Lancet. 2009;373:137–46.
11. Bosse T., Peters E.E., Creutzberg C.L., Jürgenliemk-Schulz I.M., Jobsen J.J., Mens J.W., Lutgens L.C., van der Steen-Banasik E.M., Smit V.T., Nout R.A. Substantial lymph-vascular space invasion (LVSI) is a significant risk factor for recurrence in endometrial cancer-apooled analysis of PORTEC 1 and 2 trials. Eur. J. Cancer. 2015;51:1742–50.
12. Soong R., Knowles S., Williams K.E., Hammond I.G., Wysocki S.J., Iacopetta B.J. Overexpression of p53 protein is an independent prognostic indicator in human endometrial carcinoma. Br. J. Cancer. 1996;74:562–67.
13. Zeimet A.G., Reimer D., Huszar M., et al. L1CAM in early-stage type I endometrial cancer: results of a large multicenter evaluation. J. Natl. Cancer Inst. 2013;105.
14. Talhouk A., McAlpine J.N. New classification of endometrial cancers: the development and potential applications of genomic-based classification in research and clinical care. Gynecol. Oncol. Res. Pract. 2016;3:14. doi: 10.1186/s40661-016-0035-4.
15. Colombo N., Creutzberg C., Amant F., Bosse T., González-Martín A., Ledermann J., Marth C., Nout R., Querleu D., Mirza M.R., Sessa C. ESMO-ESGO-ESTRO Consensus Conferenc on Endometrial Cancer: diagnosis, treatment and follow-up. Ann. Oncol. 2016;27:16–41.
16. Fleming G.F., Brunetto V.L., Cella D., et al. Phase III trial of doxorubicin plus cisplatin with or without paclitaxel plus filgrastim in advanced endometrial carcinoma: a Gynecologic Oncology Group Study. J. Clin. Oncol. 2004;22:2159–66.
17. Miller D., Filiaci V., Fleming G., et al. Late-Breaking Abstract 1: randomized phase III noninferiority trial of first line chemotherapy for metastatic or recurrent endometrial carcinoma: a Gynecologic Oncology Group study. Gynecol. Oncol. 2012;125:771.
18. McMeekin D.S., Filiaci V.L., Aghajanian C., et al. A randomized phase III trial of pelvic radiation therapy (PXRT) versus vaginal cuff brachytherapy followed by paclitaxel/ carboplatin chemotherapy (VCB/C) in patients with high risk (HR), early stage endometrial cancer (EC): a Gynecologic Oncology Group trial. Gynecol. Oncol. 2014;134:438 (Аbstr. LBA 431).
19. Morrow C.P., Bundy B.N., Homesley H.D., Creasman W.T., Hornback N.B., Kurman R., Thigpen J.T. Doxorubicin as an adjuvant following surgery and radiation therapy in patients with high-risk endometrial carcinoma, stage I and occult stage II: a Gynecologic Oncology Group Study. Gynecol. Oncol. 1990;36:166–71.
20. Maggi R., Lissoni A., Spina F., Melpignano M., Zola P., Favalli G., Colombo A., Fossati R. Adjuvant chemotherapy vs radiotherapy in high-risk endometrial carcinoma: results of a randomised trial. Br. J. Cancer. 2006;95:266–71.
21. Susumu N., Sagae S., Udagawa Y., Niwa K., Kuramoto H., Satoh S., Kudo R. Randomized phase III trial of pelvic radiotherapy versus cisplatin-based combined chemotherapy in patients with intermediate- and high-risk endometrial cancer: a Japanese Gynecologic Oncology Group study. Gynecol. Oncol. 2008;108:226–33.
22. Greven K., Winter K., Underhill K., Fontenesci J., Cooper J., Burke T. Preliminary analysis of RTOG 9708: Adjuvant postoperative radiotherapy combined with cisplatin/paclitaxel chemotherapy after surgery for patients with high-risk endometrial cancer. Int. J. Radiat. Oncol. Biol. Phys. 2004;59(1):168–73.
23. Greven K., Winter K., Underhill K., Fontenesci J., Cooper J., Burke T. Final analysis of RTOG 9708: adjuvant postoperative irradiation combined with cisplatin/paclitaxel chemotherapy following surgery for patients with high-risk endometrial cancer. Gynecol. Oncol. 2006;103:155–59.
24. Hogberg T., Signorelli M., de Oliveira C.F., et al. Sequential adjuvant chemotherapy and radiotherapy in endometrial cancer—results from two randomised studies. Eur. J. Cancer. 2010;46:2422–31.
26. Glasgow M., Vogel R.I., Burgart J., Argenta P., Dusenbery K., Geller M.A. Long term follow-up of a phase II trial of multimodal therapy given in a “sandwich” method for stage III, IV, and recurrent endometrial cancer. Gynecol. Oncol. Res. Pract. 2016;3:6.
27. De Boer S.M., Powell M.E., Mileshkin L., et al. Toxicity and quality of life after adjuvant chemoradiotherapy versus radiotherapy alone for women with high-risk endometrial cancer (PORTEC-3): an open-label, multicentre, randomised, phase 3 trial. Lancet Oncology. 2016;17:1114–26.
30. Nagao S., Nishio S., Michimae H., Tanabe H., Okada S., Otsuki T., Tanioka M., Fujiwara K., Suzuki M., Kigawa J. Applicability of the concept of “platinum sensitivity” to recurrent endometrial cancer: the SGSG-012/GOTIC-004/ Intergroup study. Gynecol. Oncol. 2013;131:567–73.
Хирургическое лечение рака тела матки
Стандартным хирургическим подходом при 1 стадии рака эндометрия является экстирпация матки с придатками.
Если пациентка находится в группе высокого риска (определяется в зависимости от размера опухоли, гистологического типа, степени злокачественности, глубины прорастания в миометрий), ее лечебная тактика может быть более агрессивной — хирургическое вмешательство с удалением тазовых и парааортальных лимфоузлов. В последние 15 лет всё большее распространение получает лапароскопическая методика выполнения операции при раке матки.
На распространенных стадиях рака эндометрия (3 и 4 стадия) может выполняться циторедуктивная операция в случае хорошего общего состояния пациентки, с последующим проведением одного из дополнительных специализированных методов лечения: лучевой терапии или химиотерапии. Это так называемое комбинированное лечение рака эндометрия.
Лучевая терапия при раке тела матки
Уварова Светлана Николаевна
Главный врач, онколог-химиотерапевт, врач высшей категории, врач паллиативной медицины
Базылев Андрей Сергеевич
Онколог-химиотерапевт, врач паллиативной медицины
Тверезовская Ирина Александровна
Онколог-химиотерапевт, врач высшей категории, врач паллиативной медицины
Буйнякова Анна Игоревна
Онколог-химиотерапевт, к.м.н., врач высшей категории, врач паллиативной медицины
Баженова Елена Анатольевна
Кардиолог, терапевт, к.м.н., врач высшей категории
Химиотерапия рака матки
Если пациентка находится в группе высокого риска, то химиотерапия при раке тела матки применяется комплексно, в дополнение к операции и лучевой терапии. Согласно результатам нескольких рандомизированных исследований, комбинированное лечение (последовательное применение послеоперационной лучевой и химиотерапии) позволяет снизить риск возникновения рецидива рака эндометрия на 36%.
Химиотерапия также применяется при лечении метастатического рака тела матки. В химиотерапии рака эндометрия мы используем наиболее эффективные комбинации препаратов, включая производные платины (Цисплатин, Карбоплатин) с Паклитакселом (Таксол), Доцетакселом (Таксотер), Доксорубицином, также в монорежиме проводим химиотерапию рака тела матки липосомальным Доксорубицином (Келикс) или Топотеканом, при карциносаркоме – комбинации с Ифосфамидом.
Таргетная терапия рака тела матки
- В лечении рака эндометрия получены данные о значительном увеличении выживаемости до прогрессирования при добавлении таргетной терапии препаратом Бевацизумаб(Авастин) к комбинации Карбоплатин/Паклитаксел.
- При раке тела матки в опухолевых клетках часто наблюдается активация определённого сигнального пути регуляции клеточного деления (PI3K/Akt/mTOR). В клинических исследованиях достигнуты первые положительные результаты таргетной терапии рака эндометрия препаратами из группы mTOR ингибиторов, подавляющих сигнал к делению клеток в опухоли.
- Согласно рекомендациям NCCN препарат Темсиролимус (Торизел) может быть применён при возникновении рецидива рака тела матки с метастазами после прогрессии на фоне химиотерапии.
В настоящее время исследуется комбинация Летрозола и Эверолимуса, получены обнадёживающие предварительные результаты.
В клиническом исследовании 2-й фазы продемонстрирована эффективность монотерапии препаратом Ридафоролимус у пациенток с раком тела матки, в том числе после предшествующих 2-х линий химиотерапии.
За последние 10 лет в онкологии произошли значительные изменения – лекарственное лечение вышло на качественно новый уровень. Разработаны и внедрены в клиническую практику инновационные препараты, которые позволяют нам уверенно говорить о том, что рак сегодня – это не приговор, это диагноз.
Уварова Светлана Николаевна
Главный врач, онколог-химиотерапевт, врач высшей категории, врач паллиативной медицины
