При раке молочной железы собственные гормоны и лекарства могут конкурировать за право воздействия на опухолевую клетку, поэтому необходимо понижение уровня продуцируемых половых гормонов.
У женщин детородного возраста 60% гормонов производится в яичниках, 40% — в жировой ткани. Поскольку за продукцию гормонов в большей мере ответственны яичники, именно на них воздействуют несколькими способами: удалением самого органа или прекращением его функции.
- хирургической кастрацией — удаление яичников;
- лекарственной кастрацией — введение лекарства для прекращения продукции гормонов гипофиза, которые воздействуя на яичники, стимулируют выработку стероидов;
- лучевой кастрацией — облучение яичников.
На практике выключение функции яичников тем или иным способом производится не только менструирующим женщинам, но и в течение 2-х лет после менопаузы – в этот период уровень половых гормонов ещё достаточно высок.
Разберёмся со способами кастраций. Самый основательный – хирургическое удаление яичников, после него уровень половых гормонов безвозвратно снижается, чего не скажешь про другие способы. Удаление яичников или овариэктомия в настоящее время почти повсеместно проводится эндоскопически (лапароскопия). Малая травматизация, быстрое послеоперационное восстановление, отсутствие больших рубцов.
Противопоказаниями к эндоскопической (лапароскопической) овариэктомии являются: предшествующие вмешательства на органах малого таза (операции по поводу кист, внематочной беременности и пр.), перитонит в прошлом, тяжёлые воспалительные заболевания половой сферы, то есть состояния, приводящие к образованию спаек. Противопоказания эти относительны, то есть лапароскопию можно сделать, но вот найти и удалить оба яичника чрезвычайно трудно, а иногда и невозможно.
Если есть указания на миому матки или гиперплазию эндометрия, то необходимо удаление не только яичников, но и матки. Кстати, парадокс: российские мужчины не считают изъяном отсутствие у женщины одного или обоих яичников, но почему-то женщина с удалённой маткой многими воспринимается как неполноценная. Матка всего лишь вместилище для плода и нужна только для вынашивания ребенка один-три раза за всю жизнь.
Следующий способ выключения функции яичников – лекарственная кастрация. В соответствии с продолжительностью менструального цикла, один раз в 28 дней, вводится препарат – релизинг-гормон, который подавляет продукцию гонадотропного гормона гипофиза.
Этим прерывается связь между гипофизом и яичниками. Гипофиз не требует выброса половых стероидов, яичники их и не производят. Лекарство в виде маленькой капсулы, вводимой специальным шприцем, рассасывается в жировой ткани передней брюшной стенки 28 дней. Сейчас есть трёхмесячная форма препарата.
У некоторых женщин, вступивших в климактерий, есть возможность окончательного подавления стероидогенеза, у большинства — половые гормоны не производятся покуда действует препарат. Стандартно при профилактической терапии релизинг-гормон вводится не менее 2-х лет. А дальше? Гарантировано ли после окончания профилактики сохранение стероидных гормонов на низком уровне? Врать не стану – нет. Восстановление функции яичников тем вероятнее, чем моложе женщина.
Аргументация хирурга понятна, женщина на данный момент считается излеченной, подвергать её риску операционных осложнений, которые могут нанести вред здоровью или жизни, не совсем разумно. Вновь начинать инъекции релизинг-гормона? Но ведь признаков опухоли нет? Нужно ли это? Насколько опасно восстановление функции яичников? Сколько лет вести терапию и будет ли это достаточно для окончательного подавления яичников, никто не скажет. Вопросов много, ответа нет.
Когда выполняется кастрация? Стандартов нет. Хирургическую, как правило, выполняют одновременно с операцией на молочной железе. Лекарственное выключение функции яичников может начинаться вместе с химиотерапией или откладывается на последний этап – после окончания курсов профилактики. Химиотерапия у большой части женщин вызывает аменорею.
Аменорея – отсутствие менструаций в течение 6 месяцев. Вероятность развития аменореи тем выше, чем ближе естественная менопауза. Но и вступление в климактерический период, который начинается с 45 лет, не гарантирует того, что необратимо снизится продукция половых гормонов, и функция яичников после периода постхимиотерапевтической аменореи не восстановится, поэтому лекарственная аменорея не исключает кастрацию. Лучевая кастрация может быть на любом этапе, но удобнее это сделать во время послеоперационной лучевой терапии.
Онколог, кандидат медицинских наук,
Мещерякова Наталья Георгиевна

К сожалению, существующие методики, позволяющие однократно вывести яичники из зоны облучения могут привести к необратимым изменениям в них, в результате возможного перегиба питающей ножки.
Нами была предложена хирургическая методика временного выведения яичников из зоны облучения на втором этапе лечения, позволяющая после окончания лучевой терапии вернуть сохраненные интраоперационно яичники в предварительно созданное ложе, способствующее достаточному кровоснабжению и, как следствие, адекватному функционированию гонад [9].
Остается дискутабельным вопрос о сроках полноценной овариальной функции после удаления матки. По данным одних авторов яичники прекращают свою работу в ближайшее время после гистерэктомии [1], другие исследования говорят в пользу многолетнего функционирования яичников соответственно возрасту [3, 7].
Таким образом, принимая во внимание тенденцию роста заболеваемости раком шейки матки молодых женщин, актуально провести дополнительное изучение состояния сохраненных яичников спустя более длительный срок.
Цель исследования: изучить функцию половых желез в сроки более 5 лет после проведения комбинированного лечения.
Материалы и методы исследования
Предложенный нами способ мобилизации сохраненных яичников применялся у 176 женщин репродуктивного возраста (от 20 до 45 лет) больных раком шейки матки Ib стадии (гистотип соответствовал плоскоклеточному раку) с 2003 по 2014 годы. На момент оценки результата возрастной промежуток варьировал от 25 до 56 лет. Сроки наблюдения составили от 1-го года до 11 лет. Большинство женщин (130 человек, 74 %) находились в периоде, соответствующему репродуктивному (до 45 лет), из них 104 пациентки (59 %) наблюдались после окончания лечения более 5 лет. Старше 45-ти лет (46–56 лет) было 46 пациенток (26 %), клинически у них было отмечено состояние перименопаузы.
После проведения планового обследования, оценки типа кровоснабжения яичников до операции (преимущественно из яичниковой артерии), пациенткам проводилось комбинированное лечение, включающее расширенную гистерэктомию с фиксацией сохраненных яичников к круглым маточным связкам и последующим выведением половых желез из зоны облучения при проведении дистанционной гамма-терапии на область удаленной опухоли и зону регионарного метастазирования. В работу включались женщины с достаточно длинной круглой маточной связкой, чтобы обеспечить максимально возможное удаление яичников от ромбовидного поля облучения. С целью контроля расположения гонад в брюшной полости при проведении лучевой терапии и для подтверждения их локализации в малом тазу после лечения, все яичники интраоперационно помечались рентгенконтрастными танталовыми скрепками. С помощью обзорной рентгенографии на аппарате PHILIPS BV PULSERA выполнялась визуализация яичников. Облучение осуществлялось в статическом режиме на аппарате АГАТ-С, с двух диаметральных ромбовидных полей – надлобкового и ягодично-крестцового, размерами 13х13 см. Ежедневное фракционирование разовой дозы составило 2 Гр., суммарная очаговая доза варьировала в пределах 40–46 Гр.
Результаты исследования и их обсуждение
Операция заключалась в осуществлении расширенной гистерэктомии с трубами; выкраивания тканевого стебля из воронко – тазовой связки, содержащего сосуды, питающие яичник, и выделении максимальной длины круглой маточной связки, из которой формировалось ложе для оставленных яичников. С этой целью круглая маточная связка натягивалась, ее брюшина Т-образно надсекалась и разворачивалась. Следующим этапом сохраненный яичник укладывался в подготовленное ложе. Для этого культя собственной связки яичника подшивалась к брюшине круглой маточной связки в дистальной части разреза и помечалась танталовыми скрепками. Далее, несколькими швами, яичник фиксировался к развернутым краям брюшины круглой маточной связки. Аналогичные манипуляции выполнялись на втором яичнике. На конце круглых маточных связок фиксировались две мерсиленовые нити, проведенные через тонкие силиконовые катетеры, выведенные на кожу (дистально через круглую маточную связку, проксимально в области подреберья). Перед проведением лучевой терапии подтягиванием верхней лигатуры яичники выводились из зоны облучения. Их расположение контролировалось рентгенологически.
Окончив лучевую терапию, после соответствующей обработки кожи верхние нити натягивались до упора, извлекались катетеры, содержащие нити, последние отсекались на уровне кожи. Далее, натягиванием нижних лигатур, яичники возвращались в малый таз, в положение, имитирующее их связочный аппарат. Затем, проводилось аналогичное удаление нижних нитей с катетерами. После чего, расположение яичников в малом тазу контролировалось с помощью ультрасонографии.
Нашими предыдущими исследованиями [8] было показано, что после проведенного лечения гормональная функция оставленных яичников практически полностью восстанавливается к 12 месяцам наблюдения, сохраняя свою активность, как минимум до 5 лет, таким образом, избавляя женщин от развития климактерического синдрома и связанных с ним вегетоневротических, сердечно-сосудистых и обменно-эндокринных нарушений. Основными гормонами, ответственными за отсутствие посткастрационного синдрома, развивающегося в результате выключения функции яичников, являются эстрогены, выработка которых контролируется фолликулостимулирующим гормоном (ФСГ). Поэтому, для наглядности мы остановились на рассмотрении взаимосвязи этих двух гормонов.
Учитывая фертильный период пациенток на момент операции, нас больше всего интересовало состояние яичников спустя 5 лет после лечения, так как большинство женщин не достигало перименопаузального возраста даже через 10 лет после лечения.
Так, при обследовании наших больных, находящихся в периоде соответствующему среднему репродуктивному, т.е. до 40 лет (111 человек – 63 %) гормональные показатели были стабильны и характерны для этого возраста, в среднем уровень фолликулостимулирующего гормона и эстрадиола (Э2), составил 3,8 МЕ/л и 261 пмоль/л соответственно (таблица). Несмотря на начинающуюся перестройку женского организма и периодические всплески гормонов в поздний репродуктивный период (от 41 до 45 лет – 19 женщин), концентрация гонадотропных и половых гормонов была также в пределах нормы (таблица). При ультрасонографии яичники визуализировались в виде образований овальной формы, средней эхоплотности, однородной структуры без патологических изменений с эхонегативными включениями линейной формы (изображение танталовых скрепок). В этой группе больных специфические менопаузальные симптомы (приливы, потливость, сухость влагалища) никто не предъявлял, хотя треть пациенток были пролечены 7 лет назад.
Уровень половых гормонов у больных РШМ на этапах наблюдения
Преждевременная яичниковая недостаточность (ПЯН) не всегда возникает у пациенток, получавших комбинированное лечение химиотерапевтическими препаратами, независимо от их возраста и типа химиотера-певтических агентов. Большинство молодых женщин с болезнью Ходжкина, лечившихся несколькими химиотерапевтическими препаратами и получавших лучевую терапию на области, исключающие яичники, сохраняли способность к деторождению, хотя их репродуктивные функции и начинали снижаться раньше, чем в контрольной группе.
Есть сообщение о естественном зачатии у молодой женщины с преждевременной яичниковой недостаточностью (ПЯН) после 14 курсов лечения ал-килирующими цитостатиками в комбинации с лучевой терапией на область таза в связи с саркомой Юинга в области таза. Это свидетельствует о трудности прогнозирования вероятности ПЯН после химиотерапии, что в свою очередь затрудняет оценку эффективности лечения, направленного на сохранение функций яичников у таких пациенток.
Сывороточные маркеры поражения яичников. Концентрации ингибина В, АМГ и ФСГ используют как маркеры для определения нарушения функций яичников после проведения химиотерапии, хотя ни один из них нельзя считать идеальным показателем. Ингибин В и АМГ синтезируются зернистыми клетками яичников, ФСГ секретируется в гипофизе, ингибируется эстрадиолом и ингибином В. Повышение содержания ФСГ в сыворотке крови и снижение концентрации ингибина В и АМГ отражают угнетение функций яичников у выживших онкологических больных даже при наличии регулярных менструаций.
Химиотерапия при онкологических заболеваниях связана с транзиторным подавлением ингибина В у девочек в препубертатном возрасте. Следовательно, чувствительные к изменениям показатели концентраций ингибина В и ФСГ — потенциальные маркеры гонадо-токсичного эффекта химиотерапевтических препаратов у девочек в препубертатном периоде.
УЗИ-маркеры поражения яичников. Другим методом определения состояния яичников у таких пациенток служит УЗИ, при котором определяют объем яичников и количество антральных фолликулов. У пациенток, перенесших онкологические заболевания, с нормальными функциями яичников нередко обнаруживают нормальное количество антральных фолликулов, хотя яичники у них часто имеют меньший размер, чем в контрольной группе.
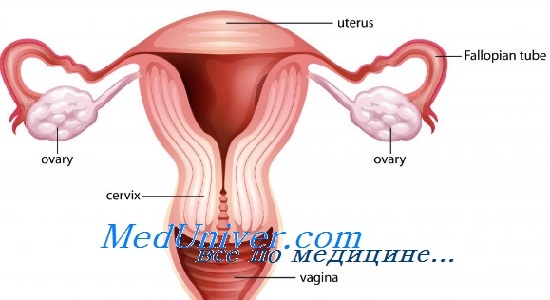
Лучевая терапия области малого таза повреждает как яичники, так и матку. Поражение яичников при лучевой терапии приводит к снижению репродуктивной функции и ПЯН. Поражения матки, вызванные лучевой терапией, проявляются нарушением роста эндометрия и олигоменореей. Это может существенно повлиять на последующие беременности.
При воздействии ионизирующей радиации наиболее уязвимыми оказываются фолликулы яичников ввиду воздействия на ДНК. Лучевая терапия приводит к атрофии яичников и уменьшению запаса фолликулов. В результате воздействия радиации происходит прогрессивное повышение содержания ФСГ и ЛГ и снижение концентрации эстрадиола в течение 4-8 нед после лучевой нагрузки.
На клеточном уровне облучение ооцитов сказывается на состоянии клеток и приводит к стремительно развивающемуся пикнозу, уплотнению хромосом, разрушению ядерной оболочки и вакуолизации цитоплазмы. Необратимость этих повреждений принято объяснять недостаточным количеством зарождающихся стволовых клеток в яичнике.
Однако недавние исследования показали присутствие зарождающихся стволовых клеток в яичниках у взрослых женщин, что доказывает способность ооцитов к восстановлению после окончания химио- или лучевой терапии.
Онкологические больные после лучевой терапии тазовой области или всего туловища относятся к группе повышенного риска по ПЯН. Степень поражения яичников связана с возрастом пациенток и общей дозой облучения яичников. Доза облучения 12 грэй (Гр; 1 рад = 1 сГр) приводила к стойкой яичниковой недостаточности у девочек в препубертатном периоде, в то время как доза всего 2 Гр давала такой же результат у женщин старше 45 лет. Обычно полагают, что однократной дозы от 6,5 до 8,0 Гр достаточно для развития стойкой яичниковой недостаточности у большинства женщин в постпубертатном периоде.
Процент уменьшения запаса примордиальных фолликулов в яичниках при лучевой терапии, направленной на область яичников, зависит от полученной дозы. Считают, что уже сравнительно малая доза облучения (3 Гр) достаточна для поражения 50% всех ооцитов у молодых женщин детородного возраста.
Проведен ряд исследований для определения зависимости поражения яичников от полученной дозы излучения у 90% пациенток в возрасте 15-17 лет. Когда средняя доза радиации, воздействовавшей на яичники, составляла 1,2 Гр, сохранялись функции яичников, тогда как при средней дозе 5,2 Гр функции яичников сохранялись только у 60% пациенток. Истощение яичников развивается практически у всех пациенток при воздействии на область таза облучения в дозах, необходимых для лечения рака шейки матки (85 Гр), рака прямой кишки (45 Гр) или общего облучения всего тела с пересадкой костного мозга (от 8 до 12 Гр на яичники). Если проводят также химиотерапию, доза облучения, вызывающая ПЯН, снижается.
Угнетение функций яичников происходит даже в тех случаях, когда облучение не направлено непосредственно на область яичников. Кратковременная лучевая терапия, направленная на периаортальные лимфатические узлы при лечении болезни Ходжкина, дает рассеянное облучение яичников дозой 1,5 Гр, в ближайшее время функции яичников при этом не нарушаются. Влияние этой дозы на развитие отдаленных по времени нарушений функций яичников остается менее ясным. Важно обсудить с онкологом, будет терапевтическая доза облучения направлена непосредственно на яичники или она будет рассеянной.
| Поиск по форуму |
| Расширенный поиск |
| Найти все сообщения с благодарностями |
| Поиск по дневникам |
| Расширенный поиск |
| К странице. |
Здравствуйте! Помогите советом, пожалуйста.
Мне 30 лет. Год назад закончили ПХТ, затем лучевую по поводу лимфомы Ходжкина. Провели 6 курсов по схеме BEACOPP (довольно токсичной). На 2-ом курсе МЦ резко прекратился. Врач предупредила, что цикл может восстановится до года сам. Во время химии никаких гормонов, защищающих яичники, не принимала — врач не захотел. У многих моих сверстниц после такого же лечения МЦ сам уже восстановился в течение года.
Симптомы климакса беспокоят с самого начала менопаузы: приливы, раздражительность, плохой сон. Менопауза также отразилась и на костях, хоть я и принимаю регулярно хондропротекторы и препараты кальция, недавно неудачно упала и сломала руку.
Коротко анамнез:
В детстве болела гепатитом А; М. с 14 лет, были регулярные, никаких проблем по гинекологии не отмечалось. Не рожала, не была беременна.
Лимфома II cт. диагностирована в 2005 г. Тогда же было проведено полное лечение, но ПХТ была по более легкой схеме, так что даже месячные шли как по часам без задержек и волосы не выпали. Рецидив выявлен в 2008, сразу же проведено лечение. Облучение велось по всем л/у. Спрашивала у радиологов, сказали, что яичники не попали в зону облучения, хотя у меня сомнения на этот счет, т.к. паховые л/у находятся очень близко к ним.
На прошлой неделе сдала анализы:
ФСГ — 65,0
ЛГ — 20,0
Эстрадиол — 5,0
Тестостерон — 0,6
Была на 2-х консультациях у гинекологов. Одна посоветовала принимать 3 месяца Фемостон 2/10, затем сделать УЗИ яичников и повторно анализ на половые гормоны. Другой сказал, что это истощение яичников (искусственный климакс) и посоветовал начать прием Климена.
Меня интересует: 1)могу ли я восстановить репродуктивную функцию и есть ли у меня шансы еще забеременеть и родить здорового ребенка (используя свои яйцеклетки и как вообще определить, остались ли они у меня)? 2)как способствует этому ЗГТ? Где-то в интернете я читала, что функция яичников после ПХТ восстанавливается до 18 мес., в моем случае прошло уже 13 месяцев. 3)Насколько реально восстановить естественный цикл при помощи назначенных препаратов?
