Доктор медицинских наук, профессор Селькова Е.П.
Сегодня человечество переживает эпидемию оппортунистических инфекций, среди которых микозам принадлежит одно из ведущих мест. По данным Всемирной Организации Здравоохранения в последнее десятилетние около 20% населения мира страдает микозами.
Микозы — инфекционные заболевания, этиологическим возбудителем которых являются микробов. Чаще всего микозом болеют люди, имеющие первичные или вторичные иммунодефицитные состояния. Микоз относится к оппортунистическим инфекциям.
Кандидоз — антропонозный микоз, характеризующийся поражением слизистых оболочек и кожи.
Возбудители кандидоза. Поражения у человека вызывают С. albicans (более 90% поражений), С. tropicalis, С. krusei, С. lusitaniae, С. parapsilosis, С. kefyr, С. guilliermondii и др. В начале XX в. кандидозы наблюдали сравнительно редко. С началом применения антибиотиков и по настоящее время заболеваемость кандидозами значительно возросла и продолжает расти. Немаловажное значение в развитии кандидозов имеет неблагоприятная экологическая обстановка, оказывающая отрицательное воздействие на иммунную систему организма человека. Кандидоз обычно возникает эндогенно в результате дисфункций иммунной системы и дисметаболических расстройств организме. В последние годы кандиды являются наиболее распространёнными возбудителями оппортунистических микозов. При поражении организма кандидами возможно развитие тяжёлых висцеральных форм, чаще с вовлечением лёгких и органов пищеварения и других систем организма.
Наиболее часто встречающийся возбудитель микозов С. albicans — нормальный комменсал полости рта, ЖКТ, влагалища и иногда кожи. С. Albicans относятся к условно-патогенным микроорганизмам с высоким уровнем носительства, которое проявляет выраженную тенденцию увеличения: если в 20-е годы оно составляло на слизистой ротовой полости 10%, то в 60 — 70-е годы возросло до 46 — 52%. На слизистой влагалища небеременных женщин носительство иногда достигает 11 — 12,7% и резко увеличивается в последней трети беременности, составляя по данным разных авторов 29,3 — 46 — 86%. В фекалиях частота выделения грибов рода Candida достигает 80%, на неповрежденной коже — до 9,5%. Общий уровень носительства этого вида грибов формируется к 16 — 18-летнему возрасту, оставаясь в дальнейшем без существенных изменений.
Во многих исследованиях показано, что любые нарушения резистентности организма или изменения нормального микробного ценоза могут приводить к развитию заболеванияКандидоза..
Мочеполовой кандидоз передаётся половым путём.
Первичное инфицирование организма человека кандидами происходит при прохождении через родовые пути матери, о чем свидетельствует высокая частота выделения Candida у новорожденных (до 58%), и почти полное совпадение видового состава Candida у ребенка и матери. Инфицированию способствует увеличенная частота носительства и кандидоза влагалища в последней трети беременности. Имеются сведения о передаче грибов рода кандида при кормлении грудью.
Кандидозный вульвовагинит у беременных развивается в 10 — 20 раз чаще, чем в контрольной группе. Предполагают, что беременность является предрасполагающим фактором в развитии кандидоза из-за иммуносупрессивного действия высокого уровня прогестерона и присутствия в сыворотке иммуносупрессивного фактора. Последующая колонизация организма ребенка происходит за счет предметов обихода, рук персонала и пищевых продуктов, в результате чего к концу 1 года почти у 60% детей формируется ГЗТ к антигенам C. albicans.
Новорожденные проявляют высокую чувствительность к экзогенному заражению: у 98,5% инфицированных детей на 5 — 6 день жизни развивается кандидоз ротовой полости. Прогноз заболевания благоприятный, за исключением недоношенных, у которых микоз может приобретать висцеральный и генерализованный характер.
Описан трансплацентарный путь заражения при кандидозе, прогноз которого зависит от степени доношенности: при рождении ребенка после 36 недель беременности заболевание, как правило, протекает в виде легко купируемых поверхностных поражений, а при рождении в более ранние сроки микоз принимает системный характер с высокой летальностью.
Поражение слизистых кандидами обусловлено тем, что C. albicans на слизистых обладает свойством активно прилипать к эпителию. Это свойство наиболее интенсивно выражено при 37 о и рН 7,3; довольно высокая степень адгезии отмечена и при слабокислых значениях среды (рН 6,0). Таким образом, условия организма способствуют активной колонизации слизистых C. albicans, где этот гриб на поверхности клеток размножается в виде дрожжевой фазы.
Патогенез. В патогенезе микозов наиболее важными факторами являются:
— нарушение целостности кожи и слизистых (ожоги, лучевая терапия, потертость и т.п.);
— длительное применение антибиотиков;
— нарушении гормонального баланса (сахарный диабет);
Грибы, паразитирующие на коже человека, питаются частицами эпидермиса, роговыми массами ногтевых пластинок, а продукты их жизни — белки — вызывают аллергическую реакцию.
Факторами патогенности грибов рода Candida являются его способность к адгезии и инвазии с последующим цитолизом ткани, а затем — и к лимфогематогенной диссиминации. Candida spp. способны к инвазивному процессу в слизистых оболочках, в первую очередь представленных многослойным плоским эпителием, и реже — однослойным цилиндрическим. Чаще всего инвазивный микотический процесс наблюдается в полости рта, пищеводе, в желудке и кишечнике.
Доказано, что даже без внедрения вглубь эпителия, Candida spp. могут вызывать патологию человека — неинвазивную форму кандидоза
Контакт поверхностных и корпускулярных антигенов гриба с имммуннокомпетентными клетками макроорганизма может привести к выработке повышенных количеств специфических IgE и сенсибилизированных лимфоцитов, что служит патогенетической основой для микогенной сенсибилизации. Аллергенами у Candida albicans являются и первичные метаболиты — алкогольдегидрогеназа и кислый P2-протеин.
Это потенциально опасно в плане развития микогенных аллергических заболеваний — специфической бронхиальной астмы, атопического дерматита, крапивницы.
Резорбция в кишечнике продуктов метаболизма грибов рода Candida его плазмокоагулаза, протеазы, липофосфорилазы гемолизин и эндотоксины могут вызвать специфическую интоксикацию и вторичный иммунодефицит.
Наконец, за счет взаимодействия с представителями облигатной нормобиоты и условно-патогенными микроорганизмами Candida spp. могут индуцировать дисбиоз и микст-инфекцию слизистых оболочек.
Ключевым фактором начала инфекционного кандидозного процесса является нарушение неспецифической и специфической резистентности организма, как на местном, так и на общем уровне.
К факторам неспецифической резистентности традиционно относят адекватный баланс десквамации и регенерации эпителиоцитов, мукополисахариды слизи, нормальную микробиоту слизистых оболочек, (Bifidumbacterium spp., Lactobacillus spp., Escherihia coli, Peptostreptococus spp.,), перистальтическую активность и кислотно-ферментативный барьер пищеварительного тракта. Показано например, что лечение больных препаратами, содержащими бифидобактерии, значительно снижает содержание грибов рода Candida в кале больных.
К неспецифическим факторам относят так же секреторный IgA, лизоцим, трансферрин, компоненты комплемента. Однако наиболее важны число и функция полиморфно-ядерных мононуклеарных фагоцитов, в частности их способность к хемотаксису, аттракции, килингу и презентированию грибкового антигена. Именно в условиях нейтропении развиваются жизнеугрожающие формы кандидоза, включая висцеральные поражения (печени, желчного пузыря, поджелудочной железы).
Специфический иммунный ответ при кандидозе представлен наработкой специфических противокандидозных антител классов IgA, IgG, IgM, инактивирующих ферменты инвазии и эндотоксины гриба, а также вместе с компонентами комплемента участвующими в опсонизации.
Конфликт между факторами патогенности гриба и факторами антифунгальной резистентности приводит к развитию той или иной формы кандидоза. Механизмы патогенеза двух принципиально различных форм кандидоза (инвазивного и неинвазивного) легли в основу классификации кандидоза кишечника. Для практических целей необходимо выделять три формы поражения.
Первая — инвазивный диффузный кандидоз кишечника, вторая — фокальный (вторичный при язве двенадцатиперстной кишки, при неспецифическом язвенном колите), третья — неинвазивный (так называемый кандидозный дисбиоз).
Отдельно выделяют перианальный кандидодерматит, обусловленный инвазией псевдомицелия микромицетов в кожу перианальной области. Однако основной симптом этого заболевания — рецидивирующий анальный зуд обуславливает большую частоту обращений не к дерматологу, а к гастроэнтерологу.
Клинические проявления микозов (кандидозов) могут быть различными в зависимости от их локализации.
Диареи. В последние годы является актуальной проблема осложнений антибиотикотерапии, и в первую очередь так называемой антибиотик-ассоциированной диареей (ААД). Согласно общепринятому определению ААД — это три или более эпизодов неоформленного стула в течение двух или более последовательных дней, развившихся на фоне применения антибактериальных средств.
Основными причинами развития ААД, развивающихся после применения антибиотиков , являются:
- Аллергические, токсические, и фармакологические побочные эффекты собственно антибиотиков.
- Осмотическая диарея в результате нарушения метаболизма желчных кислот и углеводов в кишечнике
- Избыточный микробный рост в результате подавления облигатной интестинальной микробиоты.
Симптомокомплекс, развившийся на фоне применения антибиотикотерапии, может варьировать от незначительного преходящего интестинального дискомфорта до тяжелых форм диареи и колита. Клинически выделяют три основных варианта заболевания:
Колонизации кишечника Candida spp. способствует лечение широкоспектральными антибиотиками с анаэробной активностью, применение третьей генерации цефалоспоринов, а так же антибиотиков с интенсивной концентрацией в кишечнике. Колонизация кишечника микромицетами может привести к кандидемии при наличии следующих факторов риска: массивная колонизация кишечника Candida spp., первичное повреждение кишечника, гипохлоргидрия желудка, снижение кишечной перистальтики, цитотоксическая химиотерапия.
Клинически поражение грибами кишечника может представлять собой носительство, неинвазивный микотический процесс и инвазивный кандидоз.
Клинические проявления роста микромицетов
Поверхностный и кожно-слизистый кандидоз выявляют при микроскопии соскобов кожи и слизистой оболочки и выделением культуры возбудителя. Диагностику диссеминированных форм часто затрудняет недоступность поражённых органов для биопсии. В случаях, позволяющих получить образцы ткани, обнаруживают дрожжеподобные клетки и гифы. При летальных исходах посмертный диагноз устанавливают при микроскопии гистопатологических образцов секционного материала.
Кандиды хорошо растут как на простых (среды Сабуро и др.), так и на кровяных или сывороточных средах. Оптимальная температура составляет 30-37 °С, оптимальный рН — 6,0-6,8. Колонии С. albicans на агаре Сабуро беловато-кремовые [лат. candidus, снежно-белый], блестящие, напоминают капли майонеза (рис. 36-5). Отличительными признаками С. albicans считают следующие.
• Способность кандид ферментировать глюкозу и мальтозу с образованием кислоты и газа.
• При росте в жидких белковых средах кандиды при 37 °С через 2-4 ч бластоспоры подавляющего большинства штаммов С. albicans образуют особые выросты — ростовые трубки. Штаммы, не образующие их, — авирулентны.

Выбор препаратов для лечения кандидоза зависит от клинической формы и тяжести заболевания. Для лечения кожно-слизистых форм используют нистатин, леиорин, амфоглюкамин, миконазол. При тяжёлых поражениях с высоким риском диссеминированин назначают курс амфотерицина В или флуконазола.

Учебник предназначен для студентов, аспирантов и преподавателей высших медицинских учебных заведений, университетов, микробиологов всех специальностей и практических врачей.
5-е издание, исправленное и дополненное
Книга: Медицинская микробиология, иммунология и вирусология
Кандидоз
Кандидоз (кандидомикоз) – инфекционное заболевание кожи, слизистых оболочек и внутренних органов, вызываемое дрожжеподобными грибами рода Candida. Распространен повсеместно, чаще встречается в тропиках и субтропиках.
В подавляющем большинстве случаев возбудителем является C. albicans, гораздо реже C. tropicalis и другие виды. Род Candida включает свыше 100 видов, имеющих округлые, овоидные, цилиндрические или удлиненные, иногда неправильной формы клетки, размножающиеся обычно многополюсным почкованием. Псевдомицелий – цепочки из удлиненных клеток – встречается у большинства видов, некоторые из них (C. albicans) образуют терминальные хламидоспоры. Род объединяет гетерогенную группу аспорогенных дрожжей, стабилизировавшихся в гаплоидном состоянии и потерявших способность к спариванию с последующим образованием половых спор. Они являются аэробами, для питания используют белки, пептоны и аминокислоты. Они хорошо растут на кровяных и сывороточных средах, на гидролизате дрожжей. Усваивают углеводы (глюкозу, левулозу, лактозу, мальтозу); пентозы малопригодны. Хорошо растут на отварах из картофеля и моркови, риса и кукурузы, на пивном сусле. Чаще всего выращивают на среде Сабуро. Лучше всего растут при температуре 30 – 37 °C и рН 6,0 – 6,8. Колонии C. albicans на сусло-агаре круглые, сметанообразные, беловатые, диаметром до 1 см, выпуклые, блестящие, обычно гладкие, с ровными краями и глубоким врастанием в среду ветвистого древовидного псевдомицелия. Бластоспоры (почки) располагаются нерегулярно по обеим сторонам мицелия. Хламидоспоры круглые, крупные (10 – 20 мкм), двухконтурные. C. albicans сбраживает глюкозу, мальтозу, левулезу и частично галактозу; молоко не изменяет. Патогенна для лабораторных животных.
Патогенез и клиника. Как правило, кандидоз развивается как типичная аутоинфекция и является сопутствующим заболеванием или осложнением при любой патологии, приводящей к иммунодефициту. Дисбактериоз, как следствие нерациональной антибиотикотерапии, лечения кортикостероидами, часто проявляется в форме кандидоза. Сахарный диабет и другие эндокринопатии, гиповитаминозы могут сопровождаться кандидозом. Наиболее подвержены кандидозу дети и пожилые люди.
Различают поверхностный кандидоз слизистых оболочек, кожи, ногтевых валиков и ногтей; хронический генерализованный (гранулематозный) и висцеральный кандидоз, а также аллергические формы кандидоза. Кандидоз слизистых оболочек (полости рта, влагалища) называют молочницей, так как на слизистой возникает налет, напоминающий свернутое молоко. Хронический генерализованный кандидоз обычно развивается у детей с иммунодефицитными состояниями, постепенно прогрессирует, возникают пневмонии, гастриты, гепатиты и др. При висцеральном кандидозе страдают желудочно-кишечный тракт, органы дыхания, мочевыделительная система, ЦНС. На фоне имеющегося первичного очага кандидомикоза развивается сенсибилизация всего организма, и при этом могут возникать аллергические формы кандидоза, когда появляются новые очаги воспаления, но возбудитель в них отсутствует (левуриды, или кандидамикиды).
Лабораторная диагностика. При поверхностных формах кандидоза диагноз подтверждается неоднократным обнаружением возбудителя в патологическом материале (наличие псевдомицелия) и выделением его в чистой культуре. При висцеральном кандидозе применяют серологические реакции (агглютинации и РСК) и кожную аллергическую пробу с кандида-аллергеном.
Специфическая профилактика не применяется. Для лечения всех форм кандидоза используют флюкостат по специальным схемам. Применяют также нистатин, леворин, амфоглюкамин, амфотерицин B, флуцитозин, низорал. В ряде случаев эффективна аутовакцинотерапия.
Л. Д. Вейсгейм
д. м. н., профессор, заведующая кафедрой стоматологии ФУВ с курсом стоматологии общей практики ВолгГМУ
Л. М. Гаврикова
к. м. н., доцент кафедры стоматологии ФУВ с курсом стоматологии общей практики ВолгГМУ
С. М. Дубачева
к. м. н., ассистент кафедры стоматологии ФУВ с курсом стоматологии общей практики ВолгГМУ
Диагностика и лечение кандидоза полости рта — актуальная проблема стоматологии, что определяется значительной распространенностью грибковой инфекции. Так, по данным ВОЗ, до 20 % населения мира хотя бы однократно на протяжении жизни перенесли различные формы кандидозной инфекции [2].
В последнее время заболеваемость кандидозом полости рта имеет тенденцию к неуклонному росту . Это обусловлено рядом предрасполагающих факторов, таких как неконтролируемое использование антибактериальных препаратов широкого спектра действия, длительный прием кортикостероидов, а также увеличением количества пациентов с эндокринной патологией, гиповитаминозами, иммунодефицитными состояниями [4]. Несмотря на значительные успехи научных разработок в области терапии грибковых заболеваний, диагностика и лечение кандидоза полости рта — сложная клиническая задача для врача. Нередко стоматологи допускают ошибки при обследовании и лечении пациентов с кандидозом полости рта, что негативно отражается на исходе заболевания.
Целью данного исследования явились выявление и анализ врачебных ошибок, допущенных при диагностике и лечении кандидоза полости рта.
Материал и методы исследования

При обследовании больных применяли клинические и лабораторные методы. Клинические методы исследования включали сбор жалоб пациента и анамнеза с учетом данных из выписок историй болезни, представленных лечебным учреждением для консультации, оценку клинического течения заболевания, выявление врачебных ошибок при диагностике и лечении кандидоза полости рта. Стоматологическое обследование больных проводилось по общепринятой схеме, включающей осмотр слизистой оболочки полости рта (цвет, влажность, наличие и локализация элементов поражения) и оценку состояния зубов (отсутствие санации полости рта, наличие зубных отложений, наличие и качество ортопедических конструкций). Гигиеническое состояние определяли с помощью индекса Грина — Вермильона.
Лабораторные методы включали проведение клинического и биохимического анализа крови, а также микробиологические тесты для обнаружения изменений в составе микробиоценоза полости рта и кишечника. Для выявления сопутствующей патологии больным были рекомендованы консультации эндокринолога, гастроэнтеролога, иммунолога, терапевта.
После обследования пациентам назначалось лечение, направленное на ликвидацию возбудителя заболевания и нормализацию иммунной системы, а также десенсибилизирующая терапия (рис. 2). Курс лечения кандидоза составил 21 день.
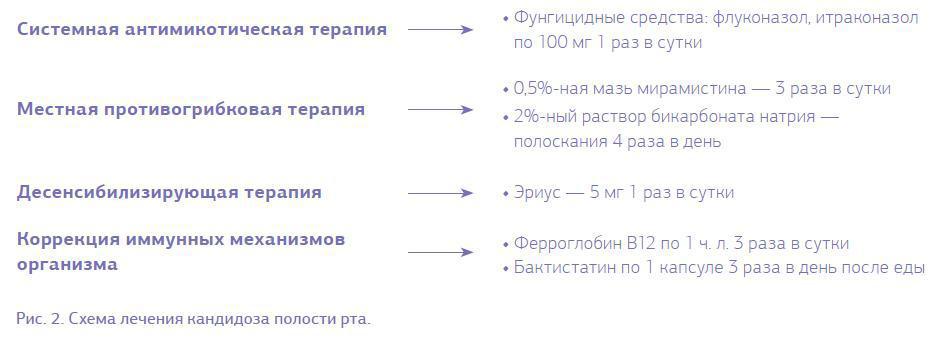
Результаты исследования и обсуждение
При стоматологическом обследовании больных врачи-стоматологи не уделяли должного внимания состоянию гигиены полости рта и наличию санации. Хотя хроническая травма слизистой оболочки рта острыми краями зубов, некачественными протезами, разрушенными коронками относится к факторам, провоцирующим развитие кандидоза полости рта, и должна устраняться в первую очередь. Однако у 98 % направленных на консультацию больных отмечено неудовлетворительное гигиеническое состояние полости рта (УИГР-У=2,8±0,2), обилие зубных отложений, отсутствие санации полости рта. Врачи не учитывали, что именно уровень состояния функциональной системы ротовой полости у каждого индивидуума с учетом гигиенических навыков, травмирующих факторов характеризует экосистему в целом.
Только 7 пациентов были направлены на консультации эндокринолога, гастроэнтеролога, из них 4 больных проигнорировали обращение к эндокринологу.
Врачи-стоматологи должны помнить, что кандидоз полости рта часто является первым и единственным клиническим признаком бессимптомно протекающего сахарного диабета.
Поэтому консультация эндокринолога является обязательным этапом при обследовании больных кандидозом. Большинству пациентов (86 %) вообще не проводилось обследование для выявления сопутствующей патологии. У всех консультируемых пациентов были выявлены сопутствующие заболевания. Заболевания желудочно-кишечного тракта диагностировали у 72 % больных, эндокринопатии (сахарный диабет, гипотиреоз) — у 28 % обследуемых.
При анализе 94 % выписок из историй болезни, представленных на консультации, было выявлено отсутствие лабораторных методов: клинического и биохимического анализа крови, а также микробиологических тестов для обнаружения изменений в составе микробиоценоза полости рта и кишечника. Однако диагностика кандидоза полости рта должна быть комплексной и включать в себя не только клинические, но и лабораторные методы, ведущим из которых является микробиологический.
При выборе препарата для системной терапии не оценивалось его влияние на возбудителя (фунгистатическое или фунгицидное), а также на макроорганизм (не учитывалось как состояние иммунной системы, так и индивидуальная чувствительность к данному веществу) . У 2/3 больных лечение назначалось без учета данных результатов бактериологического посева на чувствительность к препаратам . Принимая во внимание рост устойчивости Candida к антимикотическим препаратам, в настоящее время системная терапия должна назначаться только с учетом чувствительности возбудител я. По результатам бактериологического посева у 83 % консультируемых пациентов выявлялась высокая чувствительность к флуконазолу, у 17 % — к итраконазолу.

Игнорировались показания для применения системной антимикотической терапии, в первую очередь определенная клиническая форма поражения (острый псевдомембранозный кандидоз, клинические признаки диссеминации, хронические формы заболевания, резистентные к ранее проводимой местной терапии). У ряда больных применялась только местная антимикотическая терапия, однако местные препараты действуют только на поверхности слизистой оболочки полости рта, уменьшая проявления кандидоза, при этом элиминация возбудителя часто не достигается.
Анализ ошибок, допущенных врачами-стоматологами при диагностике и лечении кандидоза полости рта, свидетельствует о недооценке факторов риска развития кандидоза, неправильном понимании патогенеза заболевания, одностороннем представлении кандидоза как локального патологического процесса.
В настоящее время кандидоз следует рассматривать как иммуннодефицитное состояние, возникшее в результате глубокой разбалансировки экосистемы в целом. Такое представление о заболевании обусловливает принципиальную необходимость комплексного подхода к диагностике и лечению кандидоза. Терапия, направленная на все звенья патологического процесса, позволяет повысить эффективность лечения и, кроме того, способствует достижению длительного периода ремиссии заболевания [3]. С целью устранения врачебных ошибок рекомендуется постоянно проводить практические конференции по разбору клинических случаев кандидоза полости рта с участием преподавателей кафедр стоматологии ФУВ.

- Вейсгейм Л. Д., Дубачева С. М., Гаврикова Л. М. Комплексное лечение кандидоза полости рта // Международный журнал прикладных и фундаментальных исследований . — 2014, № 2 . — С. 48—51.
- Грачева Н. В. Клиника, диагностика и лечение хронического кандидоза слизистой оболочки полости рта // Дисс. канд. мед. наук. М.: 2001.— 134 с.
- Панченко А. Д., Булкина Н. В. Повышение эффективности терапевтического лечения больных кандидозом полости рта // Дентал Юг. — 2011, № 3. — С. 8—9.
- Рединова Т. Л., Злобина О. А. Частота кандидоза слизистой оболочки полости рта и эффективность его лечения у больных сахарным диабетом // Стоматология. — 2001, № 3. — С. 20—23.
