
Проблема фертильности – одна из актуальных проблем гинекологии и андрологии, а при бесплодии супружеской пары имеется крайне редкое сочетание социального, психического и – практически всегда – физического нездоровья в семье.
В России частота бесплодных браков превышает 15%, что, по данным ВОЗ, является критическим уровнем.
По данным Минздравсоцразвития, около 6 миллионов супружеских пар в России хотят, но не могут иметь детей, и число таких пар неуклонно увеличивается.
- С 1991 года смертность в России превышает рождаемость.
- Суммарный коэффициент рождаемости, необходимый для простого воспроизводства населения, снизился с 2,15 до 1,35.
- Повторные рождения сократились с 50% до 30%
- Население страны ежегодно уменьшается почти на миллион человек.
Одна из причин снижения рождаемости – бесплодие. По данным ВОЗ 8-12% семейных пар во всем мире (или 100 млн. мужчин и женщин) в течение своей репродуктивной жизни сталкивается с этой проблемой.
Еще немного фактов:
- Мужской фактор бесплодия обнаруживают у 50% бесплодных пар.
- Примерно 3-4% всех пар, несмотря на желание иметь ребенка, остаются бесплодными.
- 7-8% всех мужчин на протяжении своей жизни сталкивается с проблемой фертильности.
- Распространенность бесплодия среди мужчин в 2 раза превосходит распространенность сахарного диабета.
Причины, приводящие к мужскому бесплодию, могут быть локализованы на разных уровнях и быть следствием нарушений многих органов и систем. При этом только у одного из 10 мужчин данные причины связаны с врожденными генетическими, анатомическими, эндокринологическими или иммунными факторами. В большинстве случаев причины бесплодия – приобретенные, обусловленные воздействие неблагоприятных факторов (образа жизни, вредных привычек, проф. и экологических вредностей, социально-экономических факторов).
Учитывая многолетнее многоцентровое исследование ВОЗ (2000), был предложен и рекомендован стандартный алгоритм оценки фертильности. В его основе – принцип разумной достаточности, снижение объема и затрат на исследования. В то же время работа специализированных клиник требует более дифференцированного анализа причин мужского бесплодия. Обследование в этом случае должно включать широкий спектр лабораторных, инструментальных и даже инвазивных методов.
Важнейшим методом в оценке функционального состояния половых желез и прогноза фертильности мужчины является исследование спермы. О мужском бесплодии принято говорить, когда сперма содержит мало сперматозоидов или они плохого качества.
Критерии анализа качества эякулята основаны на анализе популяции фертильных мужчин и представлены в виде референтных значений (ВОЗ, 2010).
Лечение мужского бесплодия начинается с обращения к высококвалифицированному специалисту. Проведение грамотного обследования дает возможность установить конкретные причины нарушений в репродуктивной сфере. Только после этого начинается составление индивидуальной программы лечения мужского бесплодия, учитывающей особенности возникновений той или иной формы этого патологического состояния.

Общие рекомендации
Вне зависимости от формы мужского бесплодия мужчинам, стремящимся к зачатию ребенка, следует соблюдать следующие рекомендации:
- отказ от курения и употребления алкоголя;
- регулярная половая жизнь с партнершей с частотой половых актов не реже 1 раза в 3-4 дня;
- умеренная физическая активность;
- соблюдение сбалансированной диеты и контроль массы тела;
- избегание стрессовых ситуаций;
- отказ от тесного нижнего белья из синтетических материалов (информацию о влияние тесного мужского белья смотрите здесь;
- ограничение посещения бани и сауны.
Лечение секреторной формы мужского бесплодия
Задачей терапии секреторной формы мужского бесплодия является нормализация процессов выработки и созревания сперматозоидов. С этой целью могут проводиться следующие мероприятия:
- лечение варикоцеле – наиболее действенным методом является оперативное лечение варикоцеле с использованием микрохирургического или лапароскопического доступа. После выполнения склеротерапии или эмболизации пораженной яичковой вены в большинстве случаев наблюдается улучшение показателей сперматогенеза;
- лечение водянки яичка – коррекция водянки небольших размеров может проводиться при помощи пунктирования или склерозирования, однако наиболее часто специалисты прибегают к хирургическому лечению данной патологии;
- лечение крипторхизма – как правило, хирургическая коррекция данного заболевания проводится в раннем детском возрасте. Оперативное вмешательство может выполняться как классическим способом, так и с применением лапароскопического доступа;
- лечение гормональных нарушений – проводится заместительная гормональная терапия ФСГ, ЛГ, мужскими половыми гормонами, стимулирующая рост и созревание сперматозоидов (см. гормональный фон мужчины);
- лечение половых инфекций – своевременное выявление и адекватное лечение инфекций с половым путем передачи предупреждает хронизацию патологического процесса и способствует нормализации работы репродуктивной системы. Применяются антибактериальные, противовирусные, противовоспалительные и иммунокорригирующие лекарственные средства.
Лечение обтурационной формы мужского бесплодия
Устранение причины обструкции семявыносящих протоков позволяет значительно увеличить шансы на успешное зачатие. С целью устранения таких нарушений используются следующие группы методов:
- методы, направленные на восстановление проходимости семенных путей – в зависимости от уровня обструкции семявыносящих путей используется несколько вариантов операции: — вазоэпидидистомия – заключается в сшивании канальца придатка с семявыносящим протоком;
— вазовазостомия – направлена на удаление непроходимого участка семявыносящего протока;
— трансуретральная резекция простаты – дает возможность бороться с обтурационным бесплодием, вызванным закупоркой семяизвергательных каналов; - методы, направленные на извлечение сперматозоидов – позволяют получить материал для выполнения вспомогательных репродуктивных процедур. Возможные следующие варианты получения сперматозоидов:
— PESA – представляет собой чрескожную пункцию придатка яичка;
— MESA – микрохирургическая операция с получением содержимого придатка яичка;
— TESE – открытая пункционная биопсия яичек;
— биопсия яичка – чрескожная пункция яичек.
Лечение аутоиммунной формы мужского бесплодия
Лечение иммунологической несовместимости партнеров представляет собой наиболее сложную задачу. При выявлении такой формы бесплодия следует, прежде всего, исключить другие факторы, способные привести к нарушениям в репродуктивной сфере: урогенитальные инфекции, варикоцеле, нарушение проходимости семявыносящих путей и т.п. Если же после проведенного лечения бесплодие сохраняется, прибегают к следующим методам терапии:
- медикаментозное лечение – в зависимости от выявленных при лабораторном обследовании нарушений обоим партнерам может быть показано гормональное лечение. Системная энзимотерапия, применение иммунокорригирующих препаратов дают возможность нормализовать деятельность иммунной системы организма;
- капацитация спермы – является подготовительным этапом при использовании вспомогательных репродуктивных технологий. Капацитация заключается в специальной обработке спермы, позволяющей подготовить сперматозоиды к процессу оплодотворения яйцеклетки.
Вспомогательные репродуктивные технологии
К вспомогательным репродуктивным технологиям, позволяющим преодолеть мужское бесплодие, относятся следующие процедуры:
- внутриматочная инсеминация спермой мужа – при иммунологическом бесплодии, эякуляторной дисфункции, олигоастенозооспермии введение сперматозоидов непосредственно в полость матки дает возможность значительно повысить шансы на зачатие. При этом яйцеклетку достигают даже те сперматозоиды, которые в обычных условиях погибли бы в цервикальном канале;
- экстракорпоральное оплодотворение (ЭКО) выполняется в несколько этапов. На первом из них с помощью гормональной терапии выполняется стимуляция суперовуляции у партнерши. Затем в ходе хирургической манипуляции осуществляется получение нескольких яйцеклеток, в последствие оплодотворяемых в лабораторных условиях сперматозоидами мужа. Полученные эмбрионы имплантируются в полость матки, где получают шанс на нормальный рост и развитие;
- экстракорпоральное оплодотворение с применением методики ИКСИ – благодаря методике ИКСИ даже мужчины с выраженной азооспермией получили шанс на отцовство. Эта процедура выполняется в ходе ЭКО и заключается во введении сперматозоида в яйцеклетку при помощи специальной микрохирургической техники. Для достижения успешного результата достаточно лишь одного сперматозоида, полученного естественным путем или в ходе хирургической манипуляции;
- использование спермы донора – применение донорского материала в ходе ЭКО рассматривается как вариант достижения зачатия при выраженных нарушениях сперматогенной функции у мужчины или наличии опасных наследственных заболеваний.
Грамотное лечение мужского бесплодия, основанное на продуктивном взаимодействии урологов, андрологов, гинекологов и репродуктологов, позволяет большинству семейных пар стать счастливыми родителями.






































Главное меню
Главное меню
Мужчина сохраняет шансы стать отцом в любом возрасте. Если у женщин после 40 лет происходит стремительное снижение овариального резерва, резко снижающее перспективы деторождения, то у мужчин сперматозоиды в эякуляте остаются до самых преклонных лет. Согласно данным литературы, самый старший мужчина, сумевший стать отцом, был 94-летним [3].
ВЛИЯНИЕ ВОЗРАСТА НА ПОКАЗАТЕЛИ ФЕРТИЛЬНОСТИ
У мужчин старшей возрастной группы значимо повышается время, необходимое для достижения беременности [4]. У мужчин старше 40 лет по сравнению с мужчинами младше 30 лет вероятность наступления беременности у партнерши в течение 1 года на 30% меньше [5]. Эти же авторы отмечают, что если сравнить между собой мужчин младше 25 и старше 45 лет, – то оказывается, что время до наступления беременности у старшей группы повышается в 5 раз. В течение 6 месяцев попыток зачать ребенка среди мужчин младше 25 лет беременность наступила в 76,8% случаев, а среди мужчин старше 45 лет – в 52,9% случаев [5]. Данные факты можно объяснить тем, что c повышением возраста мужчины снижается вероятность наступления беременности при половых контактах в дни овуляции половых партнерш [6].
Помимо вероятности зачатия возраст мужчины оказывает влияние и на течение беременности и вероятность ее успешного завершения. Так, в нескольких публикациях отмечается повышение вероятности невынашивания беременности при старшем возрасте отца. Вероятность выкидыша в 1,3 раза выше, если отец старше 35 лет, причем это наиболее выражено в 1 триместре беременности [7], что, вероятно, связано с повышением фрагментации ДНК сперматозоидов. По мнению de la Rochebrochard E. и Thonneau (2002), возраст отца не оказывает значимого влияния на риск невынашивания, если возраст матери менее 30 лет. Однако, если она старше 30 и, особенно 35 лет, возраст отца приобретает важное значение, резко повышая частоту невынашивания беременности (рис. 1) [8].
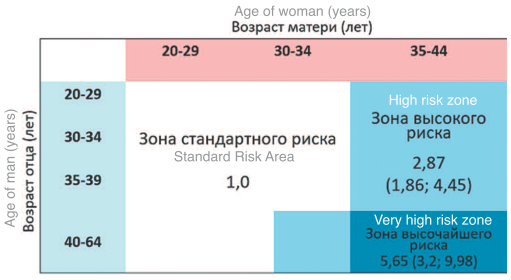
Рис. 1. Зависимость риска невынашивания беременности от возраста родителей. Представлены результаты логистического регрессионного анализа: отношение шансов (odds ratio) и доверительный интервал (95%) [8].
Fig. 1. Relation of parental age and miscarriage rate. Results of logistic regression analisis: odds ratio and confidence interval (95%) [8]
Риск преждевременных родов от мужчины старшего отцовского возраста не повышается [9]. Однако при этом значимо повышается риск мертворождения, который находится на минимальных значениях в возрасте 30 лет, существенно повышаясь после 50 лет [9]. Авторы отмечают, что влияние возраста отца на риск мертворождения во много раз менее выражено, чем влияние возраста матери [10].
ВЛИЯНИЕ ВОЗРАСТА НА ПАРАМЕТРЫ ЭЯКУЛЯТА
Изучение параметров эякулята у мужчин разных возрастных групп – самый распространенный (наиболее технически простой и объективный) способ изучения влияния APA на фертильность. Рассмотрим, как меняются с возрастом базовые показатели спермограммы. Наиболее значимым источником по этому вопросу на данный момент является систематический обзор и метаанализ, выполненный Johnson S. и соавторами в 2015 г. [11], основные результаты которого представлены на рис. 2
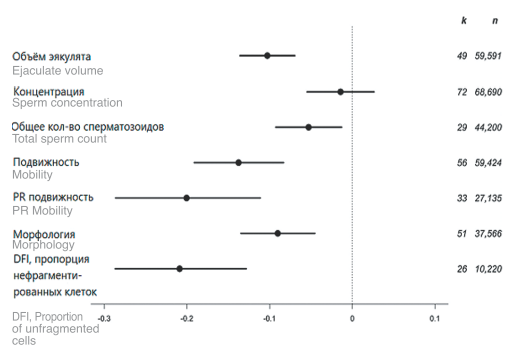
Рис. 2. Зависимость параметров эякулята от возраста мужчины. Представлены общие средние значения по данным метаанализа и доверительные интервалы (95%). k – количество анализированных исследований, n – суммарное количество субъектов, вошедших в исследования [11].
Fig. 2. Relation of paternal age and sperm parameters. Means and confidence intervals from meta-analysis. k – number of studies, n – number of patients [11].
Согласно большинству исследований, концентрация сперматозоидов в эякуляте в старшем возрасте значимо не меняется [11]. Иная картина наблюдается в отношении прогрессивной подвижности сперматозоидов. Большинство авторов отмечают существенное снижение данного показателя у мужчин старшего возраста, подчеркивая, что прогрессивная подвижность – наиболее подверженный возрастным изменениям показатель [11]. Одной из причин данных отличий авторы называют заболевания предстательной железы, которая встречается тем чаще, чем старше мужчина, а также патологию придатков яичка, чаще встречающуюся у мужчин старшей возрастной группы [12].
Помимо базовых параметров спермограммы в последние годы в рутинную практику клиник репродукции вошли несколько дополнительных функциональных исследований качеств эякулята, результаты которых могут влиять на выбор тактики лечения, планирование процедур вспомогательных репродуктивных технологий (ВРТ), выбор метода оплодотворения при ВРТ. К ним относятся тест на концентрацию активных форм кислорода в эякуляте (АФК-тест), исследование концентрации фруктозы, определение индекса фрагментации ДНК сперматозоидов (DFI). Количество публикаций, изучавших влияние возраста мужчины на функциональные пробы спермы невелико. Так, ранее было показано нарастание оксидативного стресса в эякуляте с возрастом мужчины [17]. Концентрация фруктозы, напротив, снижается, что авторы связывают с патологией семенных пузырьков [14].
В последние годы в рутинную практику клиник репродукции входят тесты DFI, под которым понимают процент поврежденных цепочек ДНК в хроматине сперматозоидов. Данный показатель не всегда коррелирует с показателями спермограммы и может быть самостоятельной причиной бесплодия, невынашивания беременности и неудач процедур ВРТ. Более того, сейчас DFI рассматривается, как наиболее важный фактор прогноза успеха процедур ВРТ со стороны мужчины [18]. Большинство исследователей утверждает, что DFI повышается с возрастом мужчины [11,19], в связи с чем некоторые авторы рекомендуют включать данный тест в перечень обязательных при обследовании по поводу бесплодия мужчины старшего возраста.
РЕЗУЛЬТАТЫ ВСПОМОГАТЕЛЬНЫХ РЕПРОДУКТИВНЫХ ТЕХНОЛОГИЙ
Помимо перспектив достижения естественной беременности, возраст отца оказывает влияние и на результаты процедур ВРТ, хотя, результаты разных исследовательских коллективов очень противоречивы. В отношении внутриматочной инсеминации (ВМИ) часть авторов утверждает, что вероятность успеха ВМИ не меняется в зависимости от возраста мужчины [20]. В то же время другие авторы показали снижение вероятности успеха ВМИ при старшем отцовском возрасте [21]. В исследовании S. Belloc и соавт. было показано, что вероятность успеха ВМИ снижается с 12,3% (за одну процедуру) у мужчин младше 30 лет до 9,3% после 45 лет. Также авторы показали, что повышается вероятность невынашивания наступившей беременности с 13,7% у мужчин младше 30 лет до 32,4% – после 45 лет [21].
Достаточно подробно освещено в литературе влияние старшего возраста мужчины на результаты процедур экстракорпорального оплодотворения (ЭКО) и интрацитоплазматической инъекции сперматозоидов (ИКСИ), однако данные весьма разнородны и противоречивы. Вероятность фертилизации (оплодотворения яйцеклетки) по данным большинства авторов не зависит от возраста отца [13], однако, нами встречены публикации, которые все-таки отмечают снижение вероятности фертилизации [22]. При этом один из наиболее важных показателей – вероятность наступления беременности не меняется при старшем возрасте отца ни при традиционном ЭКО [13], ни при выполнении ИКСИ [23]. E. de La Rochebrochard и соавт. сообщают, что вероятность наступления беременности при ЭКО становится меньше в 1,5 раза после 30 лет, а в дальнейшем – существенно не меняется. Авторы замечают, что важнейшим параметром для достижения и вынашивания беременности является возраст матери. При возрасте матери менее 30 лет возраст отца по данным авторов перестает иметь клиническое значение [24].
Самый главный параметр, характеризующий эффективность программ ВРТ – вероятность рождения живого ребенка. По данным наиболее крупного исследования, где на материале 4887 циклов ЭКО/ИКСИ с использованием донорских яйцеклеток (что исключает влияние возраста матери) было показано, что возраст отца не влияет на вероятность рождения живого ребенка [23]. Однако в другой масштабной работе, где также анализировались результаты ЭКО с использованием донорских яйцеклеток, было показано существенное снижение вероятности рождения живого ребенка при возрасте отца старше 50 лет с 56 до 41% [25].
Таким образом, можно заключить, что данные о влиянии старшего возраста отца на результаты ВРТ противоречивы и во многом зависят от дизайна исследований.
ВЛИЯНИЕ ВОЗРАСТА ОТЦА НА ЗДОРОВЬЕ РЕБЕНКА
Можно считать доказанным фактом, что возраст отца влияет не только на вероятность зачатия и исходы беременности, но и на здоровье родившегося ребенка. Наиболее авторитетным источником в этом вопросе можно считать недавний систематический обзор и метаанализ N. Oldereid и соавт., в котором они обобщили результаты всех (более 14 тысяч) публикаций по данному вопросу [9]. Согласно данному обзору, при старшем возрасте отца незначительно повышается общая смертность детей в возрасте от 5 лет от разных причин, а также повышается в целом риск врожденных пороков у детей. Традиционно противоречивым вопросом является связь риска хромосомных аномалий с возрастом родителей. В метаанализе отмечается незначительная корреляция возраста отца с частотой синдрома Дауна. Однако в литературе можно встретить публикации, сообщающие о том, что риск синдрома Дауна не ассоциирован с возрастом отца [26]. Что касается синдрома Кляйнфельтера, то его риск с возрастом отца повышается, хотя по этому вопросу информации обнаружено значительно меньше [27].
В отношении других заболеваний установлено, что с возрастом отца у детей повышается риск ахондроплазии [28], синдрома Аперта [29] и острого лимфобластного лейкоза [9]. Наиболее доказанным вопросом можно считать влияние возраста отца на риск психиатрических заболеваний потомства, таких, как аутизм и шизофрения [9]. Риск шизофрении минимален при возрасте отца 25-29 лет. Что интересно – он на 5% выше в группе 20- 24 года (OR-1,08) и на 10% выше в группе старше 30 лет. Относительный риск шизофрении в случае, когда отец старше 50 лет – выше в 1,66 раз [30].
ЧТО СЧИТАТЬ СТАРШИМ ОТЦОВСКИМ ВОЗРАСТОМ?
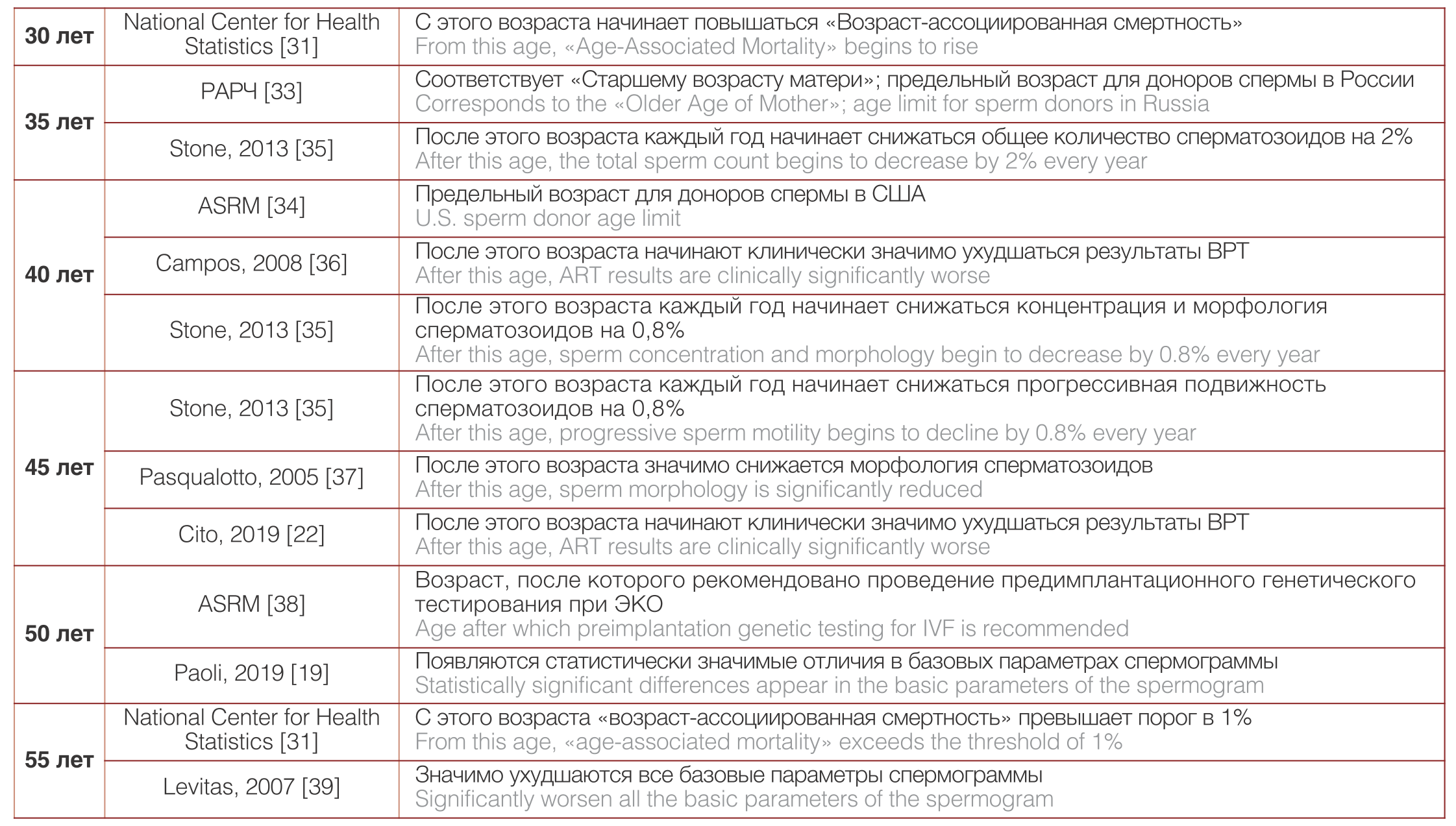
Старший возраст матери является более четко определенным понятием. Международные ассоциации акушеров-гинекологов считают таковым возраст старше 35 лет [32]. В связи с этим распространенной позицией в отношении APA является такой же возраст мужчин, несмотря на большое отличие процессов старения репродуктивных систем мужчин и женщин. Так, Российская ассоциация репродукции человека рекомендует данную отсечку возраста как максимальный возраст для доноров спермы [33]. Между тем, Американское общество репродуктивной медицины (ASRM) считает, что доноры спермы должны быть моложе 40 лет [34]. Разные доводы в пользу той или иной точки зрения отражены в таблице 1.
Разные доводы в пользу той или иной точки зрения отражены в таблице 1
ЗАКЛЮЧЕНИЕ
Несмотря на большое количество накопленных научных данных, на сегодняшний день не существует общепринятого подхода, особой тактики обследования и лечения в отношении мужчин старшего возраста с бесплодием. Из разрозненных источников и упомянутых выше исследований можно выделить несколько основных положений, которые можно внедрять в практику, а также положений, которые требуют дальнейшего изучения.
- Генетическое консультирование – на данный момент не существует специальных протоколов мониторинга генетических заболеваний при АРА. Текущим стандартом является пренатальное исследование всех беременных женщин на сроке до 16 недель [40]. При этом в случае АРА пара должна быть информирована относительно ограничений данного обследования, которое в основном направлено на диагностику анеуплоидий, таких как синдром Дауна и не способно выявлять синдромы, связанные со старшим возрастом отца.
- Вспомогательные репродуктивные технологии – хотя это положение и не отражено в клинических рекомендациях, большинство репродуктологов склонно расширять показания к процедурам ВРТ в случае бесплодия у супружеских пар старшего возраста. Даже если лечение мужчины в течение 6 или более месяцев даст положительный эффект, снижение овариального резерва партнерши нивелирует эту пользу. Кроме того, указанные выше работы показали, что результаты ВРТ ухудшаются вследствие старшего возраста в меньшей степени, чем перспективы естественного зачатия.
- Предимплантационное генетическое тестирование. В рамках программ ЭКО/ИКСИ возможно проведение генетического тестирования эмбриона на предмет анеуплоидий и моногенных заболеваний, связанных со старшим возрастом отца. ASRM, не внося это в свои официальные рекомендации, говорит о возможности предимплантационного тестирования при возрасте мужчины старше 50 лет [38].
- Оценка индекса фрагментации ДНК и лечение, направленное его на снижение – учитывая доказанный факт возрастного повышения DFI, обоснованной можно считать рекомендацию измерять DFI всем мужчинам старше 40 лет [11]. При обнаружении повышенного DFI разработан ряд методик, позволяющих снизить фрагментацию ДНК [41,42,43] и улучшить тем самым репродуктивные исходы.
Все вышеперечисленное является основанием для того, чтобы считать бесплодных мужчин старшего возраста отдельной группой, нуждающейся в разработке особого лечебно-диагностического подхода, основанного на новых клинических исследованиях, призванных прояснить поставленные выше вопросы.
Психогенные факторы бесплодия
Конфликтные ситуации в семье, на работе, неудовлетворенность половой жизнью, а также настойчивое желание иметь ребенка или, наоборот, боязнь беременности могут вызывать нарушения овуляции, имитирующие эндокринное бесплодие. Аналогичным образом индуцируемые стрессовыми ситуациями вегетативные нарушения могут обусловить дискоординацию гладкомышечных элементов маточных труб с функциональной трубной непроходимостью. Пациенткам с бесплодием назначают консультацию психоневролога. Специалист может применить транквилизаторы, седативные препараты, а также психотерапевтические процедуры. В ряде случаев подобная терапия эффективна без применения стимуляторов овуляции.
Искусственная инсеминация — введение спермы в половые пути женщины с целью индуцировать беременность. Можно использовать сперму мужа или донора.
Инсеминацию проводят амбулаторно 2—3 раза в течение менструального цикла на его 12—14-й день (при 28-дневном цикле).
Донорскую сперму получают от мужчин моложе 36 лет, физически и психически здоровых, не имеющих наследственных заболеваний и нарушений развития и без случаев потери плода и спонтанного аборта у родственниц.
По данным литературы, частота беременности после искусственной инсеминации составляет 10—20%. Течение беременности и родов аналогичны таковым при естественном зачатии, а пороки развития плода регистрируют не чаще, чем в общей популяции.
Экстракорпоральное оплодотворение — оплодотворение яйцеклеток in vitro, культивирование и перенос полученных эмбрионов в матку.
В настоящее время экстракорпоральное оплодотворение проводят с применением индукторов овуляции, чтобы получить достаточно много зрелых ооцитов.
Вспомогательные репродуктивные технологии позволяют использовать программы криоконсервации не только спермы, но и ооцитов и эмбрионов, что уменьшает стоимость попыток ЭКО.
Стандартная процедура ЭКО состоит из нескольких этапов. Сначала проводят активацию фолликулогенеза в яичниках с помощью стимуляторов суперовуляции по тем или иным схемам, затем делают пункцию всех фолликулов диаметром более 15 мм под контролем ультразвукового сканирования яичников и инсеминацию ооцитов путем введения в среду не менее 100 000 сперматозоидов. После культивирования эмбрионов в течение 48 ч переносят не более 2—3 эмбрионов с помощью специального катетера в полость матки (оставшиеся эмбрионы с нормальной морфологией можно подвергнуть криоконсервации для дальнейшего использования в повторных циклах ЭКО).
При экстракорпоральном оплодотворении единичными сперматозоидами возможно оплодотворение ооцитов (интрациоплазматическая инъекция сперматозоидов — ИЦИС).
При ИЦИС осуществляют микроманипуляционное введение единственного сперматозоида под визуальным контролем в зрелый ооцит, находящийся в стадии метафазы II деления мейоза. Все остальные этапы процедур аналогичны ЭКО.
При азооспермии используют методы в рамках программы ЭКО+ +ИЦИС, позволяющие получать сперматозоиды из эпидидимиса и яичка.
Показанием к хирургическому лечению синдрома гиперстимуляции яичников являются признаки внутреннего кровотечения вследствие разрыва яичника. Объем оперативного вмешательства должен быть щадящим, с максимальным сохранением яичниковой ткани.
Особенности течения и ведения беременности после экстракорпорального оплодотворения обусловлены высокой вероятностью ее прерывания, недонашивания и развития тяжелых форм гестозов. Частота этих осложнений зависит в первую очередь от характера бесплодия (чисто женское, сочетанное или только мужское), а также от особенностей проведенной процедуры ЭКО.
У детей, рожденных в результате экстракорпорального оплодотворения, частота врожденных аномалий не выше таковой в общей популяции новорожденных.
Частота многоплодия при экстракорпоральном оплодотворении составляет 25—30%.
Индекс массы тела (англ. body mass index (BMI), ИМТ) — величина, позволяющая оценить степень соответствия массы человека и его роста и, тем самым, косвенно оценить, является ли масса недостаточной, нормальной или избыточной. Важен при определении показаний для необходимости лечения.
Индекс массы тела рассчитывается по формуле:
m — масса тела в килограммах
h — рост в метрах,
и измеряется в кг/м².
Например, вес человека = 85 кг, рост = 164 см. Следовательно, индекс массы тела в этом случае равен:
ИМТ = 85 : (1,64×1,64) = 31,6
Показатель индекса массы тела разработан бельгийским социологом и статистиком Адольфом Кетеле (Adolphe Quetelet) в 1869 году.
В соответствии с рекомендациями ВОЗ разработана следующая интерпретация показателей ИМТ:
| Индекс массы тела | Соответствие между массой человека и его ростом |
| 16 и менее | Выраженный дефицит массы |
| 16—18,5 | Недостаточная (дефицит) масса тела |
| 18,5—25 | Норма |
| 25—30 | Избыточная масса тела (предожирение) |
| 30—35 | Ожирение первой степени |
| 35—40 | Ожирение второй степени |
| 40 и более | Ожирение третьей степени (морбидное) |
Индекс массы тела следует применять с осторожностью, исключительно для ориентировочной оценки — например, попытка оценить с его помощью телосложение профессиональных спортсменов может дать неверный результат (высокое значение индекса в этом случае объясняется развитой мускулатурой). Поэтому для более точной оценки степени накопления жира наряду с индексом массы тела целесообразно определять также индексы центрального ожирения.
С учетом недостатков метода определения индекса массы тела был разработан индекс объёма тела.
Согласно израильскому исследованию идеальным для мужчин является индекс массы тела в 25—27. Средняя продолжительность жизни мужчин с таким ИМТ была максимальна.
Кроме того, для определения нормальной массы тела может быть применен ряд индексов:
Индекс Брока используется при росте 155—170 см. Нормальная масса тела при этом равняется (рост [см] — 100) — 10 (15 %).
Индекс Брейтмана. Нормальная масса тела рассчитывается по формуле — рост [см] • 0,7 — 50 кг.
Индекс Борнгардта. Идеальная масса тела высчитывается по формуле — рост [см] • окружность грудной клетки [см] / 240.
Индекс Давенпорта. Масса человека [г], делится на рост [см], возведенный в квадрат. Превышение показателя выше 3,0 свидетельствует о наличии ожирения.
Индекс Одера. Нормальная масса тела равна расстоянию от темени до симфиза [см] • 2 — 100.
Индекс Ноордена. Нормальный вес равен рост [см] • 420/1000.
Индекс Татоня. Нормальная масса тела = рост-(100+(рост-100)/20)
В клинической практике для оценки массы тела наиболее часто используется индекс Брока.
Кроме росто-весовых показателей может быть использован метод определения толщины кожной складки, предложенный Коровиным. По этой методике определяется толщина кожной складки в подложечной области (в норме —1,1— 1,5 см). Увеличение толщины складки до 2 см свидетельствует о наличии ожирения.
Не нашли то, что искали? Воспользуйтесь поиском:
