Что такое эндометриоз?
Все бы ничего, но эндометрий – особенная ткань, которая задумана природой для приема оплодотворенной яйцеклетки и создания для нее комфортных условий. Для этих целей каждый месяц в начале цикла эндометрий активно растет и уплотняется под влиянием гормона эстрогена. Примерно к 15 дню цикла к процессу подключается другой гормон – прогестерон: ткани эндометрия начинают выделять много слизи, сосуды расширяются и становятся полнокровными, чтобы обеспечить самый лучший прием для новой жизни. Если зачатия не произошло – то к концу цикла содержание обоих гормонов резко снижается, разросшийся слой эндометрия разрушается и отторгается – начинается менструация.
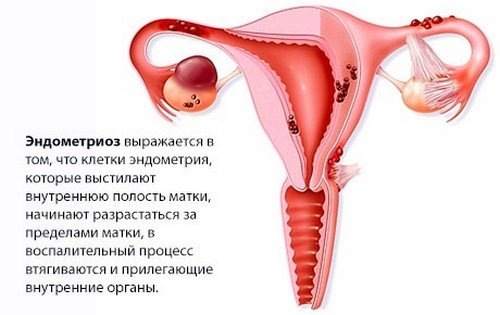
Излишнее разрастание эндометрия внутри матки или присутствие его в других органах приводит к патологии — эндометриозу. Как и нормальная слизистая оболочка матки, такие ткани растут в начале каждого цикла и разрушаются во время менструации. Это может приводить к образованию спаек и эндометриоидных кист.
Эндометриоз – это дисгормональное, иммунозависимое и генетически обусловленное заболевание, которое характеризуется доброкачественным разрастанием ткани, сходной по морфологическому строению и функции с эндометрием, но за пределами полости матки. Эндометриоз относят к наиболее распространённым гинекологическим заболеваниям, особенно часто он встречается у женщин в возрасте 20-40 лет. По локализации очагов его делят на генитальный и экстрагенитальный.
Генитальный эндометриоз бывает внутренним – когда ткань разрастается в теле матки, перешейке и интерстициальных отделах труб, и наружный – когда поражаны влагалищная часть шейки матки, влагалище, яичники, трубы и брюшина малого таза.
Экстрагенитальный эндометриоз – это поражение всех остальных органов, кроме половых. Очаги эндометриоза подвержены гормональному влиянию во время менструального цикла и именно этим циклическим изменениям обусловлены основные симптомы и жалобы женщин, страдающих данной патологией.
Причины эндометриоза
Однозначного мнения о том, почему возникает эндометриоз, во врачебном сообществе нет. Предполагают что клетки эндометрия попадают во время менструации из маточных труб в брюшную полость, либо разносятся по телу с лимфо- и кровотоком, идущим от матки.
Известны случаи возникновения эндометриоза у мужчин, проходивших терапию эстрогенами, что доказывает гормональную природу этого заболевания.
Однако из-за распространённости эндометриоза у девочек на второе место в настоящее время выходит генетически детерминированная теория происхождения эндометриоза: изменения, возникающие на этапе формирования плода в утробе матери. Часто в молодом возрасте заболевание сочетается с пороками развития половых органов.
К факторам риска эндометриоза относятся:
гормональные нарушения, когда рецепторы улавливают гормоны с повышенной активностью;
частые внутриматочные вмешательства;
хроническое стрессовое состояние организма.
Симптомы эндометриоза
Часто эндометриоз никак себя не проявляет и признаки этого заболевания видны только при ультразвуковом исследовании.
В других случаях эндометриоз может привести к таким последствиям как:
- боли внизу живота, особенно во второй половине цикла;
- неприятные ощущения во время секса;
- кровянистые выделения между менструациями;
- нарушение менструального цикла;
- трудности с зачатием.
Симптомы проявления эндометриоза крайне разнообразны. Наиболее частый симптом — ноющая боль внизу живота, возникающая циклически. Часто её интенсивность возрастает во второй половине менструального цикла и во время менструации. По мере прогрессирования заболевания боли становятся изнурительными, приобретают постоянный характер с иррадиацией в промежность и ноги. Часто при этом снижается настроение, работоспособность, возникает депрессия и хроническая усталость. Одним из симптомов проявления эндометриоза — нарушение менструальной функции: мажущие выделения до и после менструации, нерегулярные менструации. Установлено, что около 40% женщин с эндометриозом страдают бесплодием, которое возникает как вследствие гормонального дисбаланса, так и из-за изменённого эндометрия, а в ряде случаев из-за спаечного процесса (при локализации очагов в брюшной полости).
Диагностика эндометриоза
Точно диагностировать эндометриоз помогает целый комплекс методов:
Показатели опухолевых маркеров в анализе крови. При эндометриозе яичников показатели маркеров СА 125, РЭА и СА 19-9 часто бывают увеличены в несколько раз.
На УЗИ диагност может увидеть эндометриальные очаги и кисты.
Самой высокой точностью обладает лапароскопический метод – он позволяет точно определить наличие и локализацию очагов эндометриоза, спаек и кист. Кроме того с помощью лапароскопии можно одномоментно удалить диагностированные очаги и кисты, разделить спайки.
В диагностике эндометриоза, кроме оценки жалоб и объективного статуса, врачу гинекологу помогает картина ультразвуковой диагностики, которую можно для уточнения диагноза сделать не только в стандартные 5-7 день цикла, но и повторить на 21-24 дни цикла, когда более чётко видны косвенные признаки данного заболевания. Кровь на маркёры СА-125 и СА-19-9 часто несколько повышены при эндометриозе, но не являются специфическими, так как это маркёры всех онкологических процессов. Их комбинация увеличивает чувствительность диагностики, но тоже даёт 10% ложноположительных результатов. Таким образом, ни один из биомаркёров не специфичен для диагностики заболевания. Единственный точный метод — лапароскопия с обнаружением эндометриоидных очагов.
Лечение эндометриоза
К сожалению, в ряде случаев эндометриоз — препятствие для зачатия: обширные очаги заболевания могут провоцировать образование спаек в органах малого таза. Это препятствует оплодотворению и продвижению оплодотворенной яйцеклетки в матку. Кроме того, спаечный процесс может стать причиной внематочной беременности. Поэтому в ряде случаев перед планированием беременности необходим курс лечения от эндометриоза.
На сегодняшний день существует два основных метода лечения болезни:
Гормональное – врач рекомендует прием гормональных средств (в некоторых случаях достаточно правильно подобранных гормональных контрацептивов), которые на время блокируют работу яичников, останавливая циклический рост и разрушение клеток эндометрия;
Лечение эндометриоидной болезни зависит от степени поражения, локализации очагов и необходимости сохранения репродуктивной функции. У молодых женщин это чаще всего гормональная терапия, которая направлена на подавление менструаций и уменьшение клинических симптомов заболевания. Оперативное лечение показано при сопутствующем бесплодии как этап подготовки перед планируемой беременностью.
Эндометриоз и беременность
Планировать зачатие врачи разрешают, как правило, в самое ближайшее время после лечения. Затягивать не следует, ведь уменьшившиеся или хирургически удаленные очаги могут вернуться снова. Если же эндометриоз не препятствует зачатию, врач может порекомендовать нерожавшей женщине в качестве терапии… беременность и грудное вскармливание. Во время беременности и лактации останавливаются циклические гормональные процессы в организме женщины, на смену им приходят совсем другие, направленные на вынашивание и сохранение беременности. Разрастание эндометрия также останавливается, а в некоторых случаях даже идет вспять.
Признаки эндометриоза уменьшаются либо вовсе исчезают на весь период беременности и лактации, однако после окончания грудного вскармливания патологические процессы в эндометрии могут снова возникнуть, поэтому контроль над этим заболеванием необходим.
Так как эндометриоз брюшной полости часто приводит к образованию спаечного процесса, то вероятность внематочной беременности при такой ситуации достаточно велика. Сама беременность влияет на течение эндометриоза благоприятно, как и длительная лактация, потому что именно в это время не происходят циклические гормональные колебания, приводящие к ухудшению течения заболевания.
Наружный генитальный эндометриоз (НГЭ) встречается у 5–10% женщин репродуктивного возраста. Частота выявления этого заболевания при лапароскопии, в том числе проводимой с целью уточнения причины бесплодия, составляет 45–55%. Среди обращающихся в центры вспомогательных репродуктивных технологий для проведения ЭКО более 35 % пациенток имеют наружный генитальный эндометриоз. При выработке плана ведения больных бесплодием, ассоциированным с эндометриозом, следует учитывать возраст женщины, продолжительность бесплодия, наличие боли и стадию заболевания.
Несмотря на углубленные исследования проблемы бесплодия, обусловленного эндометриозом, сформированы отдельные гипотетические механизмы взаимосвязи этих состояний, к которым относят изменение нормальной анатомии тазовых органов, эндокринные нарушения, патологические гормональные и клеточно-опосредованные функции эндометрия, изменение функции париетальной и висцеральной брюшины, отсутствие овуляции, гиперэстрогения, хроническое воспаление и иммунные расстройства. При эндометриозе среди выявленных молекулярных механизмов бесплодия следует отметить многоуровневое негативное влияние эндометриоза на последовательные этапы формирования ооцитов, процессы оплодотворения, раннего эмбриогенеза и имплантации. Фолликулогенез при наличии наружного генитального эндометриоза характеризуется нарушениями стероидогенеза, синтеза простагландинов, присутствием повышенного количества иммунокомпетентных клеток (B-лимфоцитов, NK-клеток, измененным соотношением моноцитов − макрофагов).
Провоспалительные изменения фолликулярной жидкости оказывают влияние на оогенез, при этом фиксируют удлинение фолликулиновой фазы, уменьшение размера доминантного фолликула и активацию апоптоза клеток фолликула. На процесс оплодотворения может оказывать негативное влияние измененный состав перитонеальной жидкости, которая нарушает подвижность сперматозоидов, вызывает активацию апоптоза сперматозоидов, препятствует адекватной акросомальной реакции и прикреплению к яйцеклетке. В перитонеальной жидкости больных эндометриозом повышено содержание активированных макрофагов, ИЛ-1, туморонекротического фактора (ТНФ), протеаз, антиэндометриальных 17 аутоантител и лимфоцитов.
В последнее время уделяется особое внимание эпигенетическим механизмам бесплодия при эндометриозе: показано, что гиперметилирование HOXA10 и HOXA11 генов, ответственных за рост и пролиферацию de novo, децидуализацию эндометрия, приводит к резистентности к прогестерону в эутопическом эндометрии. Таким образом, эндометриоз приводит к альтерации функции ооцита, сперматозоида, эмбриона, эндометрия вследствие дефектного синтеза факторов роста, рецепторов, что приводит к нарушению трансдукции.
Прогрессирование эндометриоза ухудшает прогноз наступления беременности. Показания к проведению экстракорпорального оплодотворения (ЭКО) и переноса эмбриона (ПЭ) при эндометриозе − освобождение гамет и эмбрионов от негативного влияния провоспалительных агентов перитонеальной жидкости. Хирургическое лечение повышает частоту наступления беременности. Кроме того, в ходе лапароскопии подсчитывают ряд показателей индекса фертильности при эндометриозе (Endometriosis fertility index (EFI), предложенного G.D. Adamson. EFI является простым и надежным клиническим инструментом, фактически единственной изученной классификационной системой, имеющей прогностическое значение. С помощью него можно предсказать время наступления беременности у больных эндометриозом после хирургического лечения, использовать выжидательную тактику у пациенток с хорошим прогнозом и не тратить попусту время и сразу же переходить к процедурам вспомогательных репродуктивных технологий при неблагоприятном прогнозе.
Комбинированное лечебное воздействие хирургического вмешательства:
- эндоскопическая диагностика, биопсия, оперативное вмешательство с удалением пораженной ткани (кист яичников, лазеро-, крио- термодеструкция очагов эндометриоза, разделение спаек) с максимальным сохранением овариальной ткани (овариального резерва);
- медикаментозное воздействие с достижением антигонадотропного эффекта;
- контроль за эффективностью лечения.
Медикаментозное лечение бесплодия, связанного с эндометриозом:
- если больной эндометриозом показано ЭКО, аГнРГ в комбинации с возвратной гормональной терапией в течение 3–6 месяцев лечения перед его проведением, то это повышает частоту наступления беременности;
- если медикаментозное лечение бесплодия, связанного с эндометриозом в виде гормонального подавления, неэффективно, то его не следует предлагать пациентке.
Длительность медикаментозного лечения эндометриоза определяется:
особенностями клинической картины заболевания (характер болевого синдрома, выраженность нарушений менструального цикла, состояние репродуктивной функции);
конечной целью лечения (улучшение качества жизни и здоровья в целом, наступление беременности).
Кумулятивная частота наступления беременности, в течение первого года ожидаемого зачатия колеблется от 50 до 20% при I–II стадии НГЭ и снижается на 4% каждый последующий год. Отказ от выжидательной тактики и проведение внутриматочной инсеминации спермой мужа/донора значительно увеличивают частоту наступления беременности и родов, особенно при использовании гонадотропинов для стимуляции овуляции. Подавление функции яичников после хирургического лечения с целью восстановления репродуктивной функции при I–II стадии НГЭ неэффективно и может быть предложено только перед проведением процедур вспомогательных репродуктивных технологий.
Удаление или уничтожение (аблация) эндометриоидных очагов в сочетании с адгезиолизисом с целью улучшения фертильности при минимальной и умеренной степени эндометриоза более эффективны, чем диагностическая лапароскопия. Операция должна быть выполнена специализированной бригадой хирургов с учетом необходимости сохранения овариального резерва и оптимизации объема операции.
Показания к использованию ВРТ непосредственно после оперативного лечения эндометриоза:
- сочетание НГЭ с трубно-перитонеальным фактором;
- субфертильная сперма мужа;
- возраст женщины более 35 лет;
- безуспешность других методов лечения.
Риск рецидива не должен являться причиной отказа от использования методов ВРТ после хирургического лечения, так как даже при III–IV стадии заболевания рецидив наружного генитального эндометриоза сравнительно редко возникает после стимуляции суперовуляции в программе ЭКО.
При эндометриоидных кистах яичников важно рассмотреть желание пациентки сохранить фертильность, чтобы определить степень вмешательства и при необходимости сохранить яичники и их функцию. У пациенток, не заинтересованных в беременности, целесообразно начать терапию КОК (лучше в непрерывном режиме) после хирургического удаления эндометриодных кист яичников. Лапароскопическая цистэктомия у больных бесплодием при установленном диагнозе рекомендована при размере кист более 2 см с целью уточнения диагноза, уменьшения риска инфекции, улучшения доступа к созревающим фолликулам при ЭКО, исключения отрицательного воздействия содержимого кисты на процесс овуляции и оплодотворения, что очень важно, с целью исключения злокачественного процесса − при любых размерах образования. Важно учитывать высокую вероятность снижения овариального резерва после оперативного лечения кист яичников. Оперативное вмешательство на яичниках с доказанным гистологическим диагнозом в анамнезе – может служить основанием для назначения гормональной терапии без повторного хирургического вмешательства (при небольших размерах кист или эндометриозе брюшины). Необходимо полное обследование – онкомаркеры, УЗИ с доплерографией для соблюдения онкологической настороженности.
Преимущества использования аГнРГ в схемах стимуляции суперовуляции у больных генитальным эндометриозом:
- более синхронное созревание фолликулов;
- повышение показателей имплантации;
- более частое наступление беременности при проведении ЭКО и ПЭ.
При выполнении программы ЭКО и ПЭ у больных наружным генитальным эндометриозом предпочтение следует отдавать схемам стимуляции суперовуляции с использованием ежедневно вводимых препаратов а-ГнРГ.
Факторами, повышающими эффективность реализации программы ЭКО и ПЭ у пациенток с наружным генитальным эндометриозом, являются:
- двухэтапное комбинированное (хирургическое и медикаментозное) лечение заболевания до проведения программы ЭКО при III–IV стадии распространения;
- отказ от выжидательной тактики и проведение ЭКО и ПЭ непосредственно после завершения лечения женщинам с агрессивным рецидивирующим течением заболевания в возрасте старше 35 лет, со сниженными функциональными резервными возможностями яичников и при сочетании НГЭ с аденомиозом.
Таким образом, генитальный эндометриоз в зависимости от локализации и стадии распространения оказывает негативное влияние на активность процессов фолликуло-, оогенеза и раннего эмбриогенеза. Наличие наружного генитального эндометриоза III-IV стадии распространения, оперативное вмешательство на яичниках (при наличии кистозных форм в момент обследования), снижение их функциональных резервных возможностей и сочетание наружного генитального эндометриоза с аденомиозом любой стадии распространения значительно ухудшают эффективность реализации программы ЭКО и ПЭ. Следует помнить, что для больных эндометриозом тяжелой формы, у которых беременность наступила с использованием процедур вспомогательных репродуктивных технологий, характерны высокие акушерские риски: преждевременные роды, преэклампсия, замедление внутриутробного развития плода, предлежание плаценты. Получены убедительные клинические данные в пользу переноса одного, а не двух и более эмбрионов у таких женщин, поскольку многоплодная беременность существенно повышает риск невынашивания.
Хирургический этап лечения бесплодия при наличии эндометриоза заключается, прежде всего, в восстановлении нормальных анатомических взаимоотношений органов малого таза и удалении эндометриоидных кист яичников. Допустимо проведение только коагуляции очагов эндометриоза, расположенных вблизи мочеточника, сосудов и на стенках полых органов без их тотального иссечения. Это позволяет снизить риск развития тяжелых осложнений у пациенток, основной жалобой которых является бесплодие. Необходимо проведение тщательного сальпингоовариолизиса, гемостаза и проверки проходимости маточных труб. Целесообразно использовать противоспаечные барьеры для предотвращения развития трубно-перитонеального бесплодия. Нецелесообразно проведение повторных операций с целью восстановления естественной фертильности. Это неоправданно затягивает продолжительность лечения в целом и снижает эффективность ЭКО. При планировании ЭКО хирургическое лечение, предусматривающее удаление эндометриоидных кист и проведение сальпингэктомии при необратимых изменениях маточных труб, осуществляют в качестве подготовки. Спорным и не всегда оправданным является удаление обширного эндометриоидного позадишеечного инфильтрата или эндометриоза мочевого пузыря при отсутствии болевого симптома как этапа подготовки к ЭКО. Это значительно повышает риск развития послеоперационных осложнений, но при этом не оказывает существенного влияния на частоту наступления беременности. При хирургическом лечении необходимо использовать лапароскопический доступ, исключением могут быть только тяжелые формы эндометриоза либо экстрагенитальные заболевания, являющиеся противопоказанием к проведению лапароскопии. Важным компонентом хирургического лечения эндометриоза является предотвращение образования спаек путем минимизации травмирования тканей.
Основные принципы хирургического лечения с позиций доказательной медицины:
