Вопросы планирования и ведения беременности при сопутствующей хронической соматической и неврологической патологии чрезвычайно актуальны с учетом того, что современный уровень развития медицины позволяет добиться стойкой ремиссии основного заболевания. И
Вопросы планирования и ведения беременности при сопутствующей хронической соматической и неврологической патологии чрезвычайно актуальны с учетом того, что современный уровень развития медицины позволяет добиться стойкой ремиссии основного заболевания. Идеальный вариант — когда напоминанием о заболевании является лишь регулярный прием медикаментов, а клинические проявления патологии практически отсутствуют. На этом фоне больная женщина стремится быть полноправным членом социума и ощутить в полной мере радость материнства. Очень важно, что современные технические возможности позволяют при помощи новых неинвазивных методик мониторировать развивающуюся беременность, объективно отслеживать комплекс морфометрических, функциональных и биохимических показателей, отражающих развитие беременности. Однако, в связи с решением женщины, больной эпилепсией, завести ребенка, у акушеров-гинекологов и врачей смежных специальностей часто возникает масса проблем.
Эпилепсия является хроническим заболеванием головного мозга, в лечении которого за последние годы достигнут определенный прогресс, в частности в области ведения беременности. Кафедра нервных болезней лечебного факультета совместно с Московским областным НИИ акушерства и гинекологии в результате совместных исследований выпустила методические указания по ведению беременности у больных эпилепсией женщин [2].
Практические неврологи и эпилептологи должны проводить постоянную, планомерную работу среди больных эпилепсией женщин, учитывая возможное их материнство. В своей работе вопросы контрацепции и беременности мы обсуждаем с больной девочкой и ее родственниками, начиная с пубертатного периода, для того чтобы они были полностью информированы о проблеме. Прежде всего обсуждаются вопросы контрацепции. Дело в том, что все препараты, обладающие энзиминдуцирующими свойствами (карбамазепин, фенобарбитал, гексамидин, бензонал, дифенин, этосуксимид) снижают эффективность гормональных контрацептивов, поэтому одновременный прием антиэпилептических препаратов (АЭП) и комбинированных эстрогенгестагенных гормональных контрацептивов в 8–10% случаев может приводить к возникновению нежелательной беременности [7]. В данной ситуации следует рекомендовать использовать барьерный метод контрацепции либо применять гормональные препараты с повышенным содержанием эстрогенов, однако данный аспект лучше обсудить с гинекологом-эндокринологом. Не снижают эффективность оральных контрацептивов такие препараты, как бензодиазепины, депакин, кеппра, ламиктал, топамакс (последний в терапевтической дозе до 200 мг/сут), поэтому их совместное назначение с гормональными контрацептивами не снижает эффективности последних.
Касаясь непосредственно проблемы беременности, прежде всего следует акцентировать внимание самой женщины и ее родственников на том, что беременность у больных эпилепсией должна планироваться.
Для успешного протекания беременности у больной эпилепсией женщины необходимо тесное сотрудничество невролога, акушера-гинеколога, генетика, терапевта, самой больной и ее родственников.
Основная цель медикаментозного лечения эпилепсии — достижение ремиссии заболевания. Однако это совершенно не означает, что больным эпилепсией женщинам нельзя беременеть при повторяющихся припадках. Дело в том, что фокальные без вторичной генерализации эпилептические приступы считаются безопасными для плода. Поэтому, если не удалось достигнуть полной ремиссии заболевания, но удалось исключить генерализованные судорожные припадки, можно считать, что задача подготовительного этапа неврологом частично решена. Следует помнить, что существует прямая зависимость между дозой АЭП и частотой врожденных уродств, а также между числом генерализованных припадков и частотой врожденных аномалий, следовательно, задача терапии заключается в достижении медикаментозной ремиссии при минимальной дозе АЭП. Если же удалось исключить генерализованные судорожные припадки, а дальнейшее наращивание дозы препарата не приводит к существенному эффекту, то следует ограничиться данной минимальной терапией.
Генерализованные судорожные припадки сопровождаются грубыми аноксически-ишемическими нарушениями, в частности маточно-плацентарного кровообращения [3], поэтому их частое возникновение у больной является противопоказанием к беременности. Кроме того, противопоказаниями к беременности являются:
- труднокурабельная эпилепсия с частыми генерализованными припадками;
- статусное течение заболевания;
- выраженные изменения личности больной эпилепсией.
Беременность показана в случаях:
- стойкой медикаментозной ремиссии заболевания;
- при субкомпенсации с редкими приступами.
Вместе с тем прогноз исхода беременности в корреляции со сроками при однократных и редких генерализованных судорожных припадках до настоящего времени не изучен.
Задача акушера-гинеколога — добиться нормализации менструальной функции (до 40% пациенток с фокальной эпилепсией имеют различные отклонения длительности и характеристик менструального цикла). Следует проводить лечение анемии (по нашим данным, она наблюдается у больных с эпилепсией в 37,2% случаев) [8]. Предпочтительно использовать препарат ферро-фольгамма (по 1–2 капсуле 3 раза в сутки, курсами до 6 нед). При приеме препаратов, обладающих энзиминдуцирующими свойствами (карбамазепин, фенобарбитал, дифенин и др.), возможно повышение уровня ферментов (ЛДГ, АСТ, АЛТ, ГГТ и ЩФ). Рекомендуется использовать гепатопротектор эссенциале (по 2 капсулы 3 раза в сутки, курсами по 4 нед).
Задача генетика заключается в консультировании беременной с целью исключения наследственной патологии. При идиопатических генерализованных эпилепсиях вероятность наследования ребенком эпилепсии достигает 10%, при симптоматических парциальных — несколько выше, чем в популяции (2–3%).
Больная эпилепсией женщина должна осуществлять регулярный прием АЭП, приходить на осмотр к неврологу и акушеру-гинекологу в соответствии со схемой наблюдения. До зачатия и в период до 13 нед беременности пациентка должна принимать фолиевую кислоту в суточной дозе не менее 3 мг, обычно в составе комплексных поливитаминных препаратов.
При компенсированном состоянии эпилепсии с ремиссией эпилептических припадков регулярность наблюдения неврологом составляет 1 раз в 2 мес, акушером-гинекологом — согласно нормативам. При наблюдающихся парциальных припадках регулярность наблюдения неврологом — 1 раз в 1 мес; акушером-гинекологом — 1 раз в 2 нед. Больные эпилепсией должны знать, что им следует обращаться к эпилептологу при любом учащении эпилептических припадков. Причинами учащения либо утяжеления припадков могут быть недосыпание, соматическая патология, в том числе положительный водный баланс, нарушение медикаментозного режима и др.
ЭЭГ-исследование и определение концентрации АЭП проводятся при компенсированном течении эпилепсии 1 раз в 2 мес, при наблюдающихся припадках — при каждом обращении беременной к неврологу.
Концентрации гормонов фетоплацентарного комплекса (плацентарный лактоген, прогестерон, эстриол, кортизол) и a-фетопротеин исследуются начиная с конца первого триместра беременности и в дальнейшем не реже 1 раза в месяц.
Динамическое УЗИ плода проводится при постановке беременной на учет, в 19–21-ю неделю (для исключения аномалий развития плода) и в дальнейшем 1 раз в 4 нед. Начиная с 20-й недели беременности, учитывая высокий риск развития фетоплацентарной недостаточности, при УЗИ целесообразно проводить допплерометрическое исследование кровотока в артерии пуповины, аорте и средней мозговой артерии плода. При проведении УЗ-фетометрии необходимо учитывать факт возможного влияния на них АЭП.
С учетом определенного риска развития врожденной патологии (все противоэпилептические препараты считаются потенциально тератогенными) обязательным является консультация генетика до 17-й недели беременности и при показаниях дополнительно проводятся биопсия хориона, амниоцентез с определением концентрации a-фетопротеина в амниотической жидкости и цитогенетическим исследованием.
Начиная с 26-й недели беременности показано проведение кардиотокографического исследования с объективной оценкой показателей моторики матки и состояния плода.
Диагностика и лечение фетоплацентарной недостаточности проводится по стандартным схемам. С определенной осторожностью необходимо использовать пирацетам из-за возможного провоцирования припадков.
При компенсированном течении эпилепсии особенностей в проведении пренатальной подготовки нет. Показаниями к досрочному родоразрешению на фоне эпилепсии являются склонность к серийному течению припадков, эпилептический статус.
Эпилепсия не является противопоказанием для родов через естественные родовые пути. Эпилептический статус, учащение эпилептических припадков в предродовом периоде, а также неблагоприятная отрицательная динамика состояния плода являются показаниями к проведению кесарева сечения.
Медикаментозное ведение родов и их обезболивание при эпилепсии не отличаются от обычного.
Противопоказания к проведению эпидуральной анестезии очень редки, в частности при нарушении циркуляции спинно-мозговой жидкости вследствие перенесенной патологии с вовлечением ликвороциркуляторных пространств.
В связи с риском обострения эпилепсии в послеродовом периоде настоятельно рекомендуется соблюдение регулярности приема АЭП и режима отдыха.
Снижение потребности в АЭП после родов обусловливает вероятность их передозировки вплоть до развития интоксикации. Появление у родильницы сонливости, нистагма, атаксии требует срочного исследования концентраций АЭП. Интоксикация АЭП обусловлена относительным повышением концентрации АЭП вследствие снижения общей массы роженицы, кровопотери в родах, изменения абсорбции препаратов и некоторыми другими факторами. Обычно достаточно в послеродовом периоде возвратиться к суточной дозировке АЭП, применявшейся до беременности (в случаях, если суточная доза АЭП во время беременности повышалась).
Согласно рекомендациям международных экспертов, сразу после рождения ребенка ему необходимо внутримышечно ввести витамин К в дозировке 1 мг/кг веса [4].
При сохраняющихся парциальных припадках рекомендуется постоянное нахождение с роженицей кого-то из родственников.
Отказ от грудного вскармливания новорожденного совершенно не обоснован, так как во время беременности попадание АЭП в кровь ребенка обычно выше, чем с молоком матери. Кормление грудью необходимо осуществлять в положении лежа, для того чтобы в случае развития припадка избежать травмы.
Перечислим основные АЭП, применяемые при лечении беременных, больных эпилепсией.
Вальпроевая кислота. Среднесуточная дозировка может колебаться в пределах 600–3000 мг (15–30 мг/кг/сут и более), желательно использовать препарат c контролируемым высвобождением активного вещества депакин хроно и 2-кратный прием. По последним данным, полученным в результате популяционных исследований, дозировка вальпроевой кислоты до 1000 мг/сут не оказывает тератогенного действия [5]. Прием во время беременности вальпроевой кислоты приводит в 1–2% случаев к развитию у новорожденных дефекта нервной трубки (spina bifida aperta), а по некоторым данным, частота этой патологии даже достигает 2,5%. В результате высокого сродства препарата к транспортным протеинам концентрация его в грудном молоке достигает всего 2–3% — самый низкий показатель среди применяющихся в настоящее время АЭП.
Во время беременности суммарная концентрация вальпроевой кислоты сыворотки крови существенно не меняется. Назначение вальпроевой кислоты в первый триместр беременности из-за угрозы дефектов развития спинного мозга необходимо проводить с осторожностью, мониторируя маркеры дизонтогенеза ЦНС (a-фетопротеин, ацетилхолинестеразу) и проводя ультразвуковое исследование плода в более поздние сроки беременности.
Карбамазепин. Обычно взрослым препарат назначается в дозировке 400-2400 мг/сут (8–20 мг/кг/сут). Используется минимально эффективная доза при 3–4-кратном приеме во время беременности либо формы препарата с пролонгированным высвобождением активного вещества (тегретол ЦР, финлепсин ретард). Наши исследования показали, что использование карбамазепина в дозировке до 10 мг/кг часто бывает достаточным для компенсации эпилепсии и в то же время не отражается на показателях фетоплацентарного комплекса [6]. Прием карбамазепина во время беременности может приводить к порокам развития плода: врожденному вывиху бедра, паховым грыжам, гипоспадиям, врожденным порокам сердца и спинного мозга. Риск врожденного дефекта нервной трубки при приеме карбамазепина во время беременности достигает 0,5–1,0%. Сочетанное применение карбамазепина и вальпроевой кислоты во время беременности приводит к наивысшей частоте врожденных мальформаций, поэтому данного сочетания следует избегать.
Фармакокинетика карбамазепина во время беременности характеризуется относительной стабильностью свободной фракции препарата, и поэтому в большинстве случаев не возникает необходимости повышения дозы АЭП.
По последним данным, проникновение карбамазепина в молоко матери достигает 45% от содержания в крови.
Фенобарбитал. Препарат продолжает достаточно широко применяться в терапии эпилепсии. Его суточная дозировка обычно составляет 60–240 мг (1–3 мг/кг/сут) при 2-кратном приеме.
Относясь к категории АЭП, индуцирующих систему цитохрома Р-450, фенобарбитал, как и карбамазепин, снижает эффективность гормональных контрацептивов. По этой же причине препарат может приводить к дефициту у новорожденного витамина К.
По некоторым данным, во время беременности концентрация фенобарбитала снижается приблизительно у 1/3–1/2 всех больных, получающих монотерапию препаратом. В послеродовом же периоде, напротив, концентрация его может существенно возрастать. Поэтому, несмотря на длительный период полужизни препарата, рекомендуется следить за динамикой его концентрации во время беременности и в послеродовом периоде: учащение припадков, появление признаков передозировки либо побочных проявлений требует немедленной коррекции дозы.
Согласно последним данным, в материнское молоко поступает около 40% препарата, циркулирующего в крови матери. У новорожденных вследствие слабости ферментных систем печени период полужизни препарата может существенно варьировать от 75 до 275 часов, что необходимо учитывать при кормлении ребенка грудью. Применение фенобарбитала во время беременности может приводить как к седативным проявлениям у новорожденного (сонливость, слабое сосание груди, мышечная гипотония), так и к синдрому отмены, если по каким-либо причинам вскармливание грудным молоком не проводится либо прерывается.
Дифенин (фенитоин). В последние годы этот препарат применяется реже, однако в практической медицине продолжает использоваться достаточно широко. Суточная дозировка дифенина обычно составляет 200–600 мг (4–7 мг/кг/сут) при 2–3-кратном приеме. Относящийся к категории ферментиндуцирующих АЭП, он может приводить к дефициту у новорожденного витамина К.
Фармакокинетика фенитоина во время беременности характеризуется понижением концентрации преимущественно в третьем триместре беременности, особенно при сочетании с другими АЭП, поэтому может возникать необходимость в повышении дозы. В послеродовом же периоде доза фенитоина должна быть снижена до исходной.
В материнское молоко поступает до 20% препарата, циркулирующего в крови матери.
По предлагаемой методике за 15-летний период наблюдалось свыше 90 беременных, страдающих эпилепсией. В удовлетворительном состоянии родилось 92% детей. Эффективность предложенной методики ведения больных эпилепсией беременных позволяет рекомендовать ее к широкому применению в практическом здравоохранении.
По вопросам литературы обращайтесь в редакцию.
П. Н. Власов, доктор медицинских наук, профессор
МГМСУ, Москва
- 10446
- 8,1
- 3
- 2
Как лечить эпилепсию — задача по сей день нерешенная.

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Эпилепсия и ее терапия

Эпилепсия является патологией, известной человечеству еще в древности (падучая болезнь — одно из первых названий этого недуга; лечили ее изгнанием бесов из тела жертвы — говорят, некоторым помогало; рис. 1). Она может затрагивать сенсорные, моторные, вегетативные функции, память, поведение, эмоциональный статус, восприятие, речь, поведение. Само определение болезни вызывало споры на протяжении долгого времени, пока, наконец, в 2005 г. Международная лига борьбы с эпилепсией не утвердила следующие постулаты:
- Эпилепсия является общим названием для целой группы заболеваний, отражающих последствия дисфункции мозга.
- Эпилепсия — это мозговое расстройство, характеризующееся стойкой предрасположенностью к возникновению припадков и их нейробиологическими, когнитивными, психологическими и социальными последствиями.
- Эпилептический припадок — это кратковременное проявление признаков и/или симптомов, относящихся к аномально чрезмерной или синхронной нейрональной активности мозга.
- Для постановки диагноза требуется хотя бы один эпилептический припадок.
Сегодня около 2% людей во всем мире страдают от эпилепсии, что характеризует ее как одно из самых распространенных неврологических заболеваний. Если не вдаваться в подробности, то возникновение эпилептического припадка вызывается дисбалансом тормозной (основной медиатор — γ-аминомасляная кислота, ГАМК) и возбуждающей (основной медиатор — глутамат) систем головного мозга [8]. Перед припадком действие глутамата намного пересиливает действие ГАМК в какой-либо области мозга, и нейроны этой области начинают генерировать электрические импульсы не разрозненно, как это происходит обычно, а синхронно. Возникает т.н. эпилептический очаг, где клетки разряжаются одновременно. На электроэнцефалограмме (ЭЭГ) можно наблюдать ужасающую картину (рис. 2).

Рисунок 2. Сравнение электроэнцефалограмм здорового пациента и пациента с ювенильными миоклоническими судорогами (одной из форм наследственной эпилепсии, проявляющейся в пубертате).
Прием лекарств является в настоящее время первой и самой важной частью лечения эпилепсии. Обычно рекомендуется начинать с монотерапии противоэпилептическими препаратами (ПэП), что позволяет подавитьприкадки или хотя бы минимизировать частоту приступов у 50–70% пациентов. Для лечения пациентов, которым монотерапия не помогает, используется политерапия, т.е. сочетание нескольких антиконвульсантов. Среди часто используемых ПэП можно назвать вальпроевую кислоту, вигобатрин, тиагабин, ламотриджин, окскарбамозепин, фельбамат, топирамат, габапентин, леветирацетам, зонисамид, прегабалин. Если же медикаментозное лечение не помогает и в этом случае, то используют крайние меры: хирургическое иссечение эпилептогенного очага, кетогенную диету и глубокую вагусную стимуляцию мозга [16], [19].
Для многих ПэП сначала было показано их антиконвульсаторное (т.е., препятствующее возникновению припадка) действие, а затем уже начали выяснять конкретный механизм, по которому препарат предотвращает развитие припадка. Например, лекарство может влиять на работу потенциал-чувствительных ионных каналов и не давать клетке возможность генерировать потенциал действия; может усиливать влияния ГАМК-ергичекой системы, вызывать ослабление влияния глутаматергической системы через рецепторы медиатора, может влиять непосредственно на высвобождение медиаторов. Для части лекарств характерно сочетание нескольких вышеприведенных механизмов [8], [16].
Однако одновременно с изучением терапевтической активности препаратов начали выявляться серьезные побочные эффекты, характерные для ПэП. Поэтому лечение в каждом случае должно подбираться индивидуально, с учетом особенностей конкретного пациента. Особую группу риска представляют женщины-эпилептики детородного возраста, потому что для них стоит не только вопрос, как забеременеть (ПэП изменяют обмен веществ организма и его гормональный фон), но и как сохранить здоровье будущему ребенку — ведь все ПэП тератогенны, т.е. вызывают у ребенка и физические, и умственные дефекты.
Вальпроевая кислота
Одним из самых широко применяемых и изученных препаратов для лечения эпилепсии является вальпроевая кислота. Она помогает в разных дозах пациентам при практически всех разновидностях судорог, в любом возрасте, и именно ее назначают врачи, когда нужно купировать (заблокировать) припадок у пациента с неизвестной этиологией заболевания.
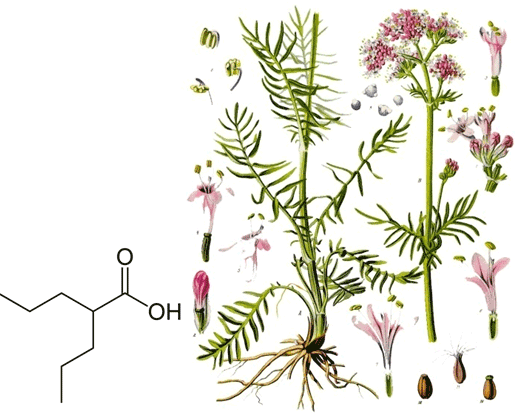
Рисунок 3. Вальпроевая кислота. Слева — химическая структура вальпроевой кислоты. Справа — Валериана лекарственная, из которой ее получают.
Вальпроевая кислота (встречается в литературе как ВПК или анион соли вальпроат) — производное валерьяновой кислоты, получаемой из эфирного масла травянистого растения валерианы лекарственной (Valeriana officinalis). ВПК была открыта в 1882 году Бартоном (B. Burton), но только в 1963 году было обнаружено ее противосудорожное действие. На сегодня, вальпроевую кислоту используют не только в спектре эпилептических заболеваний, но и при лечении биполярных нарушений, старческой деменции, лейкемии, шизофрении, мигрени, депрессиях. Антиэпилептическое действие препарата обычно связывают с тем, что он повышает тормозную активность ГАМК через увеличение ее синтеза и уменьшение деградации. Также показано нейропротекторное действие вальпроата [1], [8]. Известно, что в зоне судорожного очага нейроны повреждаются, но при введении ВПК до припадка или сразу после него, доля погибших клеток намного снижается, и снабжение клеток питательными веществами (нейротрофика) усиливается. (В частности, такое действие наблюдалось в гиппокампе — части головного мозга, ответственной за формирование памяти и ориентировки в пространстве.)
Однако лечение вальпроатом оказывает и непосредственное негативное воздействие на организм пациента-эпилептика, причем, чем выше доза препарата, тем больше обнаруживается нарушений в организме. Если говорить о самых частых проявлениях, то это увеличение массы тела, метаболические осложнения, уменьшение ночной продолжительности сна, панкреатит, острая печеночная недостаточность, коагулопатии, различные реакции гиперчувствительности, энцефалопатия, эмоциональные расстройства, депрессия, нарушения функционирования эндокринной и репродуктивной систем. Последнее особенно отчетливо проявляется у женщин: синдром поликистоза яичников, нарушения фармакокинетики пероральных контрацептивов, нарушения менструального цикла [2], [19]. Кроме того, ВПК затрудняет процесс имплантации эмбриона на начальных стадиях беременности, понижая экспрессию необходимых для этого белков (ламинина, коллагена-IV и виментина) [6]. И именно вальпроевая кислота является самым опасным препаратом для беременных женщин: она легко проникает через плацентарный барьер [3] и вызывает множество необратимых изменений зародыша.
В 1984 году впервые был описан фетальный вальпроатный синдром [4], при котором характерно возникновение мальформаций (структурных дефектов; рис. 4) сердечно-сосудистой и мочеполовой систем, скелета, черт лица; появляются аномалии глаз и центральной нервной системы (самое типичное для вальпроата — незакрытие нервной трубки), респираторного тракта [7], [18]. Само физическое развитие после рождения замедляется: дети меньше весят и медленнее растут, чем их сверстники. Частота таких явлений при монотерапии ВПК в три раза выше по сравнению с монотерапией любым другим ПэП.

Рисунок 4. Мальформации при фетальном вальпроатном синдроме.
Встает вопрос: что же может принести больший вред ребенку? Эпилептический припадок матери во время беременности (а это как минимум резкое уменьшение поступления кислорода в мозг плода, как максимум — его гибель) или лекарственная терапия для предотвращения развития этого припадка? Рассматривая статистику, подсчитанную для людей, на этот вопрос ответить практически невозможно. Поэтому проводят исследования на моделях животных, — в частности, на крысах.
Автор этой статьи взяла четыре группы крыс:
- Контрольная группа.
- Группа, получающая вальпроат натрия внутрибрюшинно в течение всего первого триместра беременности.
- Группа, у которой два раза за первый триместр — до и после имплантации зародыша в стенку матки — вызывались эпилептические припадки классическим химическим конвульсантом пентилентетразолом (ПТЗ), ингибитором постсинаптического торможения нейронов центральной нервной системы.
- Группа, которой вводился как вальпроат натрия каждый день первого триметра, так и дважды вводился ПТЗ (но судороги на фоне ВПК не развивались).
Оказалось, что неблагоприятные исходы беременностей присутствовали во всех группах, кроме контрольной (для группы, получавшей ВПК, — 87,8%; для группы, подвергшейся эпилептическим припадкам вследствие введения ПТЗ, — 50%, для группы, получавшей и ВПК, и ПТЗ, — 100%), однако только у крысят, подвергавшихся только действию ВПК in utero, наблюдалось сильное замедление физического развития (критерии: открытие глаз, набор массы и рост вплоть до взрослого состояния) и увеличение тревожности в поведенческих тестах. Также крысятам уже в выросшем состоянии проводилась МРТ-диагностика, опять же выявившая нарушения в основном в группе, получавшей только вальпроат: на рис. 5 крупные белые пятна на верхней линейке рисунков означают расширение желудочков мозга. Уменьшаются объемы и изменяется клеточная структура многих частей головного мозга:
- таламуса (посредник передачи сенсорных и моторных сигналов в кору головного мозга из низлежащих отделов нервной системы);
- бледного шара и стриатума (это базальные ядра, часть экстрапирамидальной системы, участвуют в планировании и осуществлении движений, влияют на мышечный тонус);
- миндалины (часть лимбической стстемы, отвечает не только за формирование положительных эмоций, но и за чувство страха, агрессии, беспокойства);
- гиппокампа (отвечает за пространственную ориентацию и перезапись информации из кратковременной памяти в долговременную, его объем достоверно уменьшался во всех группах по сравнению с контролем).

Рисунок 5. Томографические срезы мозга двухмесячных крыс, получавших ВПК пренатально в первом триместре (A—D), и крыс из контрольной группы (E—H), режим Т2 RARE. Явственно видны расширения желудочков мозга у опытной группы.
исследование автора статьи
Таким образом, мы можем говорить о том, что пренатальное действие вальпроата может влиять на физическое развитие плода и изменять структуру головного мозга на всю последующую жизнь, затрагивая и моторные функции, и процесс формирования эмоций, и память, и поведение в целом, и это воздействие куда более губительно, чем действие самого припадка.
В других исследованиях обнаружено, что крысята, подвергавшиеся in utero действию ВПК (доза 600–800 мг/кг), меньше весили, их развитие замедлялось, они обладали пониженной болевой чувствительностью и, напротив, повышенной чувствительностью к неболевым стимулам, локомоторной гиперактивностью и стереотипией в сочетании с низкой исследовательской мотивацией, пониженным уровнем социального поведения; у них наблюдалось уменьшенное акустическое преимпульсное ингибирование (т.е. снижение моторной реакции на резкий звук). Обычно такие же нарушения выявляют в патологиях аутизма [12], [14].
Сейчас все активнее исследуют влияние вальпроата не только на животных моделях, но и на людях, изучая статистику отклонений и проводя психологические тесты. Корреляцию между внутриутробным влиянием ВПК и развитием заболеваний спектра аутизма можно считать доказаной: IQ у детей дошкольного и школьного возрастов и склонность с общению ниже нормы, внимание и обучаемость нарушены [11], [15], [17].
Заключение: иметь или не иметь?
Но почему же просто не использовать другие ПэП или не создавать новые, когда ясно, на что именно надо действовать? За последние тридцать лет было создано более 15 новых лекарств от эпилепсии. Однако предсказать побочные эффекты при длительном применении, используя классические доклинические модели на животных (с использованием того же пентилентетразола) порой очень трудно. (Как пример можно привести токсическое воздействие при длительном применении фелбамата и вигабатрина.) Также ко многим новым лекарствам вырабатывается привыкание, и пациенту приходится менять лечение (что уже само по себе нехорошо). И, что самое главное, на 20–30% пациентов ПэП нового поколения вообще не действуют [10].
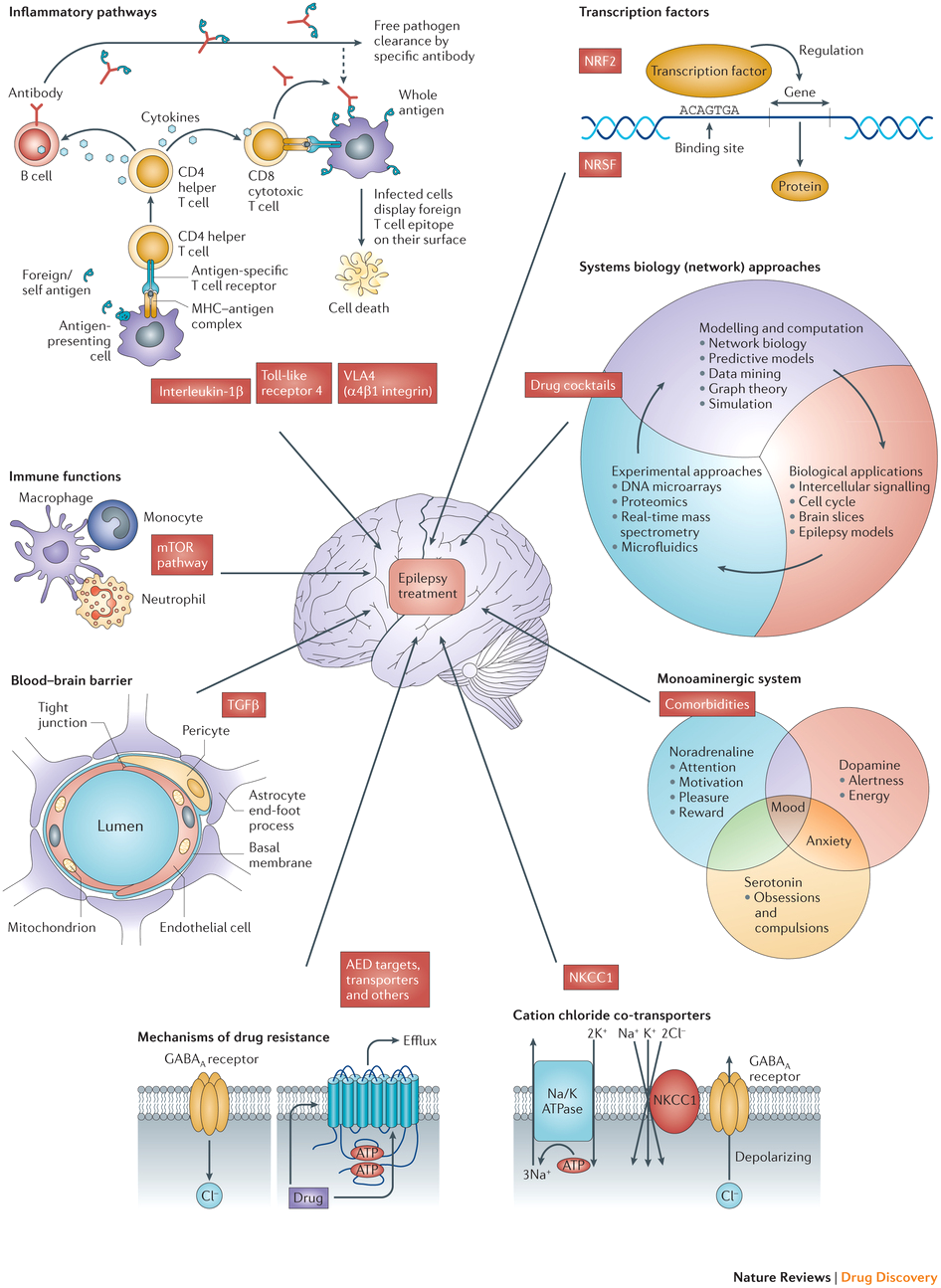
Рисунок 6. Новые молекулярные мишени, являющихся зоной повышенного интереса для будущих исследований эпилепсии.
Удлиняется и корректируется доклиническая часть исследований, и разрабатываются усовершенствованные модели эпилепсии на животных. Часть из новых ПэП уже не дает некоторых побочных эффектов (например, габапентин (Neurontin; Pfizer) или леветицерам (Keppra; UCB Pharma) не вызывают дерматологическую чувствительность). Внимание к проблеме эпилепсии со стороны общества становится все более пристальным, появляется даже спонсирование из частных фондов. Так что, кажется,
О, сколько нам открытий чудных
Готовят просвещенья дух
И опыт, сын ошибок трудных,
И гений, парадоксов друг,
И случай, бог изобретатель.
А.С. Пушкин
